Clear Sky Science · tr
ABEL-FRET, A2A adenosin reseptörünün yapısal dinamiklerinin tek molekül ölçümlerinde zaman ölçeği boşluğunu kapatıyor
Hücrenin Küçük Anahtarlarını Gerçek Zamanında İzlemek
Günümüz ilaçlarının birçoğu, reseptör adı verilen hücre yüzeyindeki moleküler “anahtarları” çevirerek etki gösterir. Bu anahtarlar sinyalleri açıp kapatırken sürekli şekil değiştirir; fakat çoğu araç sadece en hızlı veya en yavaş hareketleri görebilir—her ikisini birden değil. Bu makale, çözeltide tek bir ilaç hedefi reseptörünü öncekinden çok daha uzun süre izlemeyi sağlayan bir yöntem sunuyor ve ilacın etkisi açısından kritik olan belirli konformasyonlarda nasıl uzun süre kaldığını ortaya koyuyor.
Bu Şekil Değiştiren Proteinler Neden Önemli
Çalışma, G proteinine bağlı reseptörler (GPCR'ler) olarak bilinen önemli bir hücre yüzeyi proteinleri sınıfına odaklanıyor. Bu proteinler görme, ruh hali, kan basıncı ve bağışıklık tepkileri gibi hayati süreçleri kontrol eder ve onaylanmış ilaçların üçte birinden fazlası bunlara etki eder. İyi incelenmiş üyelerden biri olan A2A adenosin reseptörü uyku, ağrı, iltihaplanma ve beyin sinyalleşimini düzenlemeye yardımcı olur ve Parkinson hastalığı ile kanser gibi bozuklukların tedavisi için umut verici bir hedeftir. GPCR'ler son derece esnektir: farklı moleküller bağlandığında reseptörü belirli yolları tercih eden farklı şekillere iter. Ancak bu esneklik, X-ışını kristalografisi veya kriyoharekete mikroskopisi gibi statik görüntülere dayalı ilaç tasarımını zorlaştırır.
Bir Reseptörü Sabitlemeden İzlemek
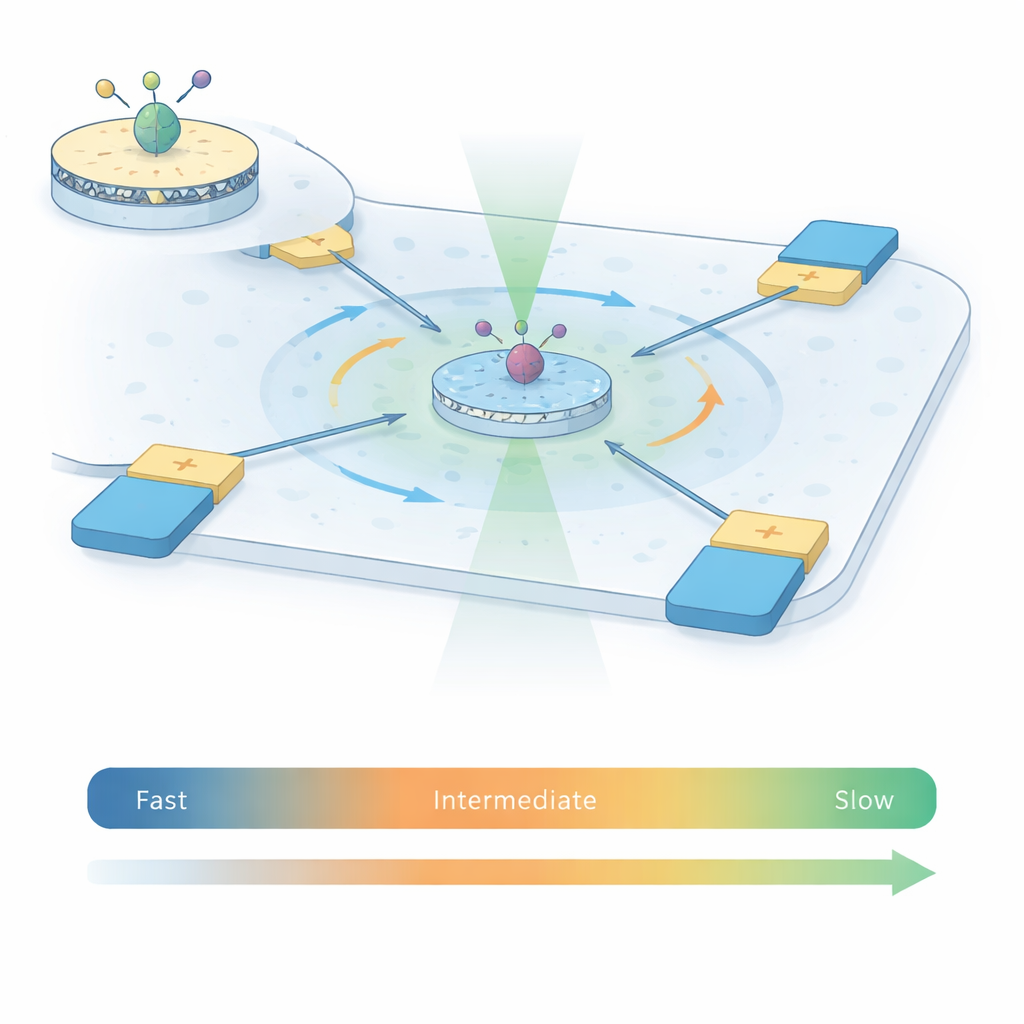
A2A reseptörlerinin nasıl hareket ettiğini yakalamak için yazarlar iki güçlü tekniği ABEL‑FRET adını verdikleri birleşik yaklaşımla birleştirir. Önce, tek reseptörleri nanodisk adı verilen yapay membran yamalarına tekrar yerleştirirler; bu, her proteine yalnız deterjan ortamından daha doğal bir çevre sağlar. Reseptörün iç tarafındaki iki hareketli bölgeye bir çift floresan boya bağlarlar. Reseptör şekil değiştirdikçe bu boyalar arasındaki mesafe ve göreli yönelim değişir ve aralarındaki enerji transferini—Förster rezonans enerji transferi (FRET) olarak bilinen olguyu—değiştirir. İkinci olarak, reseptörü bir yüzeye yapıştırmak yerine Anti‑Brownian Elektrokinetik (ABEL) tuzağı kullanırlar: nerede bir floresan parçacık olduğunu algılayan ve onu merkeze nazikçe geri iten elektrotlara sahip mikroakışkan bir hazne, böylece rastgele Brown hareketine karşı koyulur.
Kayıp Zaman Penceresini Köprülemek
Geleneksel tek‑molekül FRET deneyleri ya serbestçe difüze olan reseptörleri sadece birkaç milisaniyenin binlerde biri kadar izler ya da yüzeye immobilize edilmiş reseptörleri saniyelerden dakikalara kadar izler. Her yaklaşım farklı bir zaman penceresini kapsar. ABEL tuzağını kullanarak bu çalışma, bireysel A2A reseptörlerini çözeltide serbest kalırken bir ila iki saniye boyunca görünür tutar; bu, difüzyonla sınırlı deneylere göre yaklaşık 100 kat daha uzundur. Bu genişletilmiş izleme süresi, ekiplerin her bir tuzaklamada FRET sinyalinin nasıl dalgalandığını ve binlerce reseptör boyunca dört koşul altında—ligandsız, bir antagonist ile ve iki farklı aktive edici (agonist) molekül ile—nasıl değiştiğini ölçmesini sağlar. Varyans, korelasyon ve tekrarlanma analizleri gibi sinyal analizinden ödünç alınan istatistiksel araçlar, rastgele foton gürültüsünü reseptörün gerçek, yavaş yapısal değişikliklerinden ayırt etmelerini sağlar.
Gizli Uzun Ömürlü Konformasyonlar Ortaya Çıkıyor
FRET okumaları, reseptörlerin tipik bir kaç yüz milisaniyelik gözlem süresi boyunca tamamen birbirine dönüşmeyen birden çok ayrı konformasyon populasyonu barındırdığını gösterir. Tüm koşullarda FRET değerlerinin dağılımı yalnızca gürültüden beklenenden çok daha geniştir ve yapısal heterojenliği ortaya koyar: farklı moleküller farklı uzun ömürlü şekillerde bulunur. Aktive edici moleküller bağlandığında ortalama FRET seviyesi yukarı kayar; bu, reseptörün iç helikslerinin “aktif-benzeri” bir düzeninde daha fazla zaman geçirdiğini gösterir. Yine de korelasyon analizleri, bir reseptör yüksek veya orta FRET durumuna girdikten sonra yüzlerce milisaniye boyunca orada kalma olasılığının yüksek olduğunu ortaya koyar. Bu sonuçlar, daha hızlı deneylere dayanan önceki tahminleri günceller; uzun ömürlü durumlardaki karakteristik kalma sürelerini yalnızca milisaniyelerden onuncu saniyenin iyi üzerine uzatır.
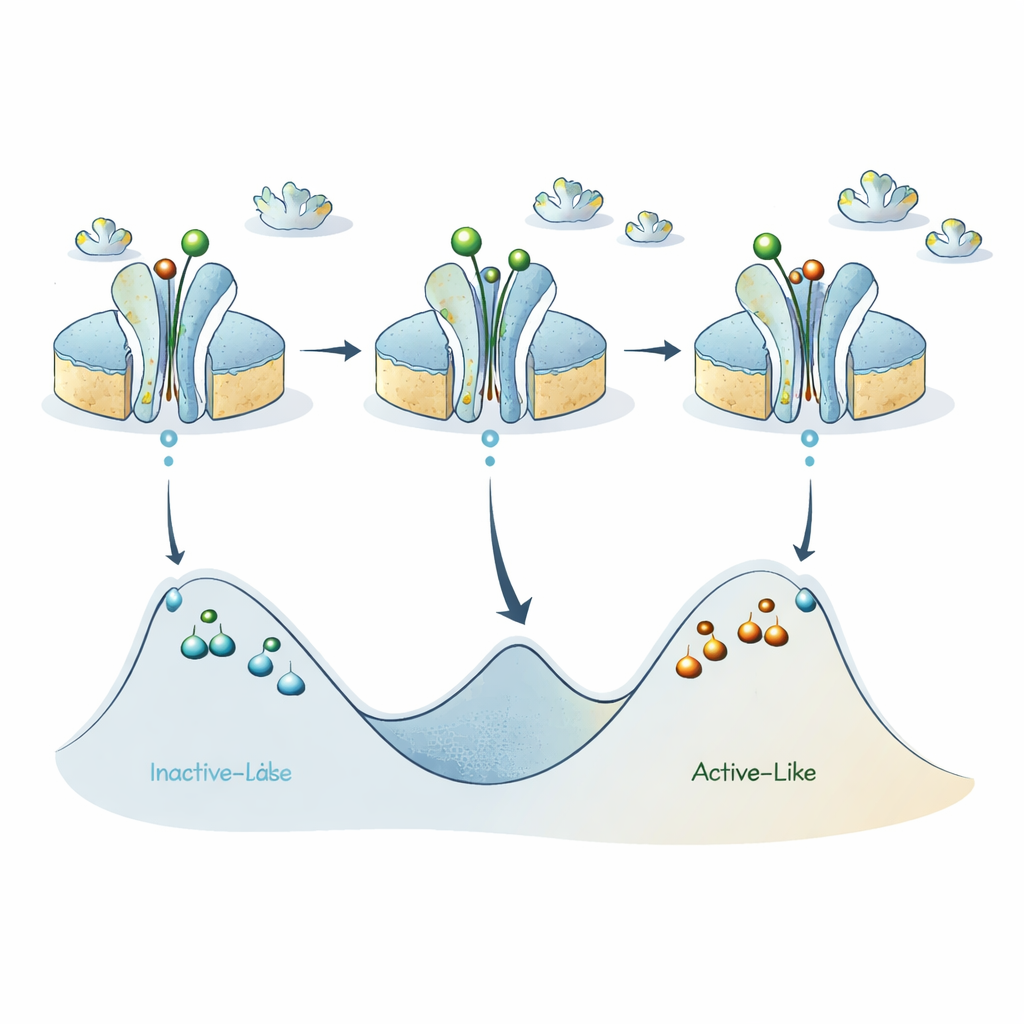
Reseptörün Enerji Peyzajının Yeni Bir Haritası
Bu parçaları bir araya getirdiklerinde yazarlar, A2A reseptörünün esasen inaktif-benzeri bir durum ile aktif-benzeri bir durum arasında geçiş yaptığı önceki modeli rafine ederler. Yeni veriler, bu iki geniş kategorinin her birinin aslında bir dizi alt-durumu barındırdığını ve bunların arasındaki enerji bariyerlerinin kayda değer olduğunu, böylece bireysel reseptörlerin aktif‑benzeri veya inaktif‑benzeri belirli bir versiyonda şaşırtıcı derecede uzun süre “takılı” kalabileceğini öne sürer. Aktive edici ligandlar ana inaktif ve aktif benzeri havzalar arasındaki bariyeri düşürerek alt-milisaniye ölçeğinde hızlı geçişleri teşvik eder, ancak her havza içindeki iç bariyerler yüksek kalır ve ABEL‑FRET'in tespit ettiği uzun ömürlü alt-durumlara yol açar.
Gelecek İlaçlar İçin Anlamı
Uzman olmayanlar için ana mesaj şudur: A2A reseptörü gibi bir ilaç hedefi basitçe “kapalı” ile “açık” arasında gidip gelmez. Bunun yerine, sinyallerin hücre içinde nasıl iletildiği ve ilaçların zaman içinde nasıl etki gösterdiği açısından önem taşıyan, bazıları yeterince uzun süre devam eden engebeli bir şekil peyzajı keşfeder. Bireysel reseptörlerin doğal, bağlı olmayan durumlarında daha uzun süre izlenebilmesini sağlayarak ABEL‑FRET, ultrahızlı ve çok yavaş ölçümler arasındaki kritik boşluğu doldurur. Bu yaklaşım artık birçok membran proteinine uygulanabilir ve potansiyel ilaç hedeflerinin nasıl nefes alıp verdiğine, kaydığına ve terapötik bileşiklere nasıl yanıt verdiğine dair daha eksiksiz, zaman çözünürlüklü bir resim sunar.
Atıf: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Anahtar kelimeler: G proteinine bağlı reseptörler, tek-molekül FRET, adenosin A2A reseptörü, protein konformasyonel dinamikleri, ABEL tuzağı