Clear Sky Science · tr
Hafif kontrollü, tek bileşenli ve organ-modüle edilebilir pDNA teslimi için azobenzen-köprülü iyonize edilebilir amfifilik Janus glikosidler
Daha Akıllı Gen Teslimine Işık Tutmak
Gen tedavileri, genetik kod parçacıklarını doğrudan hücrelerimize ulaştırarak hastalıkları kökünden tedavi etme vaadi taşır. Ancak bu hassas yükü kan dolaşımında güvenle yönlendirmek, doğru organlara ulaştırmak ve hedef hücrelerin içine sokmak hâlâ büyük bir engel. Bu çalışma, davranışı vücuda girmeden önce ışıkla değiştirilebilen yeni bir sınıf şeker bazlı parçacık tanıtıyor; bu sayede araştırmacılar terapötik bir genin nereye gideceğini ve ne kadar güçlü ifade edileceğini yeniden yönlendirebiliyor, üstelik hücrelere büyük zarar vermeden. 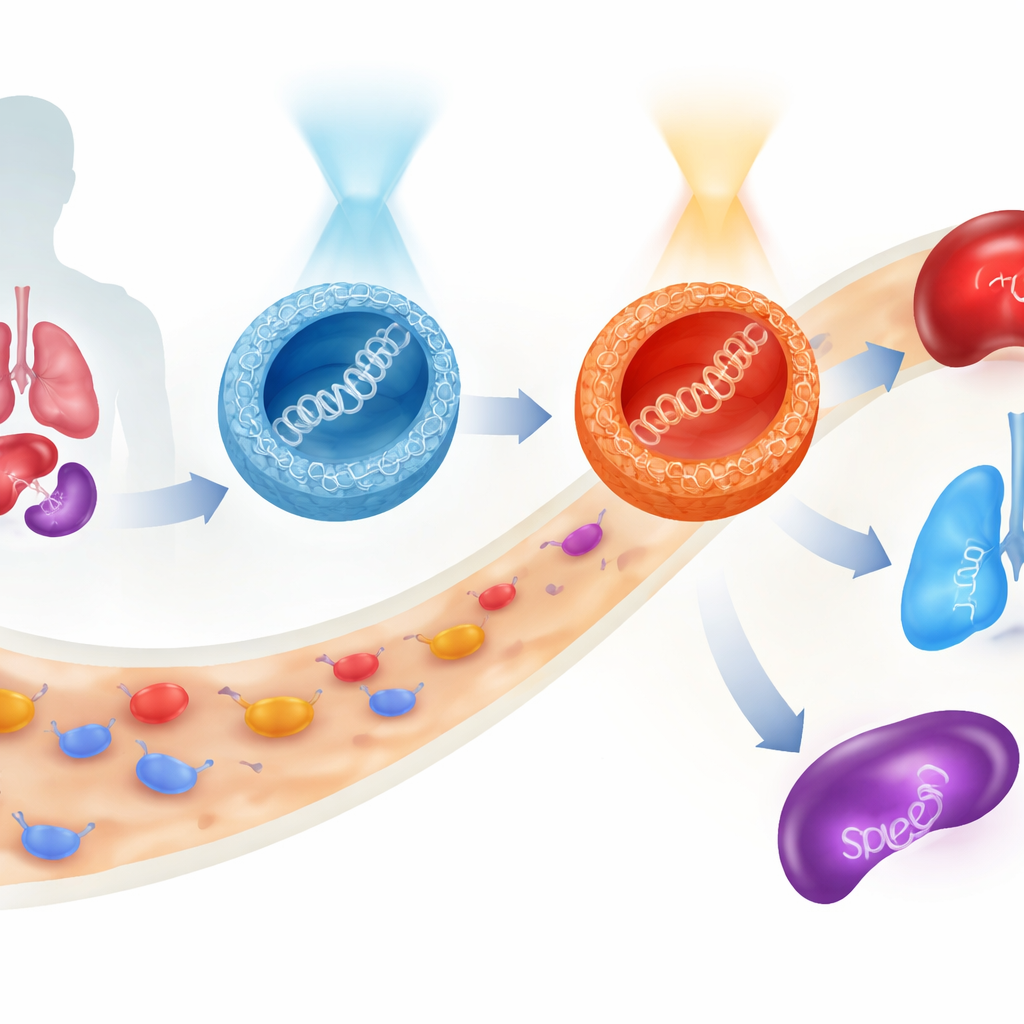
Hassas Gen Kurye Gereksinimi
Günümüzün en başarılı gen teslim araçları, mRNA COVID-19 aşılarının geliştirilmesine yardımcı olan lipid nanopartiküllerdir. Bu çok bileşenli damlacıklar nükleik asitleri sarıp korur, ancak genellikle karaciğerde birikirler ve yüklerinin yalnızca küçük bir kısmını hücre içine salarlar. Bileşimlerini ayarlamak hangi organları tercih ettiklerini değiştirebilir, yine de bu karışımlar karmaşıktır ve kesin kontrol zordur. Bu çalışmanın ekibi bunun yerine, öngörülebilir şekil ve davranışlarla kendiliğinden nanopartiküller oluşturan tek, iyi tanımlanmış moleküller tasarlamayı ve bunların dışarıdan basit bir ışık tetikleyicisiyle etkin olarak ayarlanabilmesini hedefledi.
Işıkla Kontrol Edilen Moleküler Terazi
Yeni sistemin merkezinde ikiz “Janus” glikosidler bulunuyor: iki glukoz biriminden inşa edilmiş, su sever yüklü başlara ve yağ seven kuyruklara sahip ve merkezi bir azobenzen “mafsal” ile birleştirilmiş moleküller. Azobenzen, farklı renklerdeki ışığa maruz kaldığında E ve Z olarak adlandırılan iki ayna-benzeri şekil arasında dönüşebilir. DNA içeren sulu ortamda, bu moleküllerin birçok kopyası kendiliğinden yumuşak, katmanlı parçacıklar halinde toplanarak plazmid DNA sarmallarını sarar. Araştırmacılar, şeker ile mafsal arasında stabiliteyi ve biyolojik davranışı hafifçe ayarlamak için oksijen köprüleri içeren ve kükürt köprüleri içeren iki versiyon hazırladılar. Çözeltileri önceden ışınlayarak ya E ya da Z formunu zenginleştirebildiler ve her bir durumun ortaya çıkan gen teslim partiküllerini nasıl şekillendirdiğini incelediler.
Şekil Değiştiren Parçacıkların Davranışı
Parçacık boyutu, yüzey yükü ve iç yapı ölçümleri, E ve Z durumları arasındaki ışık kaynaklı değişimin belirgin fiziksel sonuçları olduğunu gösterdi. Genel olarak Z formu, E forma kıyasla daha küçük, daha tekdüze şekilli nanopartiküller ve daha düzenli, katmanlı bir iç yapı üretti. Mikroskopi, bu iç düzenlemelerin lipid-benzeri malzeme ile DNA’nın dönüşümlü tabakalarına benzediğini ortaya koydu. Önemli olarak her iki durum da DNA’yı enzimatik parçalanmadan korudu. Böbrek, karaciğer ve bağışıklık dokusundan kültüre edilmiş hücrelerde, farklı izomer durumları aynı DNA’ya rağmen çarpıcı derecede farklı gen ifadeleri üretti. Parçacıklar hücrelere girdikten sonra uygulanan tekrar eden ışık darbeleri gen ifadesini birkaç kat artırdı; bu, şekil değiştirmenin verdiği mekanik dürtünün parçacıkların gevşemesine ve yüklerini salmasına yardımcı olduğunu ve ayrıca hücre içi kompartmanlardan kaçmalarına yardımcı olabileceğini düşündürüyor. 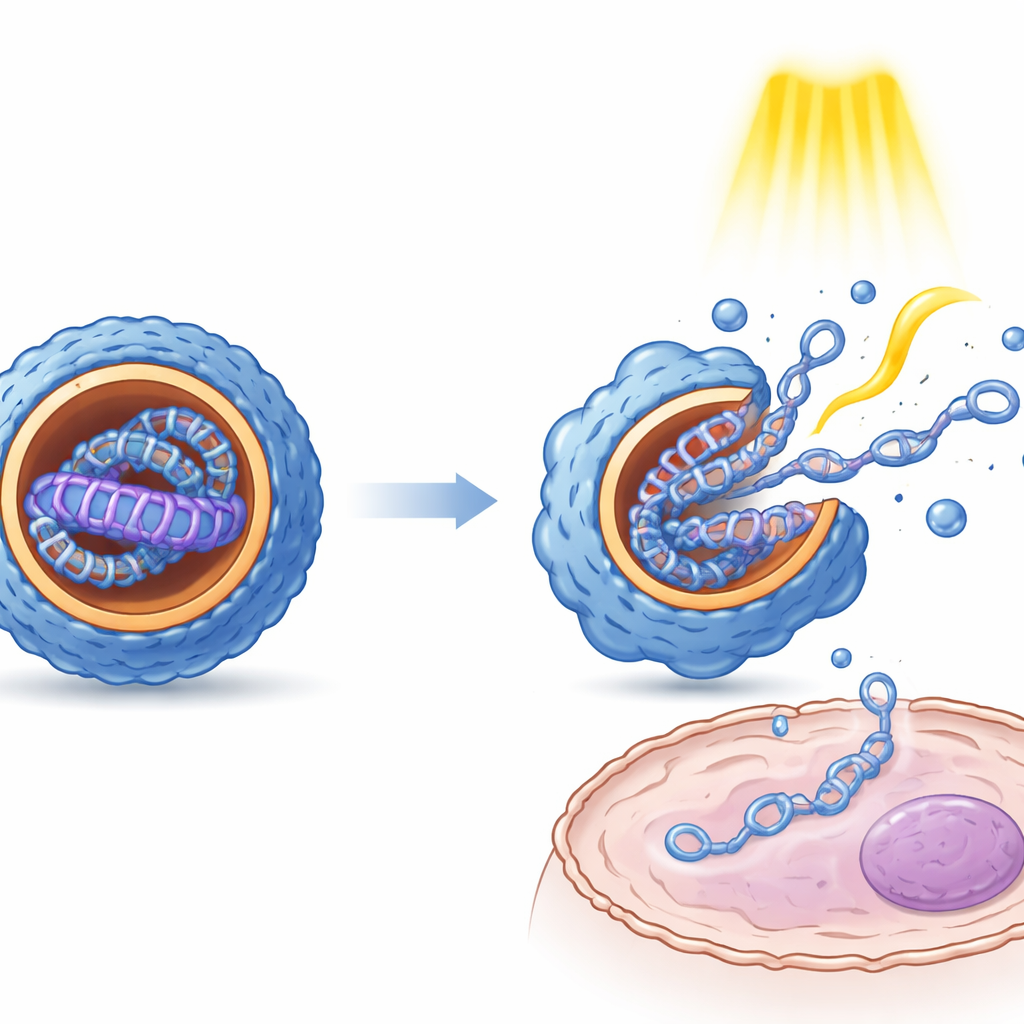
Genleri Belirli Organlara Yönlendirmek
En şaşırtıcı davranış farelerde görüldü. Oksijen-köprülü partiküller E açısından zengin formda verildiğinde, bir belirteç genin ifadesi çoğunlukla karaciğerde ve bir miktar akciğerde gerçekleşti. Enjeksiyon öncesi onları Z formuna geçirerek toplam ifade artmakla kalmadı, aynı zamanda dağılım akciğerlere kaydı. Kükürt-köprülü partiküller ise farklı bir tablo çizdi: onların Z formu dalgıç bir bağışıklık organı olan dalakta (splen) tercih gösterdi. Böylece aynı temel moleküler iskeletle —ve DNA yükünü değiştirmeden— araştırmacılar taşıyıcının bağını (oksijen veya kükürt) ve ışıkla aktive edilen şekli (E veya Z) seçerek gen aktivitesini ağırlıklı olarak karaciğer, akciğer veya dalak yönünde yönlendirebildiler. Bu testler boyunca hücre canlılığı yüksek kaldı; bu da sistemin nispeten nazik olduğunu düşündürüyor.
Geleceğin Gen İlaçlarına Işıkla Ayarlanabilir Bir Yol
Günlük anlatımla, ekip DNA için küçük, ışıkla anahtarlanabilir bir nakliye aracı inşa etti. Enjeksiyon öncesinde kısa bir ışık muamelesi ile bu araçlar iki şekilden birine “programlanıyor”. Her şekil karakteristik boyut ve yüzey hissine sahip nanopartiküller oluşturuyor; bu da hangi hücre tiplerine ne kadar güçlü yapıştıklarını ve vücutta nereye yerleşeceklerini belirliyor. Aynı kimyasal iskeletin birçok küçük değişiklikle uyarlanabilmesi ve geçişin tersinir olması ile DNA’nın kendisini değiştirmemesi sayesinde bu platform, gen terapilerinin nerede ve nasıl etki edeceğini ince ayarlarla kontrol etmeye esnek bir yol sunuyor. Klinik kullanıma ulaşmadan önce daha çok çalışma gerekse de, çalışma dikkatle tasarlanmış, ışıkla kontrol edilen tek moleküllü taşıyıcıların daha güvenli ve daha hassas gen ilaçları için güçlü araçlar olabileceğini gösteriyor.
Atıf: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Anahtar kelimeler: gen teslimi, ışığa duyarlı nanopartiküller, azobenzen anahtarları, hedefli DNA terapisi, nanotıp