Clear Sky Science · tr
S9 proteazı WprP2, RiPP biyosentezinde öncül peptitte tekdüze kesim katalizler
Hücrelerdeki küçük kesici aletlerin önemi
Bakteri içerilerinde, özelleşmiş moleküler makaslar uzun amino asit zincirlerini daha küçük, genellikle antibiyotik veya diğer yararlı doğal ürünlere dönüşen aktif parçalara böler. Bu çalışma, hedef peptidini olağanüstü bir hassasiyetle kırpan daha önce bilinmeyen bir kesici aleti — WprP2 adlı bir proteazı — ortaya koyuyor. Bu enzimin nasıl çalıştığını anlamak, bilim insanlarının yeni biyolojik etkin peptitler ve gelecek nesil antibiyotikler tasarlamasına yardımcı olabilir.
Ham zincirlerden tamamlanmış mini‑ilaçlara
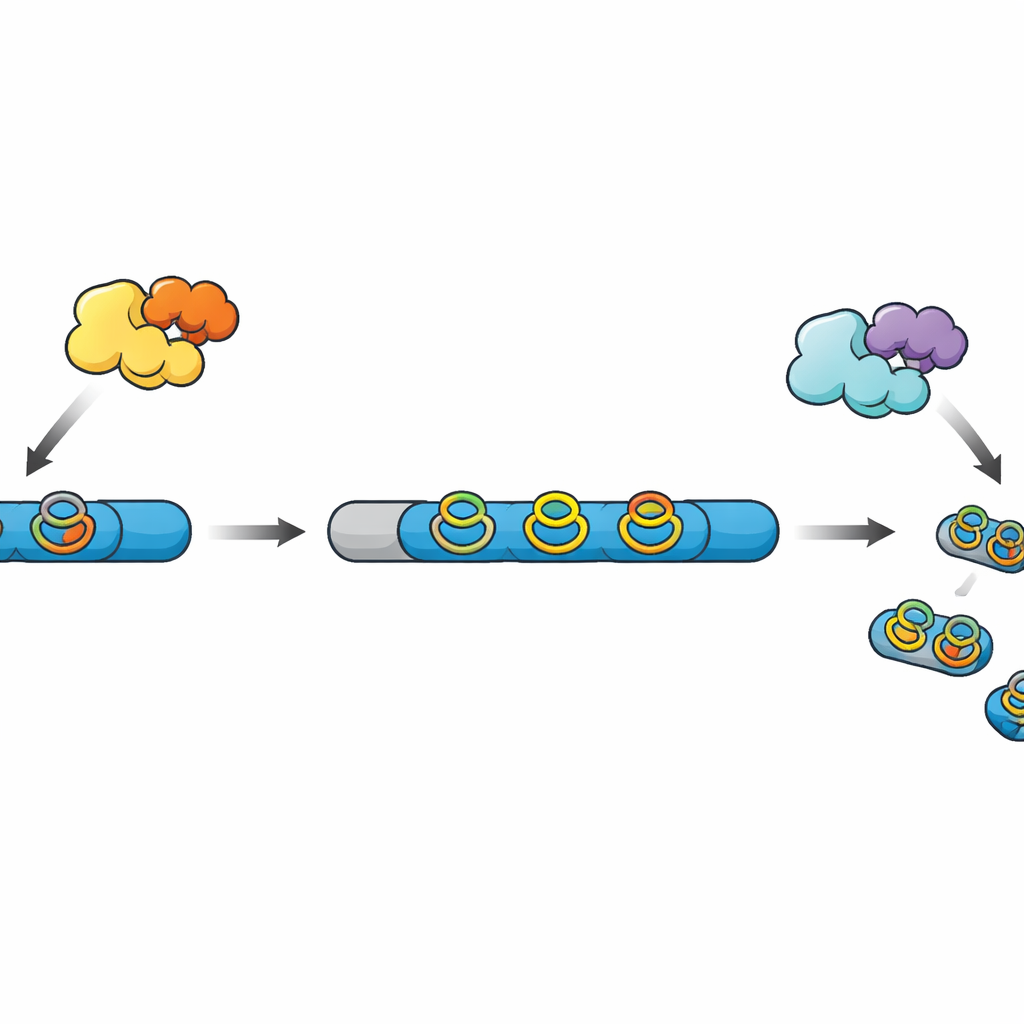
Toplu olarak RiPP'ler olarak bilinen birçok modern peptit bazlı doğal ürün, ribozomda üretilen basit zincirler olarak başlar. Bu zincirler, bir tutma yeri gibi davranan bir lider bölge ve bir dizi kimyasal yükseltmeden sonra nihai ürüne dönüşecek bir çekirdek bölge içerir. Diğer enzimler peptide çapraz bağlar ve halkalar ekleyerek onu daha kararlı ve daha aktif hale getirir ve son olarak bir proteaz lideri kesip olgun molekülü serbest bırakır. Yeni keşfedilen bir RiPP ailesinde, radikal SAM enzimleri aromatik aminoasitleri içeren sıkı “siklofan” halkaları oluşturur, ancak bilinen çoğu gen kümesinde eşleşen proteaz eksiktir ve son işlem adımları gizemli kalır.
Eksik eş enzimini iz sürme
Yazarlar daha önce öncül peptitte üç tekrarlayan WPR segmentinde aynı çapraz bağları kuran WprB1 adlı bir radikal SAM enzimi üzerinde çalışmışlardı. Yeni çalışmada, bu enzimin akrabalarını bakteri genomlarında aradılar ve yakın çevresinde proteaz kodlayabilecek genlere baktılar. Streptomyces venezuelae’de, benzer bir çapraz bağ kurucu enzim, yardımcı proteini, üç WPR tekrarı içeren eşleşen bir öncül peptit ve S9 ailesine ait aday bir serin proteaz olan WprP2’yi içeren umut verici bir küme buldular. Bu, peptidin olgun fragmanları serbest bırakmak üzere nasıl nihai olarak kesildiğini ortaya çıkarmak için ideal bir test sistemi oluşturdu.
Peptidin dilimlendiğini izlemek
WprP2’yi incelemek için ekip, öncül peptidi çapraz bağlayıcı enzimle birlikte ve onsuz olarak bakteride üretti, saflaştırdı ve ardından kontrollü in‑vitro reaksiyonlarda proteaz ile karıştırdı. Kütle spektrometrisi, WprP2’nin önce her WPR segmentinden hemen sonra zinciri kestiğini, ardından dizide daha ileriye doğru belirli bir prolin kalıntısından sabit bir mesafe önce ikinci bir kesim yaptığını ortaya koydu. Bu iki adım, bir dizi daha küçük, tekdüze fragman oluşturuyor. Dikkat çekici şekilde, WprP2 bu kesim desenini siklofan halkaları daha önce kurulsun veya kurulmasın gerçekleştirdi; bu da halkaların tanımada gerekli olmadığını gösteriyor. Belirli çapraz bağlı bölgeleri kesemeyen ticari tripsin ile karşılaştırıldığında bile WprP2 işlevini sürdürdü ve olağanüstü dayanıklılığını vurguladı.
Enzimin neyi tanıdığını çözmek
Araştırmacılar, WprP2’nin gerçekte peptitte hangi özellikleri okuduğunu sorguladılar. Kesim bölgelerinin etrafındaki tek tek amino asitleri sistematik olarak değiştirerek, birçok yakın kalıntının değiştirilmesinin az etkisi olduğunu, ancak WPR segmentindeki anahtar bir argininin veya ikinci kesim bölgesindeki glutamin ya da prolinin değiştirilmesinin o belirli adımı engelleyebileceğini buldular. Farklı kenarlandırıcı kalıntılara sahip ilişkili bir öncül peptit ile yapılan deneyler, proteazın WPR tekrarlarından sonra kesim yapmaya devam ettiğini ama yalnızca bir glutamin‑prolin çifti var olduğunda ikinci kesimi gerçekleştirdiğini gösterdi. AlphaFold3 kullanılarak oluşturulan bilgisayar destekli yapısal modeller bu görüntüyü destekledi: öngörülen komplekslerde WPR kaynaklı ve glutamin‑prolin bölgeleri sırayla enzimin katalitik merkezi ile hizalanıyordu; bu da ardışık iki adımlı bir mekanizmayla tutarlıydı.
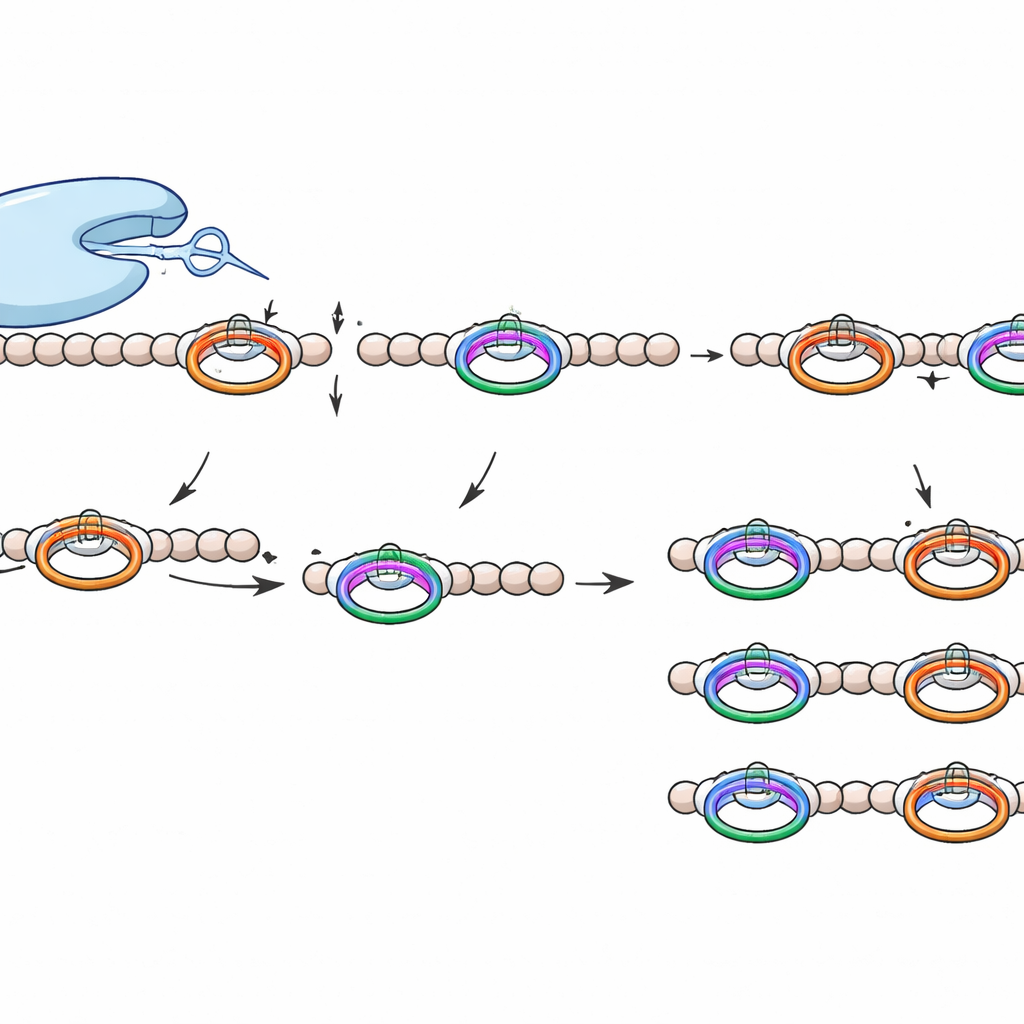
Bu kesici aleti özel kılan nedir
WprP2, tıbbi açıdan önemli enzimleri de içeren daha geniş S9 proteaz ailesine aittir, ancak birkaç yönden öne çıkar. Bir prolin kalıntısının N‑terminal tarafında kesim yapar, prolinin ardından değil; tekrar eden bir motife etki ederek tüm öncül zincir boyunca eşit boyutlu parçalar üretir; ve iki tanıma bölgesi arasındaki amino asitlere karşı geniş bir tolerans gösterir. Bu hassasiyet ve esneklik kombinasyonu, RiPP ilişkili proteazlarda daha önce görülmemiştir.
Bu keşfin nasıl kullanılabileceği
Basit dizi ipuçlarını tanıyan ve tekdüze, tekrarlı kesimler yapan bir proteazın ortaya konması, peptit mühendisliği için büyüyen araç setine güçlü yeni bir alet ekliyor. Pratik olarak, WprP2 tasarımcı peptitleri serbest bırakmak veya yeniden şekillendirmek için kullanılabilir; bunlar arasında tripsin gibi standart enzimlere dirençli karmaşık çapraz bağlara sahip olanlar da var. Uzman olmayanlar için çıkarılacak ana nokta, bilim insanlarının uzun peptid zincirlerini hassas, eşit boyutlu parçalara ayıran yeni bir tür moleküler makas keşfetmiş olmaları; bu da potansiyel antibiyotiklerin ve diğer biyolojik olarak aktif moleküllerin daha kontrollü üretimine kapı açıyor.
Atıf: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Anahtar kelimeler: RiPP peptitleri, serin proteaz, WprP2, siklofan doğal ürünleri, peptit mühendisliği