Clear Sky Science · tr
Onkojenik PI3Kα varyantları, mutasyona özgü gizli ceplere sahip dereceli konformasyon spektrumunu ortaya koyuyor
Tek Bir DNA Değişikliği Yeterli Olmayabilir
Kanser sıklıkla mutasyonların hastalığı olarak tanımlanır, ancak bu çalışma tüm mutasyonların tek başına hareket etmediğini gösteriyor. Araştırmacılar, büyüme kontrolünde kilit bir enzim olan PI3Kα’yı incelediler ve aynı gen kopyasında iki belirli DNA değişikliği birlikte gerçekleştiğinde, bu proteini tek başına olan değişikliklerden daha aktif şekillere itebildiklerini buldular. Bu önemli çünkü aşırı aktif PI3Kα yalnızca kanserleri tetiklemekle kalmaz, aynı zamanda iyi huylu aşırı büyüme sendromları ve beyin gelişim bozukluklarında rol oynar—ve bazı tümörlerin mevcut ilaçlara neden kötü yanıt verdiğini de açıklamaya yardımcı olur.
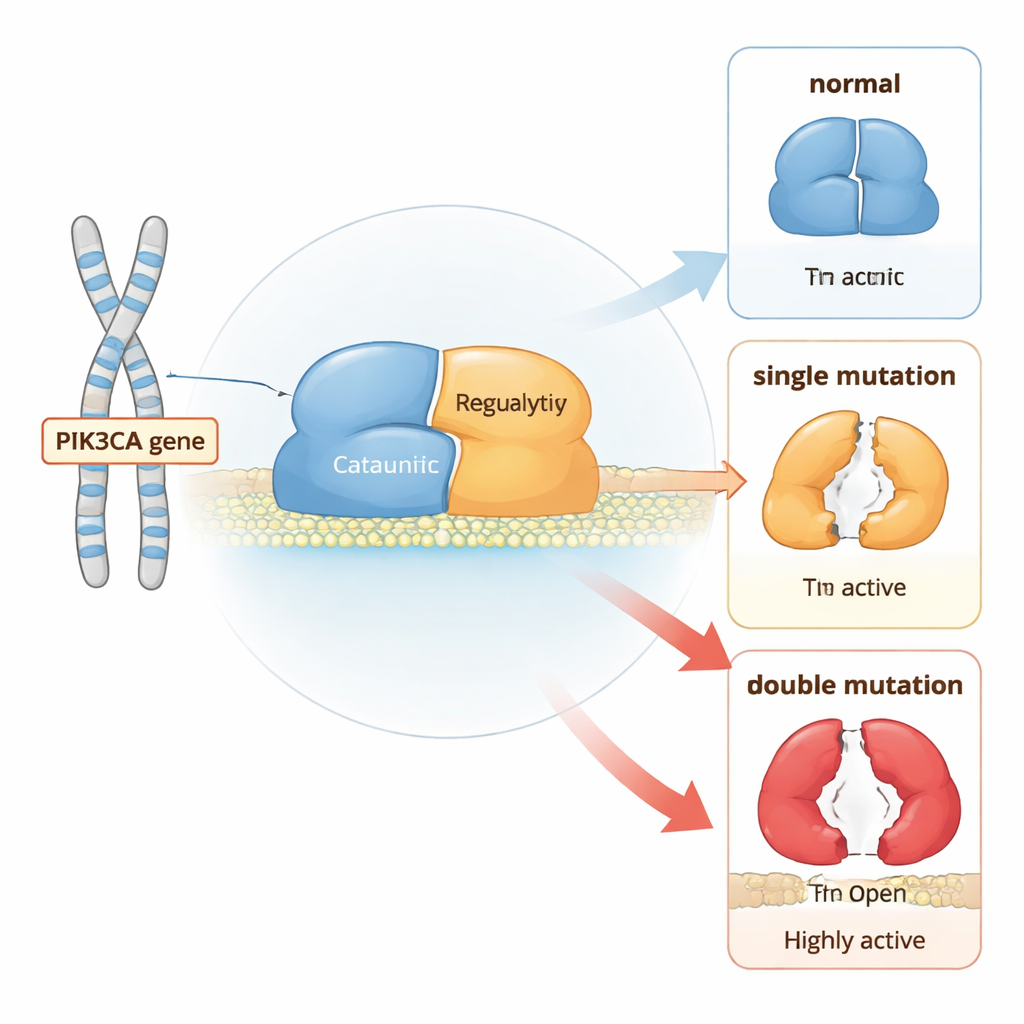
Hücre Büyümesi İçin Moleküler Bir Anahtar
PI3Kα, hücre zarına yakın duran ve büyüme sinyallerini ileten iki parçalı bir proteindir. Normal koşullarda, hücre yüzeyindeki reseptörler uyarılana kadar çoğunlukla “kapalı” konumda kalır. Ardından PI3Kα zara taşınır ve PIP2 adlı bir lipidi PIP3’e dönüştürerek hücreye büyüme ve bölünme talimatı verir. Kontrolsüz büyümeyi önlemek için proteinin birkaç bölgesi yerleşik frenler gibi davranır: bir bölge katalitik çekirdeği sıkıca kavrar, başka bir bölge esnek bir aktivasyon döngüsünü yakın tutar ve bir partner alt birim tüm kompleksi denetlemeye yardımcı olur.
Tekli ve Çift Mutasyonlar Dengeleri Nasıl Eğiyor
Yazarlar uzun, atom düzeyinde bilgisayar simülasyonları kullanarak normal PI3Kα’yı ya tekli “sıcak nokta” kanser mutasyonları taşıyan versiyonlarla ya da aynı molekülde bir sıcak noktayla birlikte daha zayıf bir mutasyon kombinasyonu içeren versiyonlarla karşılaştırdı. Her bir mutasyonun proteinin daha açık, daha aktif şekilleri ziyaret etme sıklığını değiştirdiğini, ancak çift mutasyonların dengeyi tekli mutasyonlardan çok daha ileri ittiğini buldular. Özellikle bazı mutasyon çiftleri, düzenleyici bir parçayı (nSH2 olarak adlandırılan) yerinde tutan temasları gevşetmek ve başka bir segmenti (iSH2) yer bağlanma noktasından uzaklaştırmak için birlikte çalışıyor. Bu koordine hareket katalitik çekirdeğin kilidini açar ve proteinin zara hareket edip sinyal vermeye başlamasını kolaylaştırır.
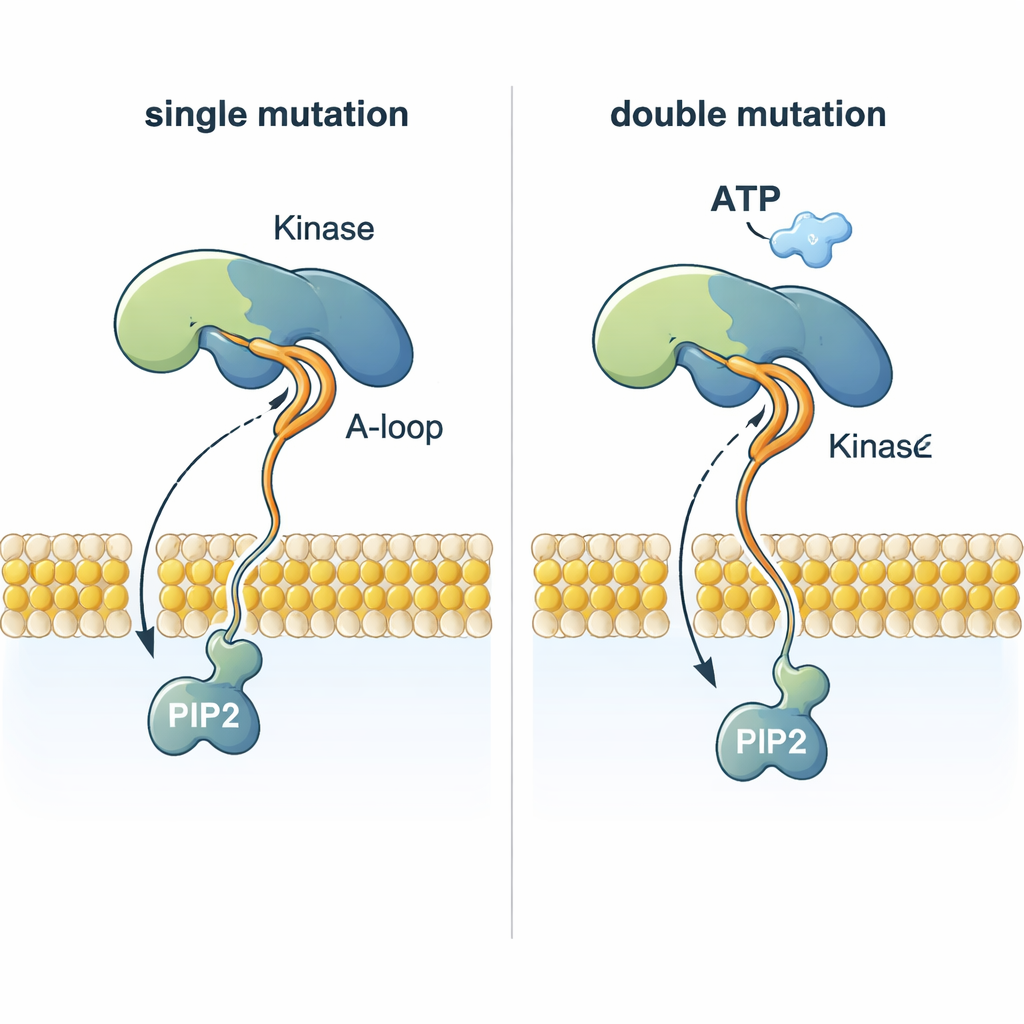
Substratın Reaksiyon Bölgesine Ulaşmasına Yardımcı Olmak
Çarpıcı bir bulmaca, PI3Kα’nın ATP’den—zarın yaklaşık 2 nanometre üzerinde duran—bir fosfat grubunu, zar içinde gömülü olan PIP2’ye nasıl ekleyebildiğidir. Simülasyonlar, belirli mutasyonların esnek bir aktivasyon döngüsünü yeniden şekillendirerek yüksek oranda pozitif yüklü bir bölümün zara doğru sivrildiğini gösteriyor. Bu döngü negatif yüklü PIP2 başını yakalayabilir, onu lipid tabakasından çekip ATP’ye doğru yönlendirebilir. Bir zar-dolaylışı mutasyon ile bu döngüyü değiştiren bir mutasyonun birleştiği çift mutantlar, PIP2’yi normal PI3Kα’ya veya tekli mutantlara göre çok daha verimli koordine ediyor; bu da aynı PI3Kα’da iki mutasyon bulunan tümörlerin neden özellikle agresif olabileceğine yapısal bir açıklama sunuyor.
Hareketle Ortaya Çıkan Gizli İlaç Bölgeleri
PI3Kα büyük ve esnek olduğu için aktif bölgeyi hedefleyen tek bir ilaç tüm mutant formlar üzerinde etkili olmakta zorlanır ve kan şekeri düzeylerinde ciddi değişiklikler gibi yan etkilere neden olabilir. Proteinin zaman içinde nasıl nefes alıp esnediğini izleyerek araştırmacılar “kriptik” cepleri—yalnızca belirli mutant şekillerde açılan ve statik kristal yapılarına görünmeyen geçici olukları—keşfettiler. Bu cepler, örneğin belirli çift mutantlarda en çok hareket eden bölgelere yakın, mutasyona özgü konumlarda ortaya çıkıyor. Bu da aktif bölgenin uzağında bağlanan, dikkatle tasarlanmış allosterik ilaçların tek tek mutant varyantları daha güvenli, daha az aktif konformasyonlara kilitlemek için uyarlanabileceğini gösteriyor.
Daha Akıllı Kombinasyon Tedavilerine Doğru
Genel olarak bu çalışma, kanser genetiğinde “bir iki darbesi” görüşünü destekliyor: güçlü bir sıcak nokta mutasyonu ile aynı PI3Kα molekülündeki daha zayıf bir partner, genellikle daha kötü klinik sonuçlarla ilişkilendirilen daha aktif şekillerin dereceli bir spektrumunu yaratabilir. Tedavi açısından yazarlar, tek bir inhibitöre güvenmek yerine farklı cepleri hedefleyen ilaçların kombinasyonunun—biri aktif bölgede, diğeri ise yalnızca belirli mutantlarda var olan bir veya daha fazla allosterik bölgede—daha etkili olabileceğini savunuyor. Bu tür kokteyller teorik olarak PI3Kα aktivitesini daha hassas şekilde azaltabilir, toksik yan etkileri düşürebilir ve tedaviyi bir hastanın tümöründe bulunan kesin mutasyon desenine daha iyi uyarlayabilir.
Atıf: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Anahtar kelimeler: PI3K alfa, onkogenik mutasyonlar, allosterik inhibitörler, moleküler dinamikler, sinyal iletimi