Clear Sky Science · tr
Dörtlü-konjüge edilmiş karbon dot nano modeli ile hedefe yönelik gliom tedavisinin geliştirilmesi
İnatçı beyin tümörleri için yeni umut
Glioblastom gibi yüksek dereceli beyin tümörleri, tedavisi en zor kanserler arasında yer alır. Vücudun diğer bölgelerinde işe yarayan birçok ilaç, beyni koruyan kan–beyin bariyerini geçememekle kalmaz, geçiş sırasında sağlıklı dokulara da zarar verebilir. Bu çalışma, beyin tümörlerine daha hassas şekilde sızmayı, güçlü bir ilaç karışımını taşımayı ve onu doğrudan tümör hücresi çekirdeğinin içinde serbest bırakmayı amaçlayan laboratuvarda geliştirilmiş “akıllı” bir nanoparçacığı tanımlıyor; böylece kanser hücrelerine maksimum zarar verilirken normal hücreler daha az etkilenir.
Karbonla inşa edilmiş küçük bir teslim kamyoneti
Yeni yaklaşımın merkezinde karbon dotlar—üretimi ucuz, suda iyi karışan ve belirli ışık türlerinde ışıldayan nanometre ölçeğinde parçacıklar—yer alır. Yüzeyleri çok sayıda kimyasal bağlama noktası içerdiğinden, aynı anda birden çok biyolojik bileşenle donatılabilirler. Bu çalışmada araştırmacılar “dörtlü-konjüge” bir nano model yarattı: her bir karbon dot, tek aşamalı bir reaksiyonda kimyasal olarak iki farklı hedefleme peptidi ve iki anticancer yük ile bağlandı. Bu modüler tasarım, her bir dottan tümör hücrelerini tanıyabilen, hücresel engelleri aşabilen ve ilaçları doğru hücre içi adrese taşıyabilen küçük bir teslim kamyoneti oluşturur.
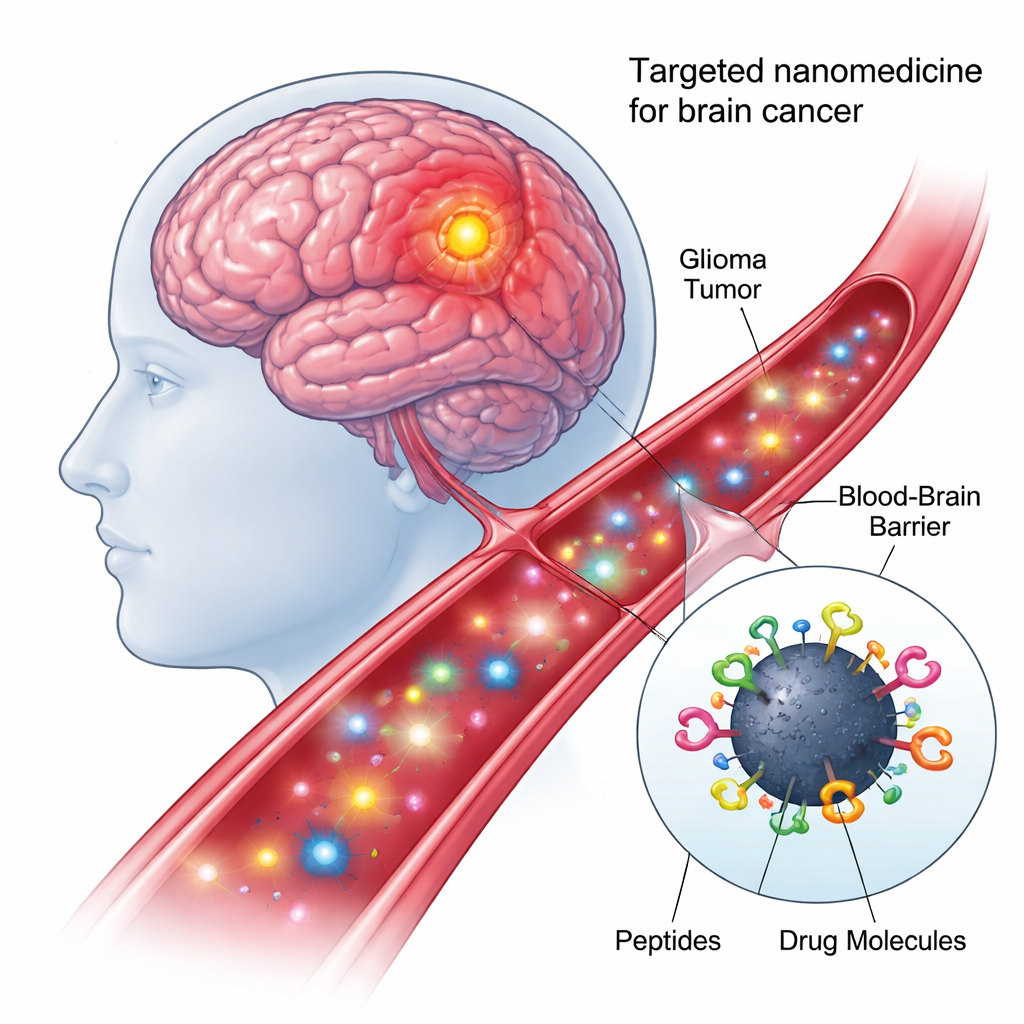
Doğru beyin hücrelerini bulma ve içeri girme
Nanoparçacığın üzerindeki ilk peptid olan shPep-1, IL13Rα2 adlı bir reseptörü tanımak üzere tasarlanmıştır. Bu reseptör, yetişkin ve pediatrik glioblastom ile diffuse intrinsic pontine glioma da dahil olmak üzere birçok agresif beyin tümöründe yüksek düzeyde bulunur, ancak normal beyin hücrelerinde zayıf olarak görülür. shPep-1, IL13Rα2’ye bağlanarak karbon dotların tümör hücrelerine yönelmesine ve reseptör aracılı alım yoluyla hücre içine girmesine yardımcı olur. İkinci, daha uzun peptid lnPep-1 ise nükleer lokalizasyon sinyali içerir: yükün nükleer zar üzerinden kayarak hücrenin DNA’sının saklandığı kontrol merkezine ulaşmasına yardımcı olan kısa bir dizi. Bu iki peptid birlikte nanoparçacığa hem tümöre yönelme özelliği hem de hücre içine girdikten sonra çekirdeğe ulaşma yeteneği sağlar.
Eşgüdümlü bir ilaç saldırısı teslimi
Terapötik yük iki küçük molekülden oluşur. İlki, DNA’ya girip çift sarmal kırıkların onarımında gerekli enzimleri bloke ederek kanser hücrelerini öldüren iyi bilinen kemoterapi ilacı epirubisinidir. İkincisi ise 5-aminoimidazol-4-karboksamid (AIC) adlı bir metabolittir; fizyolojik pH’da beyin tümörü ilacı temozolomidden üretilir. Önceki çalışmalarda aynı ekip, epirubisin ve AIC’nin bir karbon dot üzerinde birleşmesinin, tek başına herhangi bir ilaçtan daha fazla kanser hücresi öldürmeyi artırdığını göstermişti. Yeni tasarımda ikisi de çift peptidli nanoparçacıkta birlikte taşınarak tümör hücresi çekirdeğinde sinerjik bir etki hedefleniyor.
Tümör hücrelerinde güçlü, normal hücrelere karşı daha ılımlı
Nano modelin etkinliğini test etmek için ekip, birkaç yüksek dereceli glioma hücre hattını—yetişkin glioblastom, pediatrik glioblastom ve diffuse intrinsic pontine glioma modelini—dörtlü-konjüge karbon dotlara maruz bıraktı. Çok düşük konsantrasyonlarda bile (sadece 50 nanomolar kadar) tümör hücre canlılığı, tedavi edilmeyen kontrollere göre yaklaşık yarıya düştü ve daha yüksek dozlarda test edilen tüm konjügatlar çoğu tümör hücresini öldürdü. Önemli olarak, dörtlü nano model, taşınan toplam epirubisin daha az olmasına rağmen daha basit “tek peptidli” versiyonlardan daha iyi performans gösterdi. Kanser olmayan vasküler düz kas hücreleri üzerinde test edildiğinde ise çok daha az toksikti: benzer canlılık kaybını görmek için yaklaşık 25–40 kat daha fazla nanoparçacık gerekiyordu; bu da kaba kuvvetle doz arttırmak yerine tümör hedeflemesinden kaynaklanan faydalı bir güvenlik aralığı olduğunu düşündürüyor.
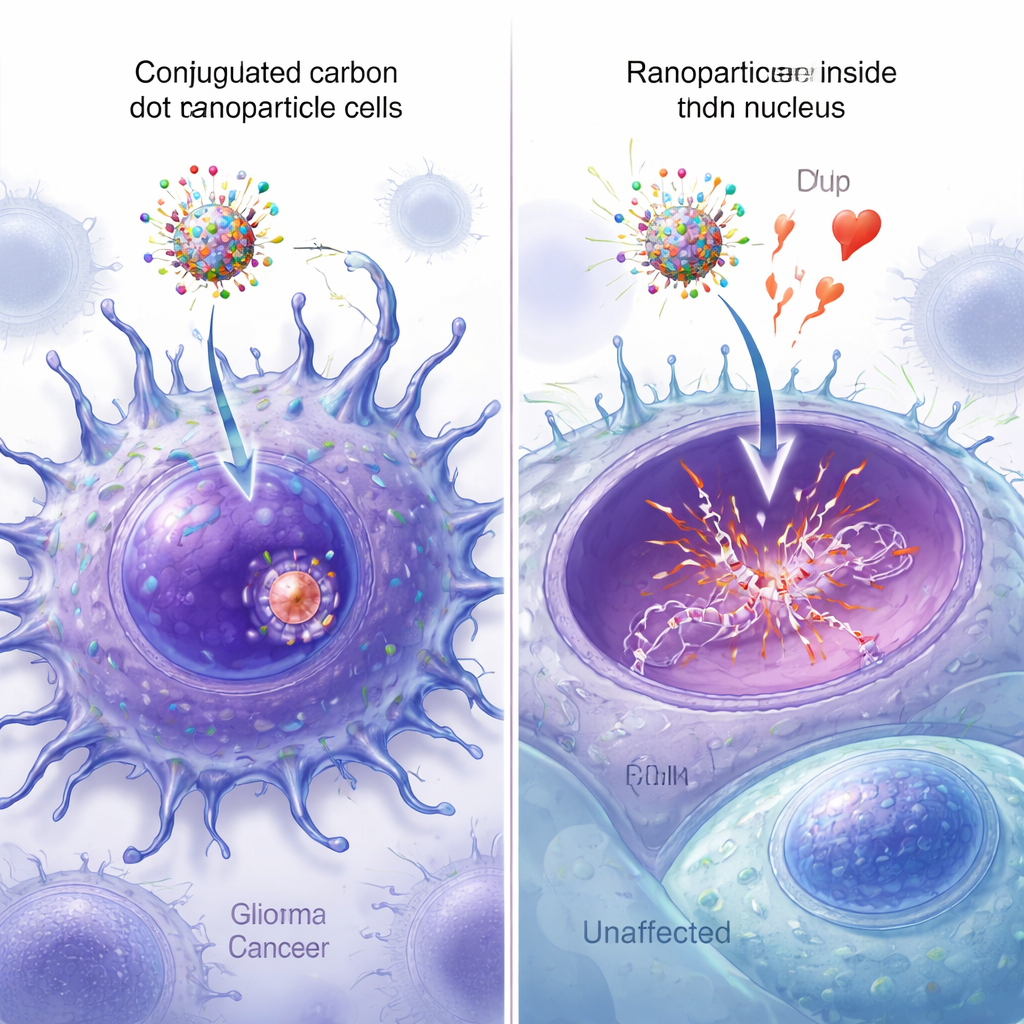
Nanoparçacıkların çekirdeğe ulaştığını görme
Nanoparçacıkların floresan versiyonları, araştırmacıların her bir tasarımın hücrelere ne kadar iyi girdiğini ve çekirdeğe ulaştığını izlemesini sağladı. Mikroskop altında her iki peptidi taşıyan karbon dotlar, kanser hücreleri boyunca yayılan en parlak sinyali gösterdi; yeşil nanoparçacık floresansı ile mavi nükleer boyamanın güçlü örtüşmesi gözlendi. Nicel görüntü analizi, çift peptidli parçacıkların en yüksek nükleer kolokalizasyona sahip olduğunu ve sadece bir peptid taşıyan veya hiç taşımayan parçacıklardan anlamlı derecede üstün olduğunu doğruladı. Ek spektroskopi, kütle spektrometrisi ve atomik kuvvet mikroskopisi ölçümleri, tüm dört bileşenin karbon dotlara başarılı bir şekilde bağlandığını ve boyutlarını ölçülebilir biçimde artırdığını, ancak epirubisinin ana DNA-bağlama işlevini bozmadığını doğruladı.
Gelecekteki beyin kanseri bakımına olası etkileri
Hastalar için bu bulgular hâlâ hazır bir tedaviden çok erken aşama, hücre-delik gösterimidir. Yine de umut verici bir fikri sergiliyorlar: küçük, stabil ve göreli olarak yapımı kolay karbon bazlı bir nanoparçacığın hedefleme peptidleri ve ilaç kombinasyonlarıyla hızla özelleştirilebilmesi. İlaçları IL13Rα2’yi aşırı üreten tümör hücrelerine özel olarak yönlendirip çekirdekte yoğunlaştırarak, bu tür nanoterapiler bir gün daha düşük dozlar, daha az yan etki ve glioblastom ile diffuse intrinsic pontine glioma gibi yüksek ölümcül beyin tümörleri için daha kişiselleştirilmiş tedavi stratejileri sağlayabilir.
Atıf: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Anahtar kelimeler: glioblastom, nanotıp, karbon dotlar, hedefe yönelik ilaç taşıma, beyin tümörleri