Clear Sky Science · tr
Kısıtlı cryo-EM gözlemleriyle AlphaFold’un ince ayarı
Protein biçimlerinin neden bu kadar zor görüldüğü
Proteinler, enerji üretiminden sinir sinyallerine kadar vücudumuzdaki neredeyse her süreci yöneten küçük moleküler makineler gibidir. Nasıl çalıştıklarını —ve ilaçların bunları nasıl kontrol edebileceğini— anlamak için, bilim insanlarının bunların kesin üç boyutlu biçimlerini bilmesi gerekir. Bu iş için ortaya çıkan iki güçlü araç vardır: donar haldeki proteinlerin birçok bulanık fotoğrafını çeken cryo–elektron mikroskobu (cryo‑EM) ve dizilerden protein yapısını tahmin eden yapay zeka sistemi AlphaFold. Ancak birçok gerçek deneyde cryo‑EM verileri eksik olabiliyor ve AlphaFold’un tahminleri her zaman gerçeğe uymuyor. Bu makale, AlphaFold’u zor cryo‑EM verilerini doğrudan dinlemeyi öğreten ve tahminlerini buna göre geliştiren CoCoFold adlı bir yöntemi tanıtıyor.
Kamera çok az gördüğünde
Cryo‑EM, proteinleri hızla dondurarak çok sayıda bireysel parçacığın birçok açıdan görüntülerini alır ve ardından bu görüntüleri bir 3B haritaya birleştirir. Ancak uygulamada araştırmacıların genellikle yeterince iyi görüntüsü olmayabiliyor. Bazen protein yalnızca kısa süreli yüksek enerjili bir durumda görünür, bu yüzden çok az parçacık yakalanır. Başka durumlarda proteinler buz yüzeyinde belirli yönleri tercih eder, dolayısıyla birçok görüntü açısı eksik kalır. Her iki sorun da bulanık, eksik haritalara yol açar ve bunları güvenilir atomik modellere çevirmek zorlaşır. Mevcut yazılımlar AlphaFold’un tahmin edilen yapılarını bu tür haritalara uydurabiliyor, fakat bunun başarısı başlangıçta keskin, yüksek çözünürlüklü verilere sahip olmaya çok bağlıdır.
AlphaFold’u ham görüntülerden öğrenmeye öğretmek
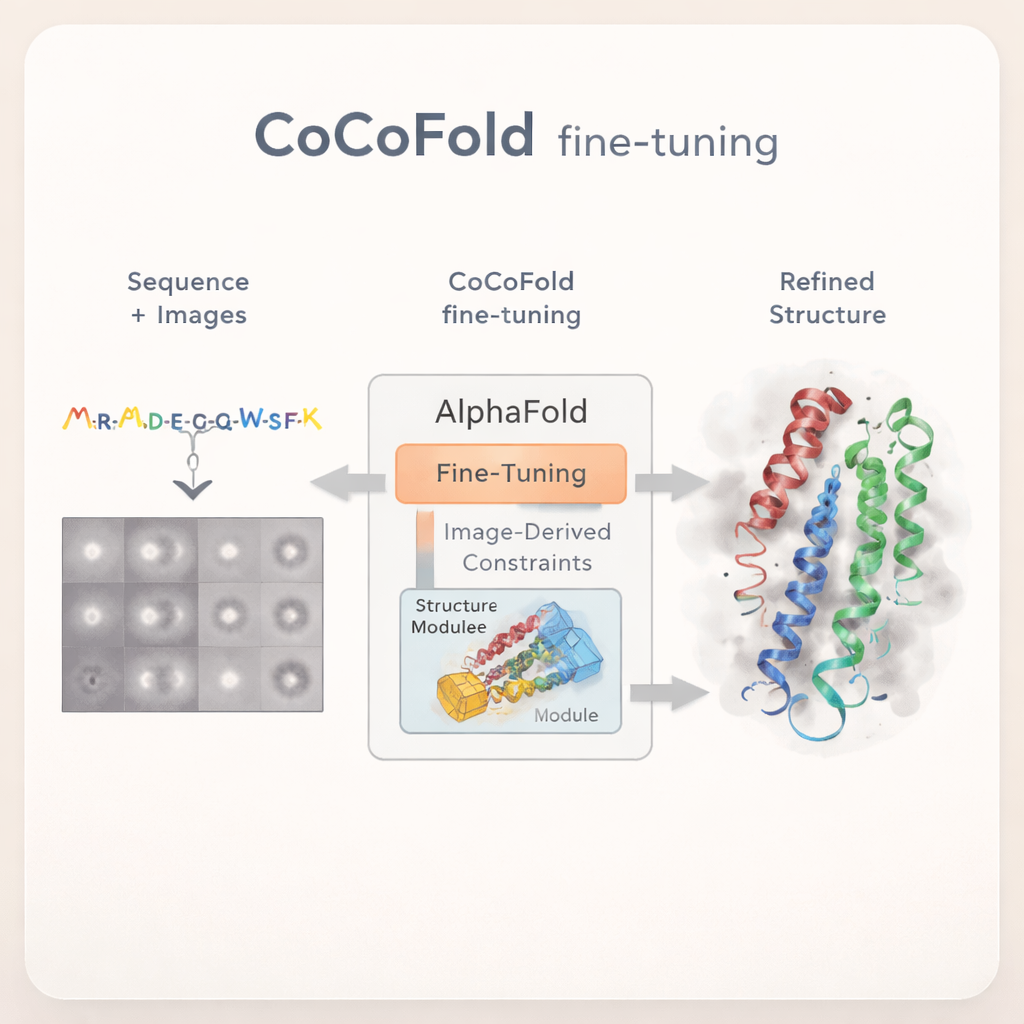
CoCoFold farklı bir yaklaşım benimser: tam yeniden yapılandırılmış bir 3B cryo‑EM haritasına güvenmek yerine doğrudan ham 2B parçacık görüntülerini kullanarak AlphaFold’u ince ayarlıyor. Yöntem, AlphaFold‑Multimer tahmininden başlar ve geniş protein katlanma bilgisini korumak için orijinal ağın çoğunu sabit tutar. Sadece son yapı‑oluşturan bölümün değişmesine izin verilir. Cryo‑EM görüntülerinden türetilen bilgileri bu yapı modülüne beslemek için hafif bir "adaptör" eklenir; bu, modelin deneysel verilerle uyumlu yapılara doğru nazikçe yönelmesini sağlar ve bilinen protein fiziğinden uç sapmaları önler.
Görüntüleri yapısal geri bildirime dönüştürmek
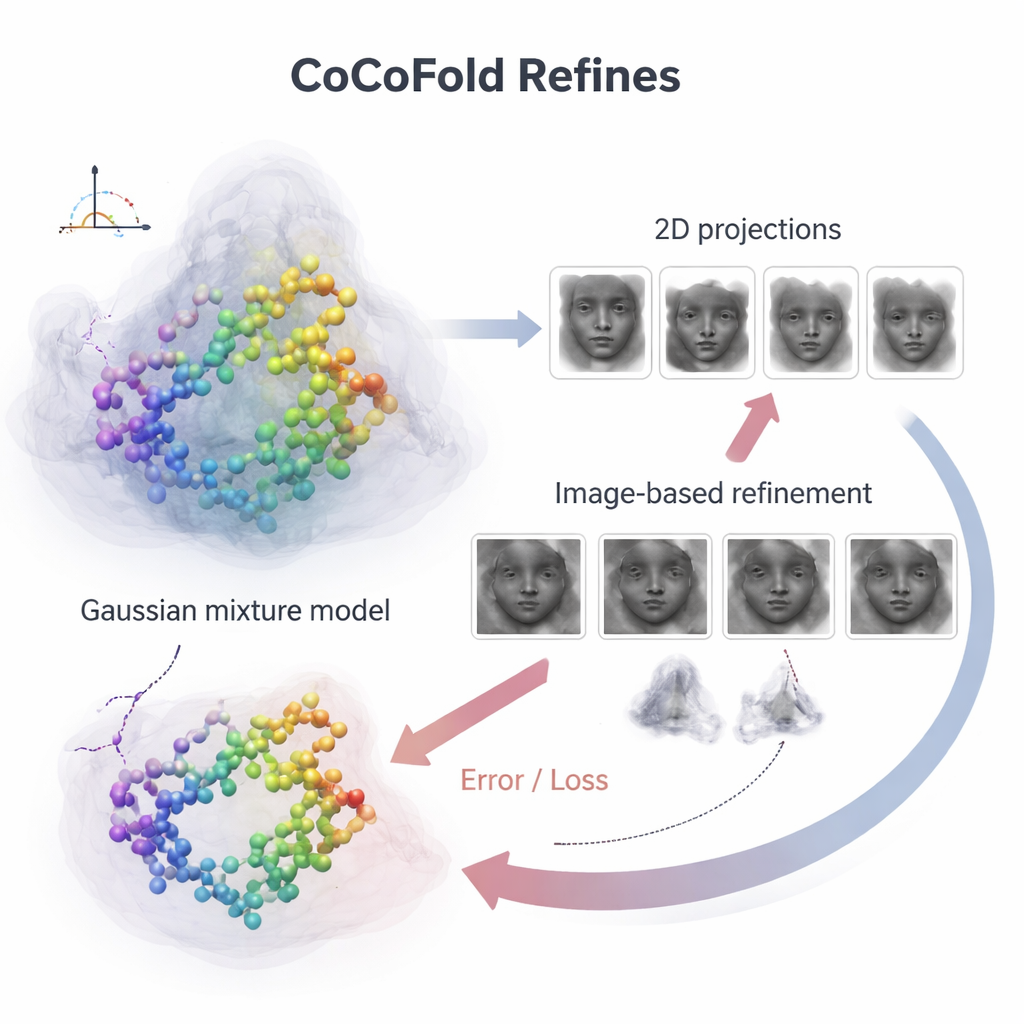
Bireysel protein atomlarını gürültülü mikroskop görüntülerine bağlamak için CoCoFold, örtüşen üç boyutlu lekelerden oluşan, Gauss karışımı olarak bilinen pürüzsüz ve esnek bir tahmin yapısı inşa eder. Bu temsilden, proteinin gerçek deneydeki aynı görüntü yönleri ve görüntüleme koşullarında mikroskopta nasıl görüneceğini simüle eder. Bu simüle edilmiş anlık görüntüler, gerçek cryo‑EM parçacıklarıyla frekans alanında halka halka karşılaştırılır ve ne kadar iyi eşleştikleri değerlendirilir. Herhangi bir uyumsuzluk, ağ üzerinden geri akan bir geri bildirim sinyaline dönüşür; bu sinyal hem protein modelini hem de yoğunluk temsilini hafifçe ayarlar. Eğitimin ardından atomik model, yerel geometrik çakışmaları gidermek için fizik tabanlı bir rafinman adımıyla daha da temizlenir.
Veriler kıt veya yanlıysa doğruluğu korumak
Yazarlar CoCoFold’u iki ana cryo‑EM sorununu taklit edecek şekilde tasarlanmış çeşitli deneysel ve simüle edilmiş veri setleri üzerinde test ettiler: çok az parçacık ve görüntü açılarında büyük boşluklar. Bu zorlu koşullar altında, yeniden yapılandırılmış haritalara dayanan diğer derin öğrenme yöntemleri dahil standart araçlar, proteinin bazı bölgelerini kaçırma, heliksleri yanlış yerleştirme veya haritalar bulanıklaştıkça ince ayrıntıları kaybetme eğilimindeydi. Buna karşılık CoCoFold tutarlı biçimde bilinen referans yapılarla daha yakın ve daha eksiksiz eşleşen modeller üretti. Hataları, parçacık sayısı büyük ölçüde azaldığında veya görüntü yönlerinin büyük konileri eksik olduğunda bile küçük kaldı; bu da ham görüntülerden doğrudan öğrenmenin harita‑tabanlı yaklaşımların yok saydığı hayati bilgileri koruduğunu gösteriyor.
Geleceğin yapısal biyolojisi için ne anlama geliyor
Uzman olmayanlar için ana mesaj şudur: CoCoFold, güçlü yapay zeka tahminleri ile kusurlu deneysel veriler arasında bir çevirmen gibi davranır. Yalnızca AlphaFold’a veya yalnızca cryo‑EM’e güvenmek yerine, özellikle deneylerin yalnızca kısmi bir görüş sağladığı zor rejimlerde, ikisinin birbirini bilgilendirmesine izin verir. Bol ve yüksek kaliteli verilerin olduğu basit durumlarda mevcut harita odaklı araçlar hala son derece iyi çalışır. Ancak parçacıkların nadir olduğu veya yönlerin eksik olduğu durumlarda —geçici veya hassas protein hallerinin peşinde koşarken sık karşılaşılan durumlar— CoCoFold, aksi takdirde boşa gidecek bilgiden güvenilir atomik modeller çıkarmanın bir yolunu sunar.
Atıf: Liao, J., Zheng, D., Zhang, H. et al. Fine-tuning AlphaFold with limited cryo-EM observations. Commun Chem 9, 95 (2026). https://doi.org/10.1038/s42004-026-01899-7
Anahtar kelimeler: cryo-EM, AlphaFold, protein yapısı, derin öğrenme, yapısal biyoloji