Clear Sky Science · tr
Memeli hücrelerinde sitozolik ilaç teslimini profillemek için genelleştirilebilir bir hücre içi birikim testi
İlaçları hücre içine sokmanın önemi
Günümüzün en umut verici ilaçlarının birçoğu — küçük moleküller, peptit adı verilen kısa protein parçaları ve tam boyutlu proteinler — hücrelerimizin içindeki hedeflere etki edecek şekilde tasarlanmıştır. Ancak hücre zarı sağlam bir güvenlik kapısıdır. Bir ilaç hücrenin dışına yapışabilir veya endozom adı verilen iç keseciklerde sıkışıp kalabilir ve yine de birçok hedefin bulunduğu sulu iç ortam olan sitozole ulaşamayabilir. Bu makale, araştırmacılara bir molekülün hücreye girip girmediğini değil, gerçekten görevini yapabileceği sitozole ulaşıp ulaşmadığını söyleyen yeni bir laboratuvar testi — CHAMP testi — tanımlıyor.
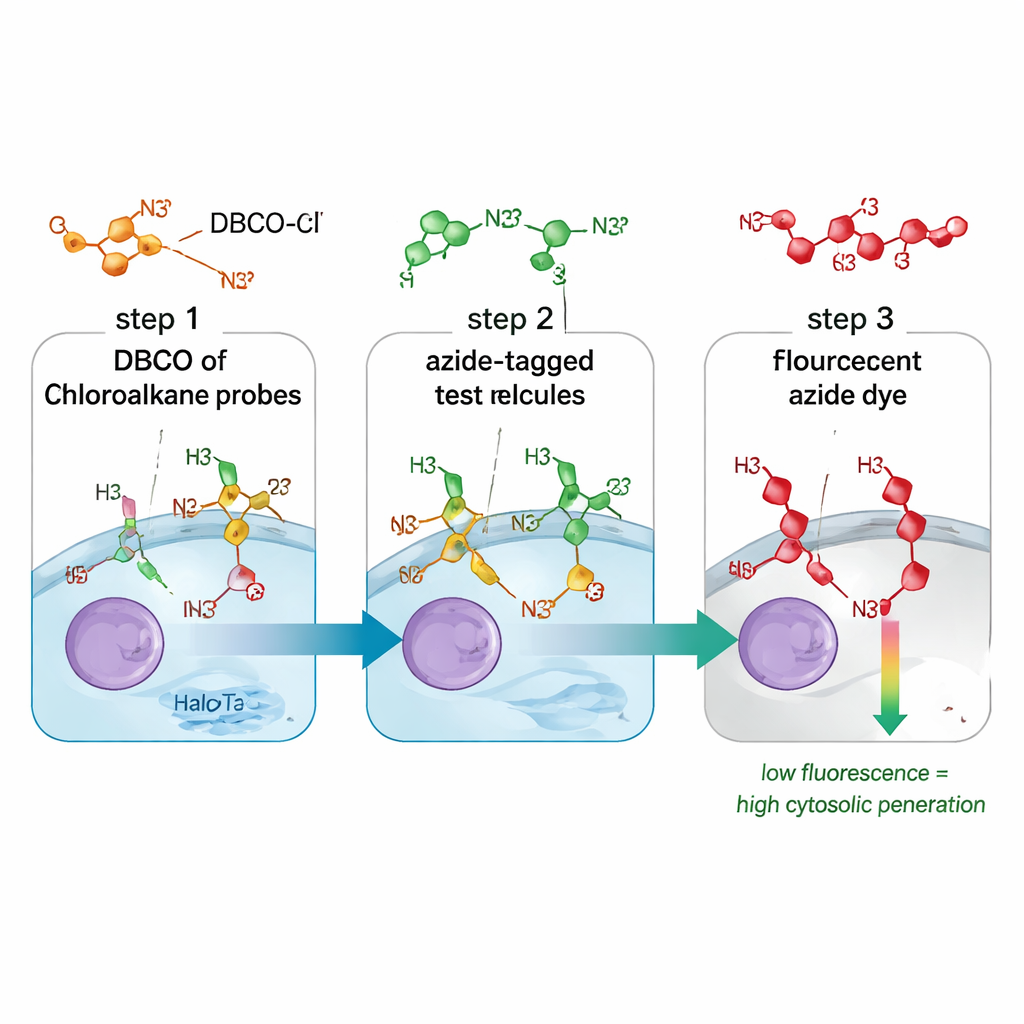
İlaç girişini izlemede yeni bir yöntem
Geleneksel ilaç alım ölçümleri genellikle hücre yüzeyine temas eden, endozomlarda oturan veya gerçekten sitozole ulaşan molekülleri ayırmakta başarısız olur. Ayrıca bir molekülün davranışını değiştiren hantal floresan etiketlere dayanabilirler. CHAMP testi, azid adı verilen küçük bir kimyasal “tutamak” ile hücre kültürlerinde sitozolde serbestçe yüzecek şekilde tasarlanmış HaloTag adlı bir protein işaretleyicisini birleştirerek her iki sorunu da çözer. Önce hücreler, HaloTag’e DBCO — gerilmiş bir alkin formu — takan bir bağlayıcı molekül ile muamele edilir. Sonra bilim insanları, küçük azid etiketini taşıyan test bileşiğini ekler. Bu bileşik ancak hücre zarını geçip sitozole girdiyse azid ile DBCO birbirine yüksek selektiviteyle bağlanabilir. Son olarak kullanılan floresan azid boya, kaç DBCO bölgesinin kaldığını ortaya koyar: sönük hücreler test bileşiğinin girip çoğu siteyi işgal ettiğini; parlak hücreler ise sitozolik erişimin zayıf olduğunu gösterir.
Kavramdan çalışan bir teste
Yazarlar önce HaloTag’in standart bir kloroalkil boyası ve görüntüleme kullanarak HeLa insan hücrelerinin sitozolünde doğru şekilde üretildiğini ve lokalize olduğunu doğruladılar. Ardından CHAMP’ın her adımını optimize ettiler: ne kadar DBCO bağlayıcı eklenecek, ne kadar süre inkübe edilecek ve hangi floresan azid boyasının hücrelere zarar vermeden güçlü, özgül bir sinyal verdiği belirlendi. Akış sitometrisi — binlerce bireysel hücredeki floresansı ölçen bir cihaz — testin hızlı, sağlam ve ayarlanabilir olduğunu gösterdi. Kritik olarak ekip, floresansın hücre bileşenlerine yapışan boyalardan ziyade gerçekten HaloTag bölgelerindeki özgül reaksiyonlardan kaynaklandığını ve küçük azid etiketinin moleküllerin hücrelere girişini gözle görülür şekilde bozmadığını gösterdi.
Küçük ilaçlar ve peptitler hakkında testin ortaya koydukları
CHAMP ile araştırmacılar yüzlerce azid ile etiketlenmiş küçük molekülü test edip yük, boyut ve esneklik gibi özellikleri sistematik olarak değiştirdiler. Örneğin negatif yüklü bir karboksilik asidi nötr bir amide dönüştürmenin sitozolik birikimi artırdığını ve nitrojen metilasyonunun derecesi ve konumunun bileşiklerin hücre içine girişini etkilediğini gözlemlediler. Serbest boncuklar üzerindeki reaksiyonları canlı hücrelerle karşılaştırarak, kimyasal reaktivitenin kendi içsel etkisini membranın dayattığı bariyerden ayırabildiler. Ekip ayrıca CHAMP’ı yaygın antibiyotiklerden oluşan bir panoya uygulayarak bazılarının sitozole diğerlerinden çok daha iyi ulaştığını gösterdi — bu, konak hücrelerin içinde saklanan bakterileri tedavi ederken önemli bilgiler sağlar.
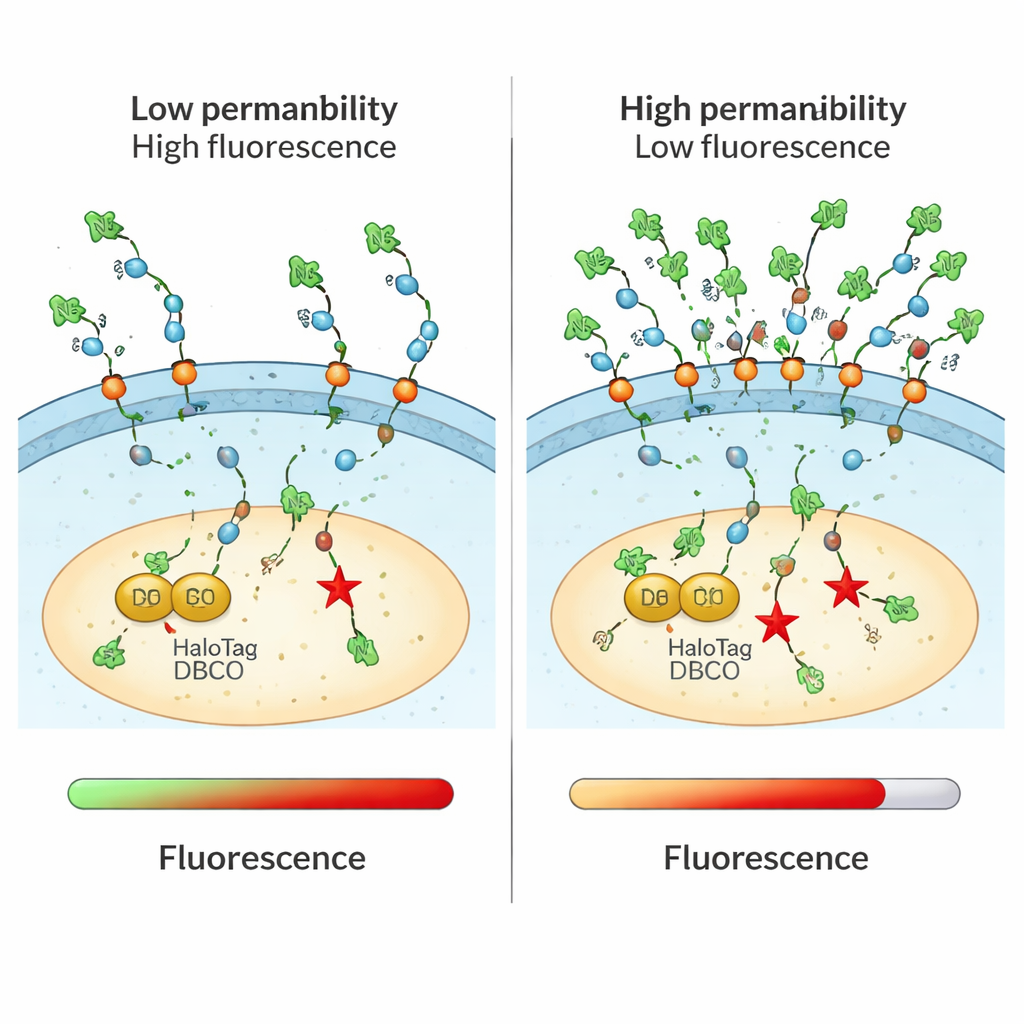
Engeli aşan süper yüklü peptitler ve proteinler
Test özellikle başka yollarla izlenmesi zor olan daha büyük, yüksek yüklü molekülleri çalışmada güçlüydü. Yazarlar çok sayıda arginin kalıntısından oluşan hücre geçirgen peptitleri incelediler ve açık bir eğilim doğruladılar: daha uzun, daha pozitif yüklü zincirler belirli bir noktaya kadar daha fazla materyali sitozole taşıdı. Bazı amino asitlerin sağ/sol el (stereokimya) yapısını tersine çevirmenin giriş üzerinde nasıl etkili olduğunu araştırdılar ve ayna görüntü versiyonların bazen daha iyi birikim gösterdiğini, membranla ince kiral etkileşimlere işaret eden bulgular elde ettiler. CHAMP ayrıca birçok pozitif yük taşıyacak şekilde tasarlanmış “süper yüklü” proteinlerin normal karşıtlarından daha etkili şekilde sitozole ulaşabildiğini göstererek, bunların büyük terapötik yükleri taşıyıcı olarak kullanma potansiyelini destekledi.
Gelecekteki hücre içi ilaçlar için tasarım kuralları
Küçük moleküller, peptitler, makrosiklik peptitler ve modifiye omurgalar sistematik olarak test edilerek çalışma genelinde tasarım ilkeleri ortaya çıkarıldı. Omurgaları halka şeklinde kapatılmış makrosiklik peptitler, esnek lineer versiyonlara göre genellikle sitozole daha kolay ulaşıyordu. Peptit omurgalarına dikkatle yerleştirilmiş N-metil grupları girişi mütevazı şekilde artırdı, fakat çok fazla olması ters etki yaratabiliyordu. Tek bir standartlaştırılmış testle ortaya konan bu yapı–geçirgenlik ilişkileri, hedeflerine bağlanmakla kalmayıp gerçekten hücre içinde onlara ulaşabilen moleküller tasarlamak isteyen kimyagerler için pratik rehberlik sunuyor.
İlaç geliştirmeye katkısı
Basitçe söylemek gerekirse, CHAMP testi hücrenin ön kapısı ve iç koridorundaki hassas ayarlı bir trafik sayacıdır. Deneysel hangi ilaçların gerçekten zarı geçip sitozole ulaştığını, yüzeyde veya iç kompartmanlarda sıkışmış moleküller tarafından yanıltılmadan bildirir. Geniş bir moleküler şekil ve boyut yelpazesiyle çalışması ve yalnızca küçük bir azid etiketi kullanması sayesinde CHAMP, yüksek verimli keşif hatlarına entegre edilebilir. Zamanla bu, en önemli hedeflerin hücrelerimizin içinde kilitli olduğu hastalıklar için daha etkili tedavilerin tasarımını hızlandırmalıdır.
Atıf: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
Anahtar kelimeler: hücre içi ilaç teslimi, hücre zarı geçirgenliği, sitozolik birikim, hücre geçirgen peptitler, biyooksidatif tıklama kimyası