Clear Sky Science · tr
Vanadyum bileşiğinin insan serum transferrini ile reaksiyonunda oluşan bir adüktün ilk kristal yapısı
Kan proteini ve metal ilacın neden önemi var
Birçok deneysel ilaç, diyabetten kansere kadar çeşitli hastalıkların tedavisine yardımcı olabilen metal atomları içerir. Ancak bu metal bazlı ilaçlar kana girdikten sonra vücudun doğal taşıyıcı proteinlerine tutunmak zorundadır. Bu çalışma, ana demir taşıyıcımız olan insan serum transferrini ve umut vaat eden bir vanadyum bileşiğinin nasıl etkileştiğini inceliyor; böylece metal ilaçların vücutta nasıl taşındığı ve daha güvenli, daha etkili tedaviler için nasıl ayarlanabileceği konusunda fikir veriyor.
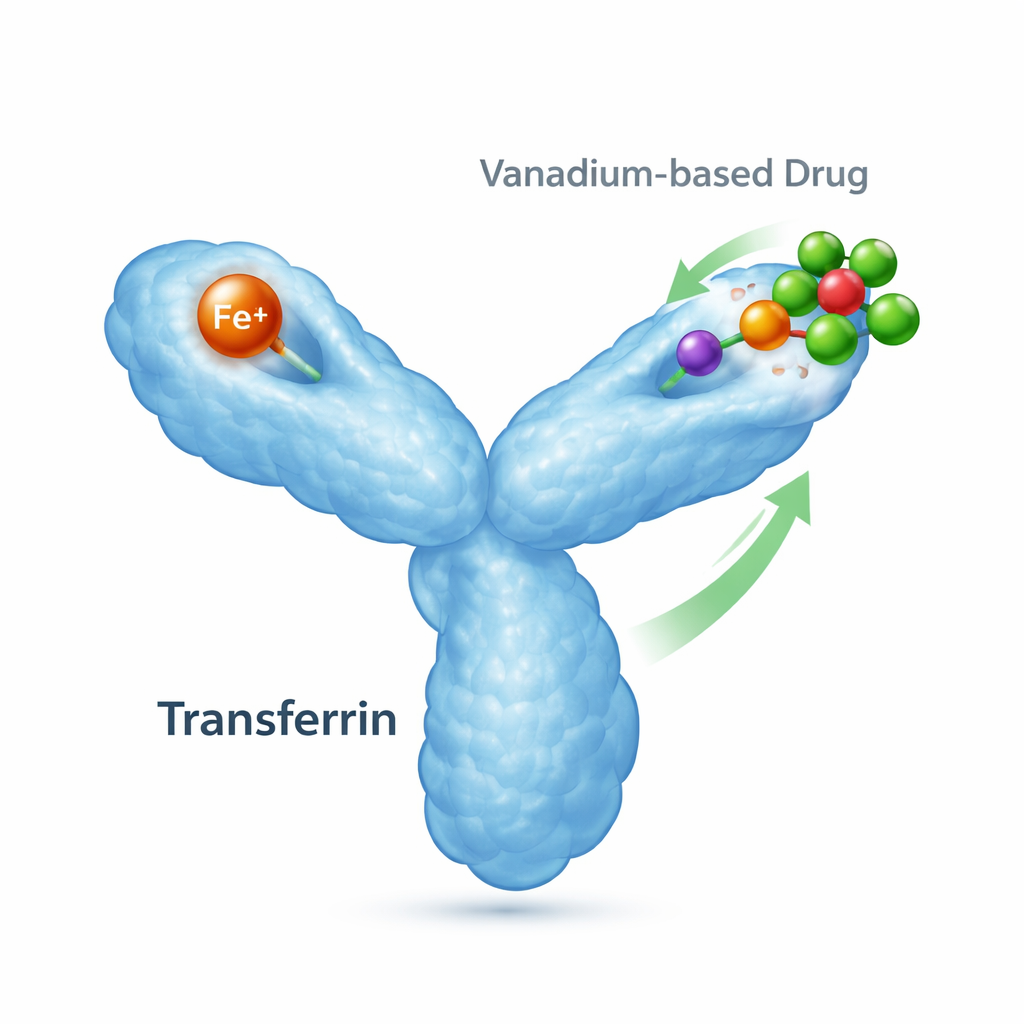
Vücudun demir kuryesi ve yan görevleri
Transferrin, görevi demiri yakalayıp ihtiyaç duyan hücrelere ulaştırmak olan yaklaşık 80 kilodaltonluk bir proteindir. Her biri bir demir iyonu bağlayabilen iki “lob”a sahiptir ve demirin varlığına göre şekil değiştirir. Demir bağlandığında bir lob kapanır; demirsizken açık kalır. Hücre yüzeyindeki özel reseptörler, demirle yüklü bu formları tanır ve içeri alır; bu nedenle transferrin demir dengesi ve hücre sağlığı için merkezi bir rol oynar. Bununla birlikte transferrin, tıbbi tedavilerden gelen metaller de dahil olmak üzere diğer metalleri bağlayabilir; bu da metal bazlı ilaçların nerelere gidebileceğini ve nasıl etki gösterebileceğini etkileyebileceği anlamına gelir.
Transferrinde vanadyumun bir şekil anlık görüntüsü
Araştırmacılar, bis(asetilacetonato)oksovanadyum(IV) olarak sıkça yazılan ve iyi çalışılmış bir vanadyum ilaç adayı olan [VIVO(acac)₂] üzerine odaklandılar. Önceki çalışmalar bu bileşiğin veya sudaki türevlerinin transferrine bağlanabileceğini göstermişti, ancak tam olarak nasıl bağlandığı görülmemişti. X-ışını kristalografisi kullanarak ekip, yalnızca C-terminal lobunda demir taşıyan ("FeC" formu) transferrinin yüksek çözünürlüklü yapılarını, vanadyum ilacına maruz bırakılmadan önce ve sonra elde etti. Vanadyumla işlenen kristallerde orijinal ilaç değil, demirsiz N-terminal lobunda bağlanmış, dönüştürülmüş bir vanadyum-oksijen kümesi gözlendi. Bu, insan transferrinine bağlı bir vanadyum fragmanının ilk doğrudan yapısal görüntüsünü sağladı.
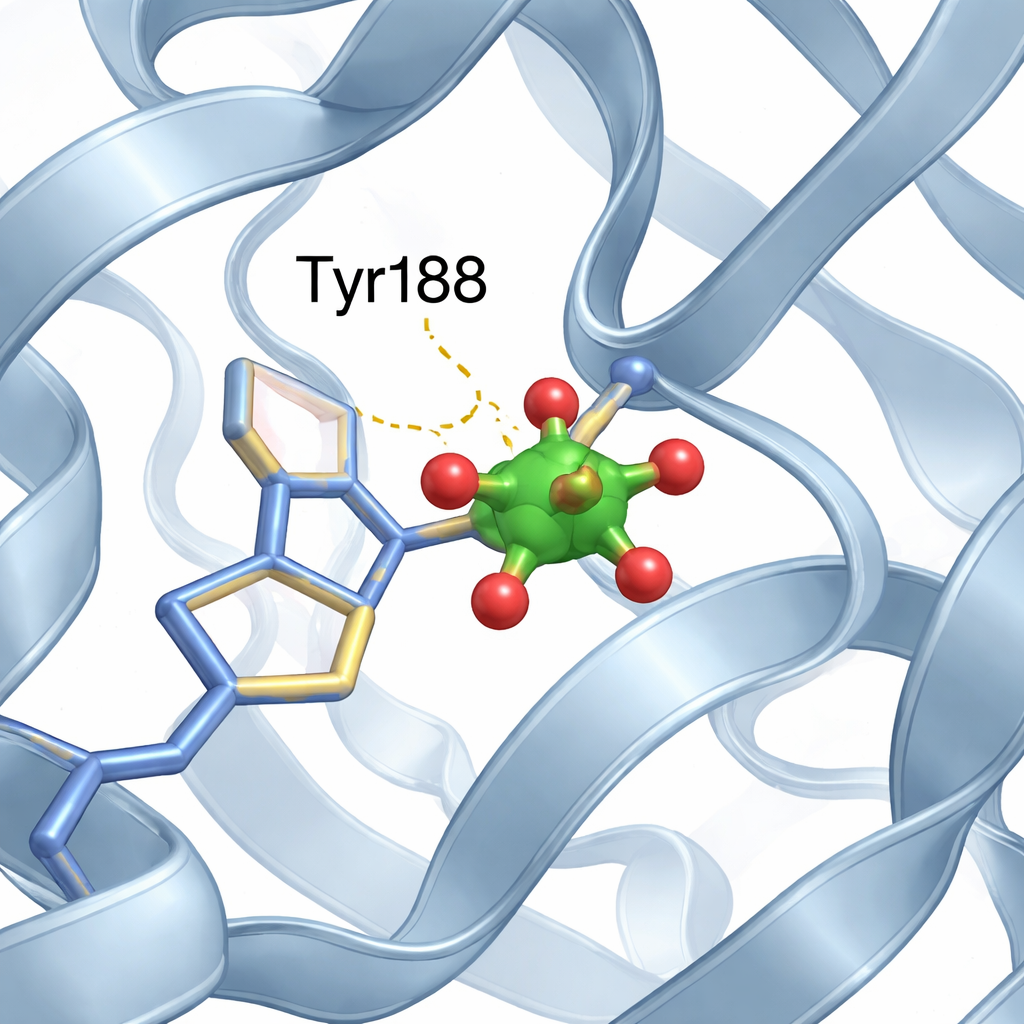
Küçük bir vanadyum kümesi uygun bir yuva buluyor
N-lobun demir bölgesinin içinde ekip, iki vanadyum atomu ve oksijen atomlarından oluşan küçük bir küme tanımladı; en iyi tanımıyla modifiye olmuş bir “divanadat” birimi. Kümenin oksijen pozisyonlarından biri, tirozin 188 (Tyr188) adlı belirli bir aminoasidin oksijeni tarafından üstlenilmiş ve böylece protein ile metal küme arasında doğrudan bir bağ oluşmuş. Yakın protein bölgelerinden gelen hidrojen bağları gibi ek nazik etkileşimler kümenin yerinde daha da stabilize olmasını sağlıyor. Önemli olarak, bu yeni metal misafir bir demir bağlama cebini işgal etmesine rağmen, proteinin genel olarak N-lobunun açık ve C-lobunun kapalı olduğu düzeni neredeyse vanadyumsuz yapı ile özdeş kalıyor.
Transferrin vanadyumun kimyasını nasıl yeniden şekillendiriyor
Kristalleştirme için kullanılan pH ve konsantrasyondaki çözelti ortamında, kristalde görülen iki vanadyumlu tür genellikle sadece küçük bir bileşendir; daha büyük vanadyum-oksijen kümeleri baskın olma eğilimindedir. Spektroskopik ölçümler ve teorik türleşme hesaplamaları, orijinal vanadyum ilacının suda yavaşça okside olup parçalandığını, bunun basit vanadat iyonları ürettiğini ve ardından çeşitli kümeler oluşturmak üzere bir araya geldiklerini gösteriyor. Kristal yapı, transferrinin bu küçük divanadat-benzeri fragmanı daha büyük kümelere göre seçici olarak stabilize ettiğini; Tyr188'de sıkı bir bağlanma bölgesi ve destekleyici bir hidrojen bağ ağı sağlayarak kalabalık bir çözelti karışımından tek bir kimyasal formu “seçtiğini” gösteriyor.
Hücre reseptörüyle el sıkışmasını sürdürmek
Transferrinin demiri teslim etmek için hücre yüzeyindeki bir reseptöre bağlanması gerektiğinden, araştırmacılar bu vanadyum kümesinin bu hayati el sıkışmayı bozup bozmayacağını sordular. Denatüre etmeyen jel elektroforezi ve biyokatman girişimciliği (biolayer interferometry) olarak bilinen hassas bir teknik kullanarak, vanadyumla muamele edilmiş transferrinin transferrin reseptörüne bağlanmasının, işlenmemiş yalnızca demirli forma kıyasla nasıl olduğunu ölçtular. Her iki form da neredeyse özdeş şekilde davranarak düşük nanomolar aralıkta çok güçlü bağlanma gösterdi. Bu, N-lobuna yerleşmiş olan vanadyum kümesinin, reseptörün etkileştiği yerde transferrin’in şeklini anlamlı şekilde değiştirmediğini ve dolayısıyla proteinin hücreler tarafından tanınmasını engellememesi gerektiğini doğruluyor.
Metal bazlı ilaçlar için bunun anlamı
Uzman olmayanlar için çıkarım, bu çalışmanın bir vanadyum ilaç türevinin vücudun ana demir kuryesine nasıl moleküler düzeyde bağlandığını ve normal işlevini bozmadan nasıl taşınabildiğini gösteren bir anlık görüntü sağlamasıdır. Transferrin, bir demir bölgesinde belirli küçük bir vanadyum-oksijen kümesini yakalayabilir; buna karşın proteinin genel şekli ve reseptöre bağlanma yeteneği esasen değişmeden kalır. Bu bulgu, vanadyum ilaçlarının transferrine bağlı olarak dolaşabileceğini açıklamaya yardımcı olur ve farklı proteinlerin farklı vanadyum küme boyutlarını tercih edebileceğini vurgular. Bu tür bilgiler, kan dolaşımındaki davranışları—hangi formları aldıkları, nereye gittikleri ve ne kadar süre kaldıkları—öngörülebilir ve kontrol edilebilir metal bazlı daha akıllı terapiler tasarlamak için anahtardır.
Atıf: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Anahtar kelimeler: vanadyum ilaçları, insan serum transferrini, metal bazlı terapötikler, protein–metal bağlanması, yapısal biyoloji