Clear Sky Science · tr
Microglia insan beyin organoidlerinde HIV kaynaklı transkripsiyonel ve metabolik değişikliklere yol açıyor
Neden HIV’e bağlı beyin değişiklikleri hâlâ önemli
Güncel HIV ilaçları birçok kişinin uzun ve sağlıklı yaşamasına olanak sağlasa da, yarıya kadar birey hâlâ hafıza, dikkat veya ruh halinde ince sorunlar yaşar. Bu çalışma acil bir soruyu gündeme getiriyor: virüs kontrol altında olsa bile, zaman içinde sinir hücrelerine gizlice zarar verebilecek beyin içindeki süreçlerde neler oluyor? İnsan beyin dokusunu taklit eden laboratuvarda yetiştirilen küçük “mini-beyin”ler kullanarak araştırmacılar, HIV ile beynin bağışıklık hücreleri arasındaki etkileşimin inflamasyon ve hücresel enerji kullanımını nasıl bozduğunu ve bu durumun kalıcı sorunların altında yatan mekanizmalar olabileceğini inceliyor. 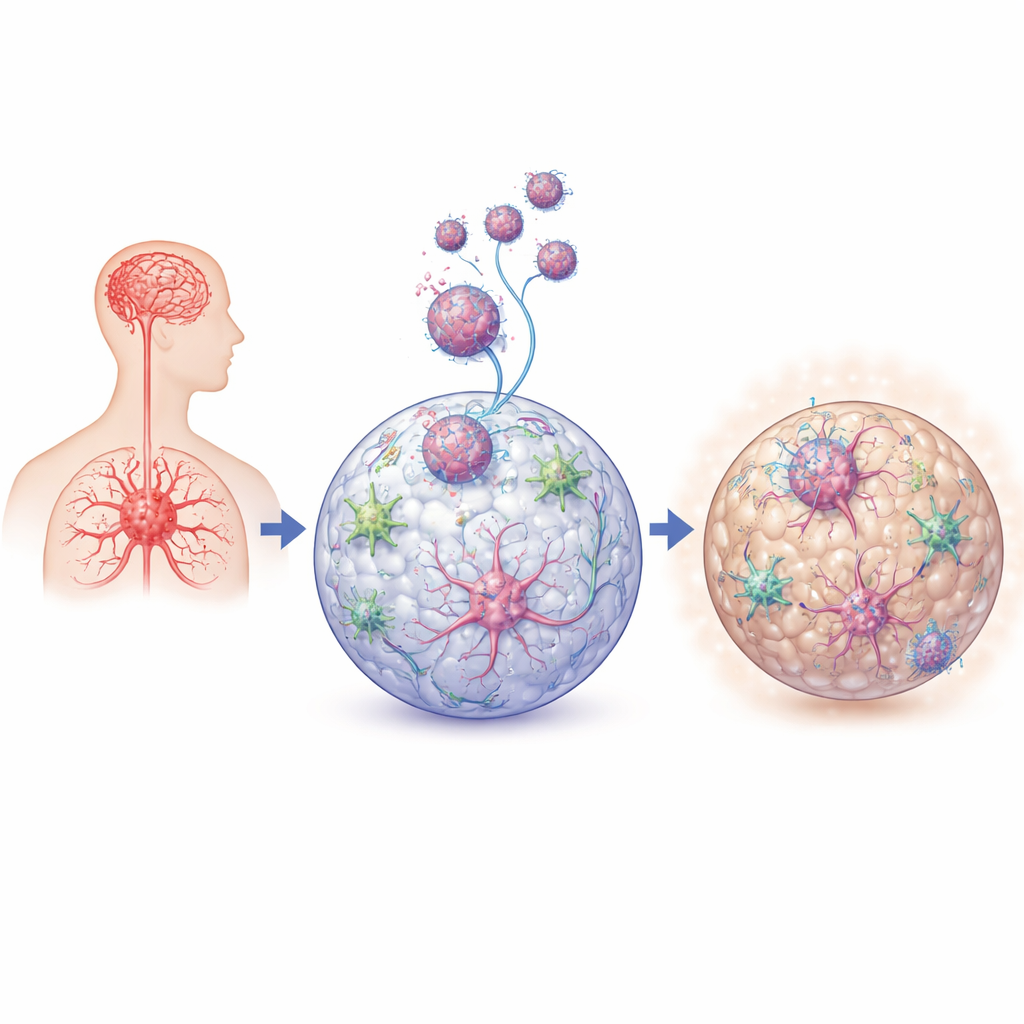
Mini-beyinler ve beynin nöbetçi bekçileri
Canlı insanlarda tam bir beyni incelemek nadiren mümkün olduğundan, ekip üç boyutlu nöral organoidleri kullandı: kök hücrelerden yetiştirilen bezelye büyüklüğünde insan sinir dokusu topları. Bu organoidlere, tehditleri denetleyen ve nöronlar arasındaki sağlıklı bağlantıların korunmasına yardımcı olan beynin yerleşik bağışıklık hücreleri mikrogliyaları eklediler. Daha sonra mikrogliyalara beyin hücrelerini hedefleyen bilinen bir HIV suşunu enfekte edip bu enfekte mikrogliyaların organoidlerin içine yerleşmesine izin verdiler. Bu düzenek, beynin ortamına erken HIV invazyonunu insan temelli, kontrol edilebilir bir modelde yeniden yaratarak bilim insanlarının mikrogliya bulunan ve bulunmayan, aktif veya inaktif virüs içeren organoidleri karşılaştırmasına olanak verdi.
Virüs nerede saklanıyor ve kimleri etkiliyor
Mikroskop görüntüleme ve viral ölçümler, virüsün mikrogliyalarda güçlü şekilde çoğaldığını ve viral proteinlerin komşu hücrelere yayıldığını gösterdi. Geç dönem viral proteinler yalnızca mikrogliyalar içinde değil, aynı zamanda astroglia adı verilen yıldız biçimli destek hücrelerinde de bulundu; öte yandan nöronlar kendilerinde doğrudan enfeksiyona ait belirgin işaretler göstermedi. Buna karşın viral düzenleyici proteinler nöronlara yakın görünüyordu; bu da HIV’in davranışlarını dolaylı olarak etkileyebileceğini düşündürüyor. Mikrogliya içeren organoidlerde viral genetik materyal düzeyleri mikrogliya içermeyenlere göre çok daha yüksekti; bu da mikrogliyanın beyinde uzun ömürlü bir rezervuar ve HIV’i güçlendiren bir rol üstlendiğini vurguluyor.
Bağışıklık alarmı ve HIV için yeni bir kapı
Araştırmacılar hangi genlerin açılıp kapandığını incelediklerinde, mikrogliya varlığında HIV’in çok daha yaygın değişiklikler tetiklediğini buldular. İnflamasyon ve antiviral savunmayla bağlantılı yüzlerce genin etkinliği arttı; bu genler arasında sinyal moleküllerini ve interferon yanıtını kontrol eden yolaklar vardı. Dikkate değer bir bulgu, hem HIV için ikincil bir giriş noktası olabilen hem de bağışıklık hücresi hareketini şekillendiren CCR6 adlı reseptörün güçlü şekilde artmasıydı. Beyin inflamasyonunda sık görülen astroglia aktivasyon belirteçleri de yükseldi ve çevre sıvıda CCL13 gibi bazı kemokinler arttı. Bu değişiklikler bir araya geldiğinde, HIV ile enfekte mikrogliyaların sahnede olduğu yerde beyin dokusunun çok reaktif ve inflamatuvar bir ortam haline geldiği bir tablo ortaya koyuyor.
Stres altındaki beyin hücrelerinde yakıt karışımında kayma
Gen etkinliğinin ötesinde ekip, HIV’in hücresel metabolizmanın—hücrelerin yakıt ve yapı taşlarını nasıl işlediğinin—kimyasını nasıl değiştirdiğini inceledi. Gen verilerinden oluşturulan bilgisayar modelleri kullanarak enfekte organoidlerde hangi metabolik reaksiyonların hızlandığını veya yavaşladığını haritaladılar. Arjinin, prolin, triptofan ve enerjiyle ilişkili alfa-ketoglutarat gibi moleküller başta olmak üzere amino asit kullanımında ve taşınmasında belirgin bir “yeniden kablolama” keşfettiler. Bu maddeleri hücresel bölümler arasında taşıyan transport proteinleri enfekte ve mikrogliya içeren organoidlerde daha aktiftir. Modeller, hücrelerin bazı amino asitleri dışarı verdiğini, diğerlerini alternatif enerji yollarına yönlendirdiğini ve daha fazla ara ürünü mitokondriye ittiğini gösteriyordu; sanki doku metabolik stres altındaymış ve yüksek enerji taleplerini karşılamak için çabalıyormuş gibiydi. Bu tür değişiklikler glutamat düzeylerini yükseltebilir ve triptofandan yıkımı bozabilir—bunların her ikisi de oksidatif stres, nöronlar arası iletişimin bozulması ile ruh hali ve bilişsel sorunlarla bağlantılıdır. 
HIV ile yaşayan insanlar için bunun anlamı
Genel olarak çalışma, HIV ile enfekte mikrogliyaların nöronların doğrudan enfekte edilmemiş olması halinde bile yakınındaki beyin hücrelerinde hem bağışıklık sinyallemesini hem de enerji yönetimini yeniden şekillendirebileceğini gösteriyor. Mikrogliya kaynaklı bu “immünometabolik” dengesizlik, nöronların dayandığı destek sistemini zayıflatarak kronik inflamasyon ve ince ama ilerleyici beyin işlev bozukluğunu teşvik ediyor olabilir. CCR6 yükselmesi ve belirli amino asit kaymaları gibi erken moleküler ve metabolik değişiklikleri belirleyerek, bu organoid modelleri gelecekte HIV’e bağlı bilişsel sorunlar açısından daha yüksek riske sahip kişileri işaretleyecek biyobelirteçlerin tespit edilmesine yardımcı olabilir ve yalnızca viral çoğalmayı değil, aynı zamanda beynin sessiz metabolik yükünü koruyacak terapilerin geliştirilmesine yol gösterebilir.
Atıf: Capendale, P.E., Helgers, L.C., Ambikan, A.T. et al. Microglia cause HIV-induced transcriptional and metabolic changes in human neural organoids. Commun Biol 9, 436 (2026). https://doi.org/10.1038/s42003-026-09864-9
Anahtar kelimeler: HIV ve beyin, nörokognitif bozukluklar, mikrogliya, beyin organoidleri, beyin metabolizması