Clear Sky Science · tr
Acinetobacter türünün tip VI salgılama sistemi: mekanizmalar, biyoloji ve terapötik potansiyel
Hastane mikroplarının gizli silahları
Birçok kişi bazı hastane mikroplarının antibiyotiklere karşı koyabildiğini bilir; daha az kişi ise bu mikropların aralarında şiddetli mücadeleler de verdiğini fark eder. Bu derleme, Acinetobacter içinde bulunan mikroskobik “yaylı mızrak”a — kötü şöhretli hastane patojeni Acinetobacter baumannii'yi de içeren bakteri grubunun bir parçası — odaklanıyor. Bu yerleşik silahın nasıl çalıştığını, ne zaman devreye girdiğini ve enfeksiyonların yerleşmesine nasıl yardımcı olduğunu anlamak, yaşamı tehdit eden ve ilaca dirençli enfeksiyonları teşhis edip etkisiz hale getirmek için yeni yollar açabilir.
Yalnızca zehirli ok değil, bir hayatta kalma makinesi
Acinetobacter türleri toprakta, suda ve cildimizde yaşar, ancak bazıları hastane patojeni olarak son derece başarılı hale gelmiştir. Silah depolarındaki önemli araçlardan biri Tip VI salgılama sistemi (T6SS) — hücre zarfına sabitlenmiş küçük bir kasılıp uzayan makinedir. Tetiklendiğinde, komşu hücrelere toksik proteinlerle yüklü iğne benzeri bir sivri uç fırlatır ve çoğunlukla temasta rakip bakterileri öldürür. Bazı diğer mikropların bu sistemin birkaç varyantını taşımasının aksine, patojenik Acinetobacter genellikle yalnızca bir T6SS'e sahiptir; yine de bu tek platformu rakipleri uzaklaştırmaktan enfeksiyonları şekillendirmeye kadar birçok amaç için yeniden tasarlamıştır.
Yeniden inşa edilmiş donanım: alışılmadık bir fırlatma platformu
Çoğu bakteri T6SS'ini standart parça seti etrafında kurar, ancak Acinetobacter birkaç önemli parçayı yeniden şekillendirmiştir. Yaygın bir dış zar ankrajı olan TssJ'den yoksundur ve bunun yerine üç özel yardımcıya güvenir: TsmK iç zarda bir temel oluşturur, TslA hücre duvarını geçen uzun bir “tünel” proteini (TssM) için stabilite sağlar ve TagX silahın yolu için duvarı yerel olarak keser. Bunun üzerine, VgrG1 adlı belirli bir sivri uç proteininin sistemin ateşlenebilmesi için neredeyse kusursuz biçimde şekillenmesi gerekir—tek bir amino asit değişikliği onu işlevsiz hale getirebilir. Bu değişiklikler, eksik parçaların yeni çözümlerle nasıl ikame edilebileceğini ve temel fırlatma ilkesinin nasıl korunabildiğini gösterir.
Akıllı kontroller: saldırı modunun mantıklı olduğu zamanlar
Bu nanomakineyi inşa etmek ve ateşlemek pahalıdır; bu yüzden Acinetobacter onu sıkı kontrol altında tutar. Küresel bir DNA bağlayıcı protein (H‑NS) ve çoklu ilaç dirençli plazmidlerde taşınan özel baskılayıcılar sistemi “kapalı” konuma kilitleyebilir, özellikle direnç genleri hücreler arasında paylaşıldığında. Yüksek hücre yoğunluğunda kimyasal “çapraz” (quorum) sinyalleri sistemi açabilir ve bakterileri yakın mesafe rekabetine hazırlar. Metal iyonları da rol oynar: oksidatif stres altında içeri alınan manganez, anahtar T6SS mesajlarının yok edilmesine yol açan küçük bir RNA'yı aktive ederek silahı azaltır ve konak içinde hayatta kalmayı destekler. Kapsül — şekerli dış örtü — hem kalkan hem de fren görevi görür; gelen saldırıları engelleyip aynı zamanda Acinetobacter'in kendi ateşlemesini fiziksel olarak sönümlendirir.
Mikroskobik darbelerin çeşitli aleti
Acinetobacter tetiklediğinde, geniş bir toksin yelpazesi teslim edebilir. Bazı enzimler rakiplerin dayanıklı hücre duvarını parçalarken; diğerleri hücre zarlarını sessizce aşındırır, bazıları ise hedef hücre içindeki DNA'yı keser. Her toksin, saldırganı dost ateşinden koruyan eşleşen bir “bağışıklık” proteiniyle eşleştirilmiştir. Şimdi TafE olarak adlandırılan bir DNA kesici toksin mantarları bile öldürebilir; bu da bağırsak veya akciğer gibi yerlerde krallıklar arası çatışmalara işaret eder. Genomik çalışmalar, Acinetobacter'un genellikle modüler taşıyıcılar olarak görev yapan büyük Rhs proteinleri içinde paketlenmiş hâlen tanımlanmamış daha birçok toksin kodladığını öne sürüyor. Bu bakteriler, tek bir darbeye güvenmek yerine, aynı anda birkaç hayati yapıyı zarar veren katmanlı saldırılar kullanıyor gibi görünmektedir.
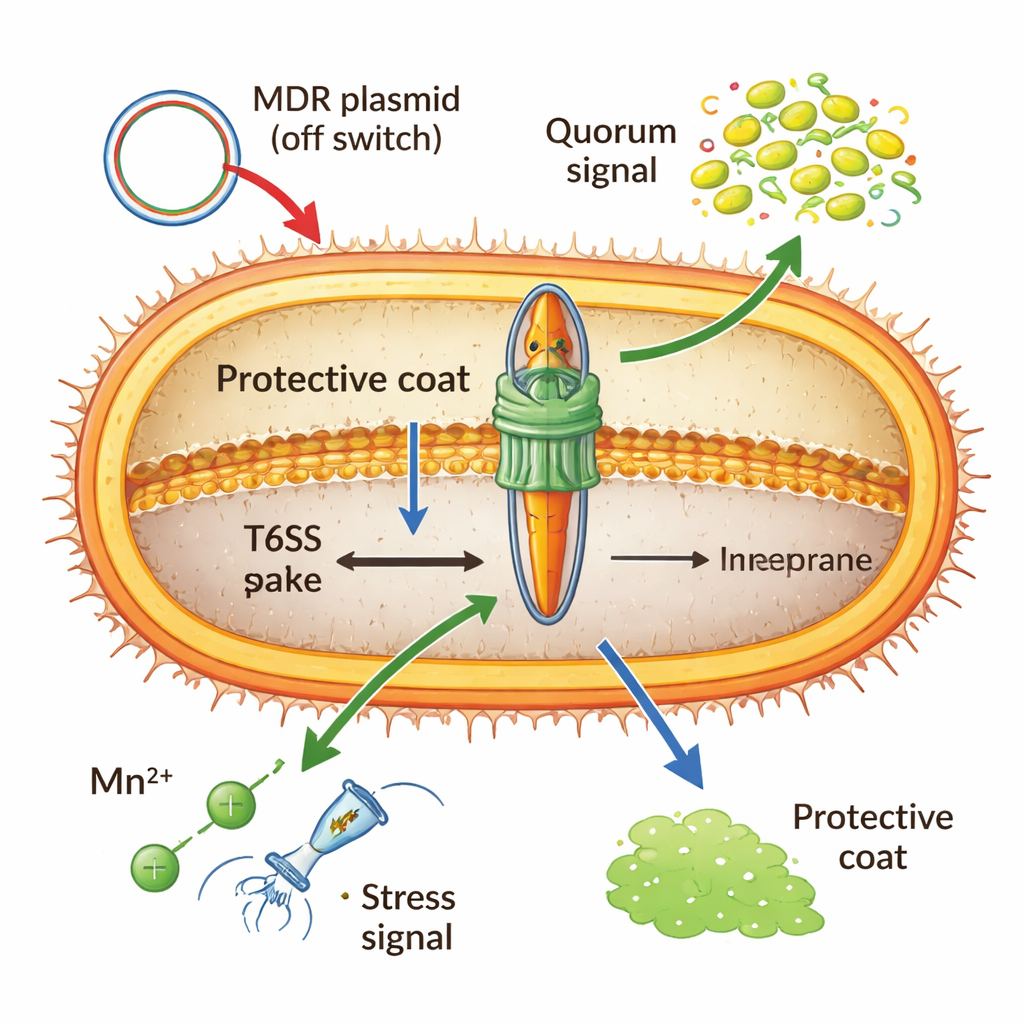
Enfeksiyonları, genleri ve gelecekteki tedavileri şekillendirmek
Hasta izolatları ve hayvan modellerinden elde edilen kanıtlar, aktif bir T6SS'in genellikle daha ağır hastalıklar, daha güçlü inflamasyon ve bakterilerin konak içinde daha iyi hayatta kalması ile birlikte olduğunu gösteriyor. Sistemin komşu mikropları öldürmesi ayrıca doğal olarak kompetan Acinetobacter hücrelerinin alabileceği DNA'yı serbest bırakarak antibiyotik direnç gibi özelliklerin yayılmasını hızlandırır. Yine de silahı sürekli aktif tutmak masraflıdır; bu yüzden birçok başarılı hastane suşu, direnç güvence altına alındıktan sonra onu susturan plazmidler veya mutasyonlar taşır. Genel olarak yazarlar, bu salgılama sisteminin basit bir virülans faktörü olarak değil, Acinetobacter'un saldırganlık, dayanıklılık ve enerji kullanımı arasında denge kurmak için açıp kapattığı esnek bir “uyum modülü” olarak görülmesi gerektiğini savunuyor. Bu yeni görüş, korunan T6SS parçalarını hedef alan aşılar ya da ateşleme mekanizmasını seçici olarak kilitleyen ilaçlar gibi pratik uygulamalara işaret ediyor; bunlar doktorların tehlikeli ve uyum sağlayabilen bir hastane düşmanını alt etmesine yardımcı olabilir.
Atıf: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Anahtar kelimeler: Acinetobacter, tip VI salgılama sistemi, antibiyotik direnci, bakteriyel rekabet, hastane enfeksiyonları