Clear Sky Science · tr
RLR ve cGAS-STING doğuştan gelen bağışıklık sinyal yolaklarının dinamik düzenleyicisi olarak glikozilleme
Şeker Etiketleri Hücrelerin Virüsleri Nasıl Hissettiğine Nasıl Yardımcı Olur
Hücrelerimiz sürekli olarak istilacı virüslere karşı tetikte ve bu savunmanın büyük bir kısmı proteinlere bağlanmış küçük şeker etiketlerine dayanır. Bu derleme, glikozilleme olarak bilinen bu şeker etiketlerinin ana antiviral yolaklar için basit bir açık/kapat düğmesi yerine kısma anahtarları gibi davrandığını açıklar. Bu şeker bazlı ince ayarı anlamak, aşıları güçlendirmenin, viral enfeksiyonları tedavi etmenin ve hatta bağışıklık sistemini kanserle mücadelede kullanmanın yeni yollarını açabilir.
Hücrenin Erken Uyarı Alarmı
Virüsler bir hücreye girdiğinde, arkalarında belirgin RNA veya DNA iplikçikleri bırakırlar. Özelleşmiş “alarm” sistemleri hücrenin içini bu genetik artıklar için devriye gezer. RIG-I-benzeri reseptör (RLR) yolu olarak adlandırılan bir sistem viral RNA’yı algılar. cGAS–STING yolu olarak bilinen diğer bir yol ise hücrenin yanlış bir yerinde beliren DNA’yı hisseder. Tetiklendiklerinde, her iki yol da tip I interferonlar ve inflamatuar moleküllerin salınımıyla sonuçlanan kimyasal kaskatları açar—komşu hücreleri uyaran ve bağışıklık savunmalarını seferber eden güçlü sinyaller. Bu yanıtın çok fazla veya çok az olması tehlikeli olabileceğinden, hücrenin bu alarmları dikkatlice ayarlaması gerekir ve glikozilleme bunun başlıca yollarından biridir. 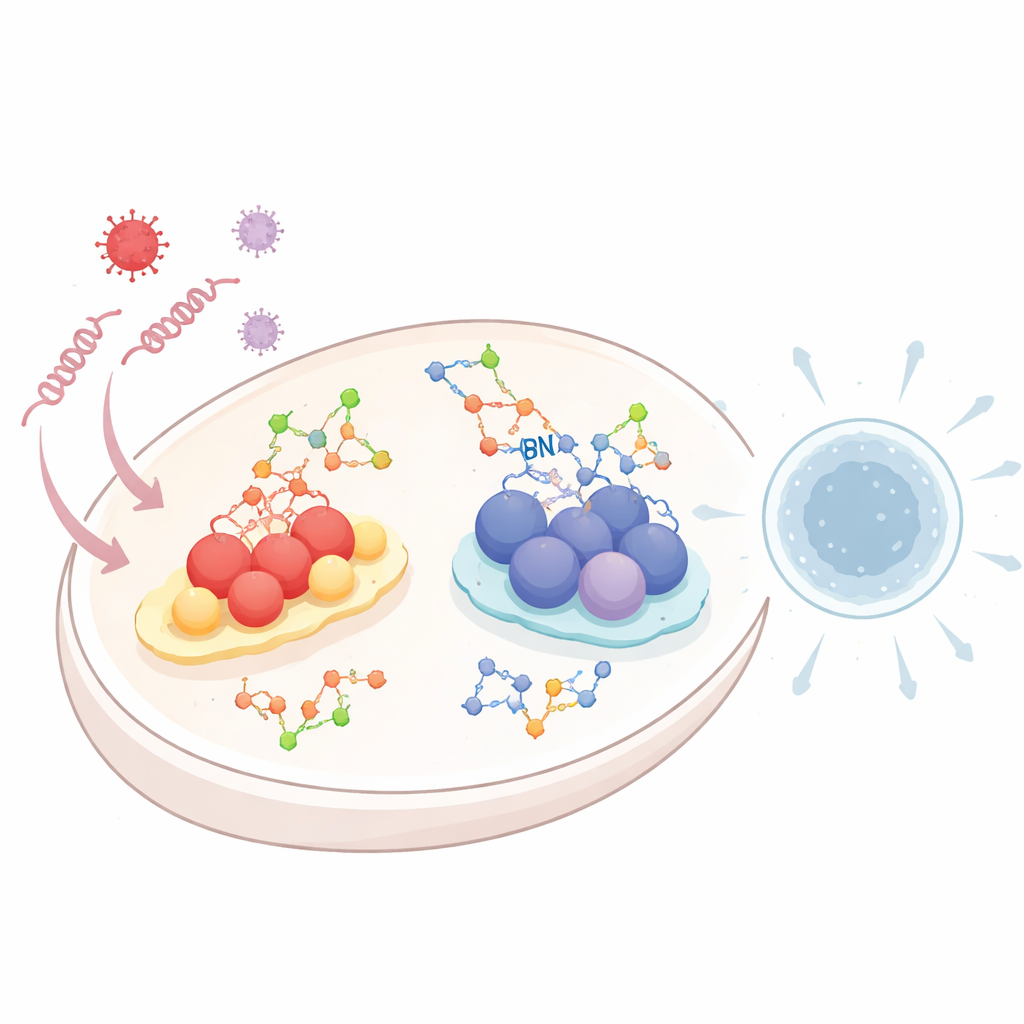
Hassas Kontroller Olarak Şeker Kaplamaları
Glikozilleme, farklı hücresel konumlarda proteinlere küçük şeker birimleri ekler. Hücrenin iç nakliye ağı olan endoplazmik retikulum ve Golgi'de, hacimli N-bağlı şeker zincirleri proteinlerin doğru katlanmasına, kararlı kalmasına ve doğru membrandaki yere ulaşmasına yardımcı olur. Buna karşılık, O-GlcNAcylation adı verilen daha yalın bir biçim sitoplazma ve çekirdekte proteinlere tek bir şeker yerleştirir. Bu minimalist etiket son derece dinamiktir; besin düzeyleri ve stres yanıtına göre iki enzim tarafından hızla eklenip çıkarılır. Derleme, bu farklı şeker türlerinin bağışıklık algılayıcılarını basitçe açıp kapatmadığını; bunun yerine algılayıcıların kümelenme kolaylığını, ömürlerini ve ne kadar güçlü sinyal verdiklerini ayarladığını anlatır. Bu şekilde glikozilleme, hücrenin metabolik durumunu enfeksiyonla savaşma hazırlığıyla doğrudan bağlar.
RNA Algılayıcı Yolunu Ayarlama
RNA algılayan RLR sisteminde, mitokondrilerde yer alan ve ana bir merkez görevi gören MAVS adlı merkezi bir röle proteini bulunur. Derleme, MAVS üzerindeki O-GlcNAcylation’ın şekere bağlanma yerine bağlı olarak antiviral sinyallemeyi hem hızlandırabileceğini hem de frenleyebileceğini gösterir. Bazı bölgelerdeki şeker etiketleri, MAVS’in büyük sinyal kümeleri oluşturmasına ve RNA virüslerine karşı güçlü interferon üretimini tetiklemesine yardımcı olan belirli bir tip ubiquitin zinciri gibi daha fazla protein modifikasyonunu teşvik eder. Diğer şeker siteleri ise normal koşullar altında MAVS’in sessizce dağınık ve inaktif kalmasını sağlayarak gereksiz inflamasyonu önler. Viral enfeksiyon ve hücrenin şeker üreten metabolik yolundaki değişiklikler, bu aktive edici ve inhibe edici etiketler arasındaki dengeyi kaydırabilir. IRF5 adlı başka bir faktör üzerindeki ilgili modifikasyonlar bağışıklık sistemini zararlı “sitokin fırtınalarına” doğru itebilir; bu da daha fazla şekerin her zaman daha iyi olmadığını vurgular. Paralel olarak, virüsler büyüme faktörü reseptörü EGFR gibi hücre yüzeyindeki proteinlerdeki N-bağlı şekerleri kullanarak RIG-I gibi yukarı akış sensörlerini degradasyona işaretleyebilir ve antiviral savunmaları köreltebilir.
DNA Algılayıcı Yolunu Ayarlama
DNA algılayan cGAS–STING yolu da glikozillemeden güçlü biçimde etkilenir. Endoplazmik retikulumdaki bir membran proteini olan STING, doğru katlanmak, kararlı kalmak ve DNA kaynaklı haberciler tarafından aktive edildikten sonra sinyal kümeleri oluşturmak için N-bağlı şeker zincirlerine ihtiyaç duyar. Bu şekerler olmadan STING, güçlü interferon salınımı için gereken daha yüksek düzen yapıları oluşturamaz ve hücre bölmeleri arasında gerekli trafiği sağlayamaz. Aynı zamanda STING’in belirli bir sitesindeki O-GlcNAcylation, kümelenmesini ve hareketini teşvik eden farklı bir dizi kimyasal etiketi güçlendirerek DNA virüslerine karşı antiviral sinyalleri artırır. Golgi'de inşa edilen sülfatlanmış glikozaminoglikanlar adı verilen şeker zincirleri ise aktive olmuş STING’in uzun yapılar halinde polimerleşmesine ve aşağı akış enzimlerini toplamasına yardımcı olarak ek destek sağlar. Virüsler, kendi glikoproteinlerini değiştirerek veya STING’i hedef alan degradasyon yollarını tetikleyerek karşı saldırıya geçer; bu genellikle bu şeker süslemelerinin eklendiği veya işlendiği aynı hücresel alanlarda gerçekleşir. 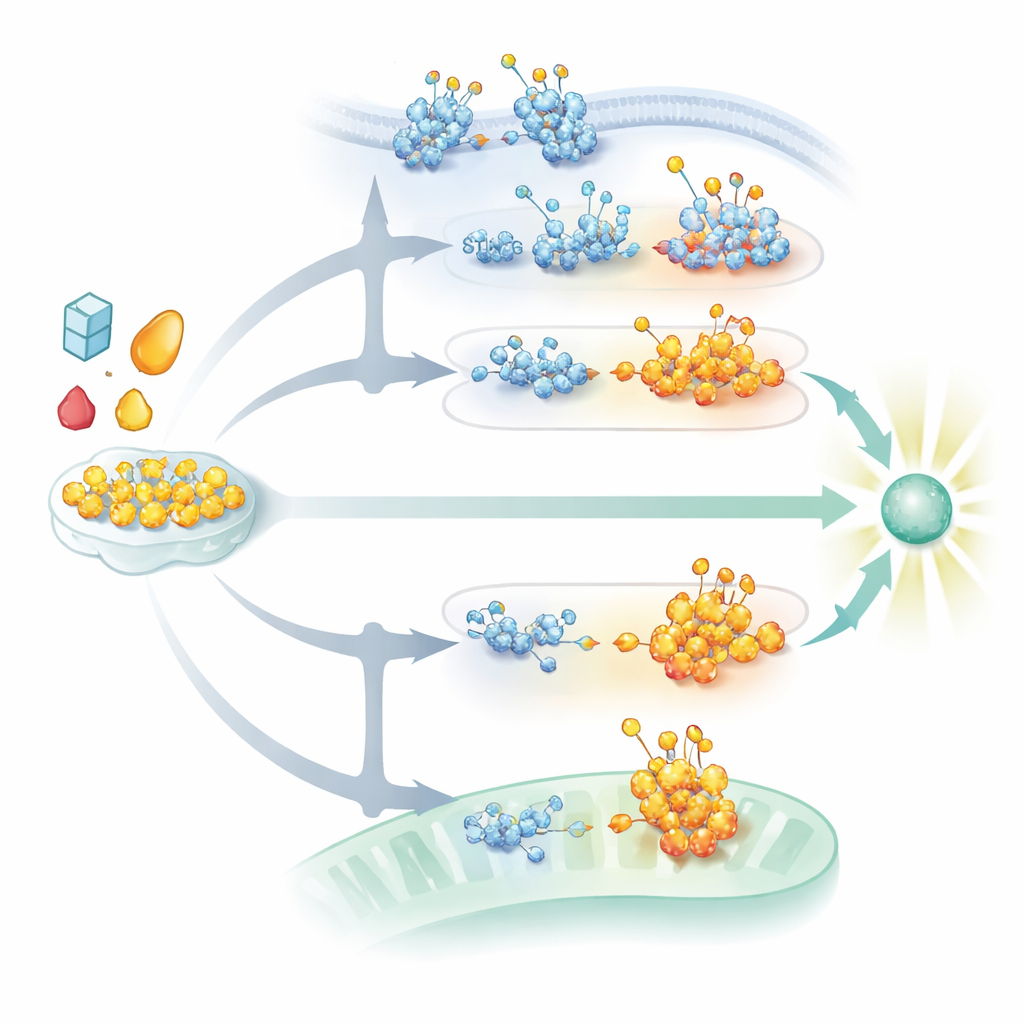
Metabolizma, Hastalık ve Gelecek Tedaviler
O-GlcNAcylation için ana şeker vericisi, hekzosamin biyosentetik yol olarak bilinen bir metabolik yol tarafından üretildiğinden, besin kullanımındaki değişimler doğrudan antiviral sinyallemeyi şekillendirir. Birçok virüs bu yolu kendi yararına yönlendirir; deneysel olarak hekzosamin akışını artırmak veya engellemek hayvan modellerinde antiviral yanıtları güçlendirebilir veya zayıflatabilir. Derleme bu mekanizmaları insan hastalıklarıyla ilişkilendirir: tümörler sıklıkla interferon sinyallemesini bastırmak ve bağışıklıktan kaçmak için glikozillemeyi yeniden düzenlerken, kronik metabolik stres veya glikan işleme bozukluklarındaki kalıtsal hatalar dengeyi zararlı otoimmüniteye doğru kaydırabilir. Yazarlar, özellikle O-GlcNAc ekleyen veya çıkaran ya da temel N-bağlı yapıları inşa eden enzimlerin umut verici ama zorlu ilaç hedefleri olduğunu savunur. Gelecekteki terapilerin büyük olasılıkla bölge-spesifik ve bağlama duyarlı biçimde hareket etmesi gerekecek; böylece enfeksiyonlar, kanser ve inflamatuar bozukluklara karşı daha iyi koruma sağlanırken yeni bağışıklık dengesizlikleri tetiklenmez.
Günlük Sağlık İçin Büyük Resim
Günlük terimlerle bu makale, vücudun ön saftaki antiviral alarmlarının izole çalışmadığını—enerji kullanımı ve şeker kimyasıyla bağlantılı olduğunu ortaya koyuyor. Bir avuç kritik proteindeki küçük şeker etiketleri, bir yabancı viral genomun ölçülü bir uyarı mı, tam teşekküllü bir savunma mı yoksa tehlikeli bir aşırı tepki mi tetikleyeceğine karar verir. Bu şeker bazlı kontrol sistemini çözerek ve nihayetinde ayarlamayı öğrenerek araştırmacılar, aşıları daha etkili hale getirecek, inatçı enfeksiyonları temizlemeye yardımcı olacak, tümörleri bağışıklık sistemine açığa çıkaracak ve otoimmün hastalıklarda kontrolden çıkmış inflamasyonu yatıştıracak tedaviler tasarlamayı umut ediyorlar.
Atıf: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
Anahtar kelimeler: doğuştan gelen bağışıklık, glikozilleme, RLR yolu, cGAS-STING, O-GlcNAcylation