Clear Sky Science · tr
Büyüme hızı odaklı modelleme, fenotipik adaptasyonun BRAFV600E-mutan melanomada ilaç direncine yol açtığını öne sürüyor
İlaçlarla Birlikte Yaşamayı Öğrenen Kanser Hücreleri
Hedefe yönelik ilaçlar, ciddi bir cilt kanseri olan melanomlu birçok kişinin tedavisinde devrim yarattı. Yine de bu ilaçlar neredeyse her zaman etkisini yitiriyor: bir zamanlar küçülen tümörler tekrar büyümeye başlıyor. Bu çalışma basit ama güçlü bir soruyu gündeme getiriyor: melanom hücreleri yalnızca genetik mutasyonlara dayanmak yerine, davranışlarını değiştirerek tedaviden “öğrenip” hayatta kalmayı başarabilir mi—ve bu öğrenme, ilaç verme biçimlerinden bazılarının neden diğerlerinden daha iyi çalıştığını açıklayabilir mi?
Duyarlı Hücrelerden Sağ Kalanlara
Araştırmacılar, BRAF adı verilen bir gendeki yaygın bir değişikliği taşıyan ve BRAF inhibitörü adı verilen bir ilaç türüne özellikle duyarlı olan melanom hücrelerine odaklandı. Önceki laboratuvar çalışmalarında bu hücreler farklı dozlarda ve farklı sürelerde encorafenib ilaçına maruz bırakıldı. Her koşul altında hücrelerin ne kadar hızlı çoğaldığını veya öldüğünü dikkatle ölçerek yazarlar hücreleri iki geniş kategoriye ayırdı: daha önce ilaca maruz kalmamış olan ilaç-naif hücreler ve en az bir hafta boyunca ilaçta yaşamış olan ilaç-adapte hücreler. İlaç-naif hücreler tedavi olmadan iyi büyürken ilaca güçlü şekilde yavaşlıyor veya ölüyordu. Buna karşılık, ilaç-adapte hücreler ilacın varlığında daha iyi büyüdü ama ilaç çıkarıldığında bu avantajı kaybetti—bu da hayatta kalmalarının kalıcı genetik hasardan ziyade esnek, geri döndürülebilir bir durum değişikliğiyle bağlantılı olduğuna işaret ediyordu.
Gizli Hücre Davranışlarının Haritası
Bu değişiklikleri anlamak için ekip her kanser hücresine “fenotip durumu” atayan bir matematiksel model kurdu—çok duyarlıdan çok dirençliye kadar uzanan bir ölçek üzerinde soyut bir konum. Sadece iki hücre türü varsaymak yerine, direnç göstergelerindeki kademeli değişimleri yansıtacak şekilde birçok ara duruma izin verdiler. Her durum ve ilaç dozu kombinasyonu için net bir büyüme hızı tahmin edildi; bu hız pozitif (ölümlerden daha fazla bölünme) veya negatif (bölünmelerden daha fazla ölüm) olabiliyordu. Tüm bu hızlar bir ızgaraya, yani bir “uyum matrisi”ne yerleştirildi ve bu bir peyzaj gibi davrandı: bazı durumlar bazı dozlarda hücrelerin gelişmesi için elverişliyken, diğerleri ölümcül. Modeldeki hücreler, tedavi açılıp kapandıkça bu peyzaj üzerinde adım adım hareket edebiliyordu.
Hücreler Avantaja Doğru Sürüklenir mi yoksa Tırmanır mı?
Ana belirsizlik, hücrelerin bu peyzaj üzerinde nasıl hareket ettiğiydi. Yazarlar dört olası stratejiyi test etti. Birinde hücreler asla durum değiştirmiyor; bu nedenle herhangi bir dirençli hücre başlangıçtan itibaren var olmalıydı. Başka birinde hücreler durumları ne kadar iyileşirse iyileşsin, iyileşmese de, komşu durumlar arasında rastgele dolaşıyordu—sarhoşun yürüyüşü gibi. Kalan iki stratejide ise hücreler büyüme hızlarının daha yüksek olduğu durumlara doğru eğilim gösteriyordu—ya gürültülü bir şekilde, bazı yanlış adımlarla, ya da güçlü bir şekilde, her zaman daha iyi hayatta kalma koşullarına tırmanarak. Ekip bilgisayar simülasyonlarını çalıştırıp bunları özellikle ilaç sürekli verildiğinde veya aralıklı olarak (bir hafta açık, bir hafta kapalı) uygulanan gerçek laboratuvar verileriyle karşılaştırdığında, yalnızca hücrelerin daha yüksek uyum yönüne tırmandığı stratejiler gözlemlenenleri yeniden üretebildi: yüksek dozda aralıklı tedavi, aynı toplam süre ve daha yüksek toplam ilaç miktarıyla sürekli tedaviye göre hücre sayısını daha iyi baskıladı.
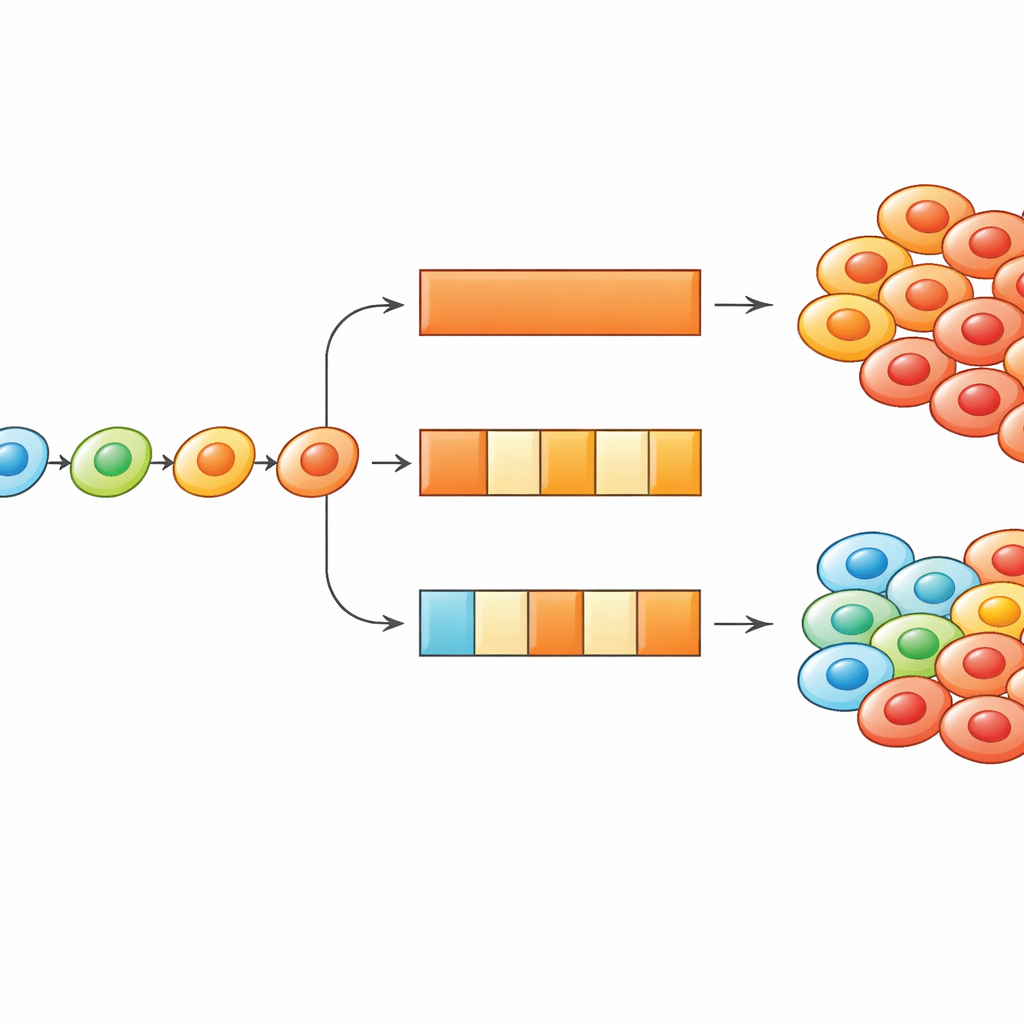
Adaptasyonu Kanserin Aleyhine Çevirmek İçin Aç-Kapa Dozlamayı Kullanmak
Daha derine inerek, araştırmacılar hem simülasyonları hem de daha basit denklemleri kullanarak hücrelerin ne sıklıkla durum değiştirmelerine izin verildiğini ve ilaça açık/kapalı dönemlerin ne kadar sürdüğünü inceledi. Yönlendirilmiş şekilde adapte olduklarında, tedavi programlarının bu adaptasyonu ya yavaşlatacak ya da onu avantaja çevirecek şekilde ayarlanabileceğini buldular. Hücrelerin durumlarını güncelleyebilme sıklığını kısaltmak—kavramsal olarak fenotipik değişimi mümkün kılan biyolojik mekanizmaları yavaşlatmak—aralıklı tedavileri daha güçlü kılma eğilimindeydi, çünkü hücreler çok hızlı biçimde yüksek dirençli durumlara tırmanamıyordu. Tersine, hücreler şiddetli dirençli bir durumda başlarsa, ilaç tatilleri onların daha duyarlı durumlara geri kaymalarına zaman tanıyabiliyor; böylece ilacın yeniden verilmesi hücre ölümünde bir patlama tetikliyor. Çalışma, dozlamanın zamanlaması ile hücresel adaptasyon hızının birlikte hangi programın en iyi sonucu verdiğini şekillendirdiğini gösteriyor.
Geleceğin Kanser Bakımı İçin Anlamı
Bir sivil için temel mesaj, kanser hücrelerinin sabit düşmanlar olmadığı; şekil değiştiren varlıklar olduğudur. Bu melanom sisteminde hücreler karşılaştıkları koşullar altında büyümelerine yardımcı olan davranışlara doğru aktif olarak hareket ediyor gibi görünüyor. Yazarların modeli, farklı kalıcı klonları devreye sokmadan—sadece yönlendirilmiş adaptasyonla—niçin aç-kapa ilaç programlarının bazen sürekli dozlamayı yendiğini ve hatta daha az toplam ilaç kullandıklarında bile bunu açıklayabileceğini öne sürüyor. Bu sonuçlar laboratuvarda yetiştirilen hücrelerden elde edildiği ve hasta bakımına yönlendirmeden önce daha fazla çalışma gerektirdiği halde, yaklaşım pratik bir çerçeve sunuyor: kanser hücrelerinin ne kadar hızlı ve hangi yönde adapte olduğunu ölçerek, doktorlar nihayetinde sadece tümörleri yok etmeye çalışmakla kalmayıp fenotipik “öğrenmelerini” çıkmaz sokaklara yönlendiren tedavi programları tasarlayabilirler.
Atıf: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Anahtar kelimeler: melanom, ilaç direnci, hücre plastisitesi, aralıklı tedavi, matematiksel modelleme