Clear Sky Science · tr
Neisseria meningitidis kinole bağlı nitrik oksit redüktazının dimerleşme ile aktivasyonunun yapısal temeli
Hücresel Bağışıklık Savunmasını Bakterilerin Nasıl Atlatabildiği
Zararlı bakteriler vücuda girdiğinde bağışıklık hücrelerimiz onları öldürmek için nitrik oksit gibi toksik moleküller salgılar. Ancak bazı patojenler bu saldırıyı etkisiz hale getirmek ve hayatta kalmak için moleküler hileler geliştirmiştir. Bu çalışma, önemli bir bakteri enzimlerinin atomik ayrıntıda nasıl çiftler hâline gelerek nitrik oksiti detoksifiye etmede çok daha etkin hâle geldiklerini ve bu şekil değiştirme davranışının neden antibiyotik tasarımına yeni yollar açabileceğini ortaya koyuyor.
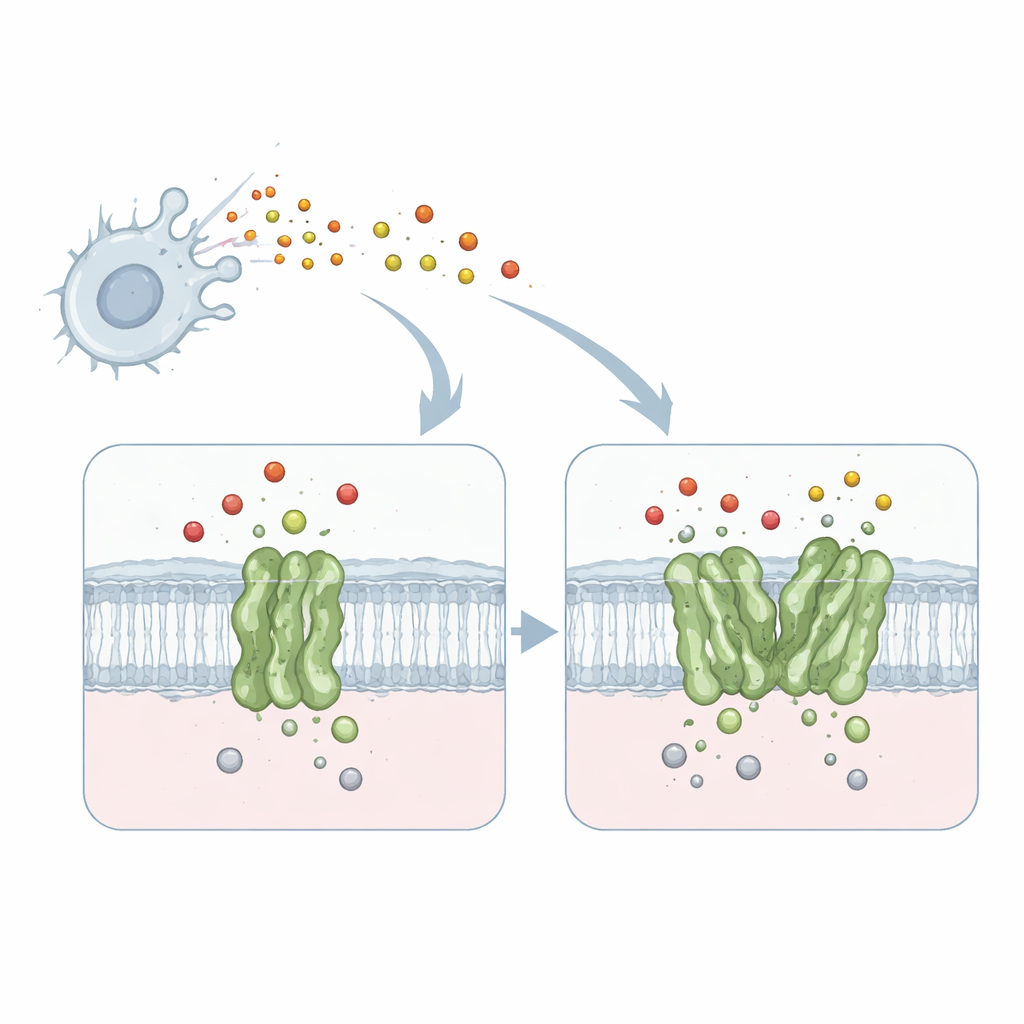
Toksik Bir Gazı Nötralize Eden Küçük Bir Makine
Çalışma, menenjit yapan bakteri Neisseria meningitidis’ten kinole-bağımlı nitrik oksit redüktaz adı verilen bir zar proteini olan qNOR üzerinde yoğunlaşıyor. qNOR, bakteri hücre zarında yer alır ve bağışıklık sistemimiz tarafından üretilen toksik bir gaz olan nitrik oksiti daha az zararlı ürünlere dönüştürür. Bu detoksifikasyon, mikroorganizmanın insan makrofajları gibi düşmanca ortamların içinde bile solunum yapmaya ve çoğalmaya devam etmesine olanak tanır. Solunum ve nitrik oksit uzaklaştırma patojenin hayatta kalması için hayati olduğundan, qNOR yeni antimikrobiyal ilaçlar için cazip bir hedeftir.
Tek Olması İyi Ama İkisi Daha İyi
Önceki biyokimyasal çalışmalar qNOR’un ya tek birim (monomer) ya da çift (dimer) hâlinde bulunabildiğini ve dimerin nitrik oksiti nötralize etme konusunda iki ila dört kat daha hızlı çalıştığını göstermişti. Şimdiye dek aynı enzimin iki kopyasının sadece eşleşmesinin performans üzerinde neden bu kadar dramatik bir etki yarattığı belirsizdi. Bunu açıklamak için araştırmacılar aynı bakteri suşundan hem monomerik hem de dimerik qNOR’un yüksek çözünürlüklü tek partikül kryo-elektron mikroskopisi ile üç boyutlu yapılarını yakaladılar. Dimer için 1.89 ångström ve monomer için 2.25 ångström olmak üzere yakın atomik çözünürlükte görüntüler elde ettiler — tek tek amino asit yan zincirlerini, metal iyonlarını ve birçok su molekülünü konumlandıracak kadar net.
Esnek Bir Heliks, Stabilize Edici Bir Destek Haline Geliyor
Şaşırtıcı bir şekilde, enzimin katalitik merkezi — nitrik oksitin dönüştüğü metal merkezi — her iki formda da neredeyse aynı görünüyordu. Bunun yerine ana farklar biraz uzakta, TM10 adlı bir transmembran heliksinde ve iki qNOR molekülü çiftleştiğinde bunun TM2 adlı başka bir heliksle nasıl temas ettiğinde ortaya çıktı. Monomerde TM10 gevşekçe ankastre olmuş ve kryo-EM verilerinin hesaplamalı analizinin gösterdiği üzere önemli ölçüde sallanıp bükülebiliyordu. Dimerde ise her bir partnerin TM10’u komşusuna karşı kilitlenip dört heliksli bir demet oluşturarak hareketini büyük ölçüde kısıtlıyordu. Bu stabilizasyon kritik bir amino asidi, Glu563 adlı bir glutamatı, aktif bölgeye yakın başka bir glutamat olan Glu494’e yaklaştırarak gelen protonlar için daha odaklı bir yol şekillendiriyordu.
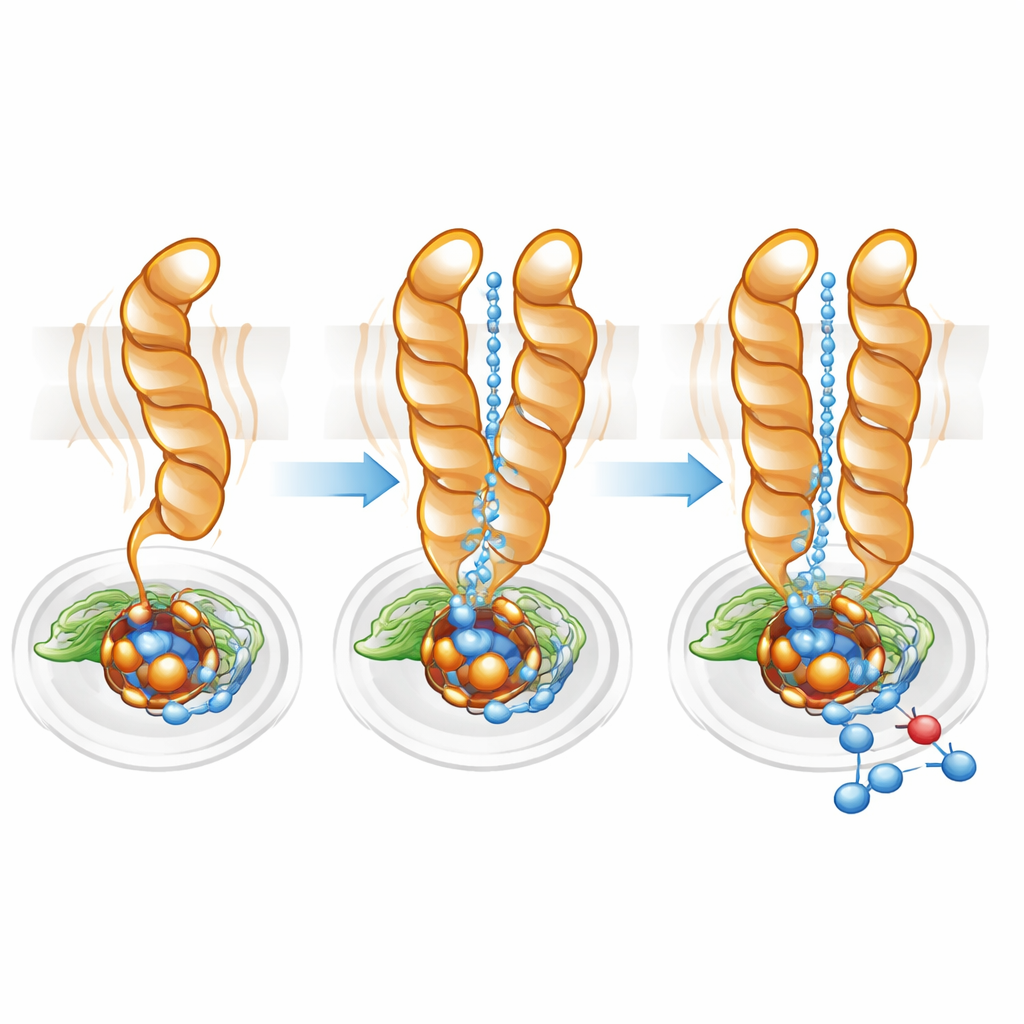
Proton Otoyolunu İnce Ayarlamak
Protonlar — pozitif yüklü hidrojen iyonları — nitrik oksit indirgenmesinin ilerleyebilmesi için hücre içinden gömülü aktif bölgeye verimli biçimde iletilmelidir. Yol haritası çıkaran yazılımlar kullanılarak ekip, hem monomerde hem de dimerde sitoplazmayı aktif bölgeye bağlayan hidrofilik bir boşluk buldu. Ancak monomerde bu kanal daha geniş ve daha dağınık olup, TM10’un daha büyük hareketliliğiyle tutarlıydı. Dimerde TM10’un kilitli pozisyonu ve Glu563’ün elverişli yönelimi daha doğrudan, daha iyi organize olmuş bir yol tanımlanmasına yardımcı oldu. Glu563’ü aynı etkileşimleri kuramayan amino asitlere mutasyonla değiştirmek enzimin aktivitesini normalin %10’unun altına düşürdü ve dimeri de kararsızlaştırdı; ilgili pozisyonlardaki diğer mutasyonlar ise aktif bölgedeki gerekli olmayan demirin miktarını azalttı. Birlikte bu sonuçlar, dimer oluşumu ile Glu563 ve Glu494’ün hassas konumlandırılmasının hem yapısal bütünlükle hem de katalitik verimle sıkı bağlantılı olduğunu gösteriyor.
Yapısal Bulguları Yeni Tedavilere Dönüştürmek
Bu bulgular, zar yüzeyinde protein eşleşmesinden aktif bölgenin derinliklerindeki ince ayarlara kadar uzanan ve qNOR’un nitrik oksiti ne kadar etkili uzaklaştırdığını kontrol eden açık bir bağlantı ortaya koyuyor. Basitçe söylemek gerekirse, enzimden iki kopya bir araya geldiğinde esnek bir segment düzleşip sertleşiyor; bu segment protonları reaksiyon merkezine yönlendirmeye yardımcı olarak enzimin çıktı düzeyini arttırıyor. İlaç geliştirme açısından bu, gelenekselin dışında bir strateji öneriyor: aktif bölgeyi doğrudan engellemek yerine, dimeri ayıran veya Glu563–Glu494 etkileşimini bozan moleküller tasarlamak, enzimi yavaş monomerik hâline zorlayabilir. qNOR ve ilgili enzimler birkaç tehlikeli, ilaçlara dirençli patojenin hayatta kalması için kritik olduğundan, yapı kılavuzluğunda geliştirilecek yaklaşımlar bir sonraki nesil hedefe yönelik antimikrobiyallere katkıda bulunabilir.
Atıf: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Anahtar kelimeler: nitrik oksit detoksifikasyonu, bakteriyel solunum, zar enzimleri, kryo elektron mikroskopisi, antimikrobiyal ilaç hedefleri