Clear Sky Science · tr
Uzamsal multiomik, karaciğer kanserinde geri dönüşsüz elektroportasyonun iltihabi marjindeki immün-metabolik özelliklerini ortaya koyuyor
Neden yeni bir karaciğer kanseri tedavisi daha yakından incelenmeli
Geri dönüşsüz elektroportasyon (IRE), tümörü ısı yerine kısa, yüksek voltajlı elektrik darbeleriyle yoklamanın görece yeni bir yolu. Yakınlardaki kan damarları ve safra kanallarını koruyabilmesi nedeniyle hassas konumlardaki kanserler için özellikle yararlı. Buna rağmen hastaların üçte birine kadarında tümör, tedavi edilen bölgenin hemen yanında yeniden ortaya çıkıyor. Bu çalışma, IRE sonrası o dar sınır bölgesinde neler olduğunu —ve oradaki bağışıklık hücreleri ile hücresel metabolizmada gizli değişikliklerin sessizce kanserin yeniden çıkışını hazırlayıp hazırlamadığını— sorguluyor.
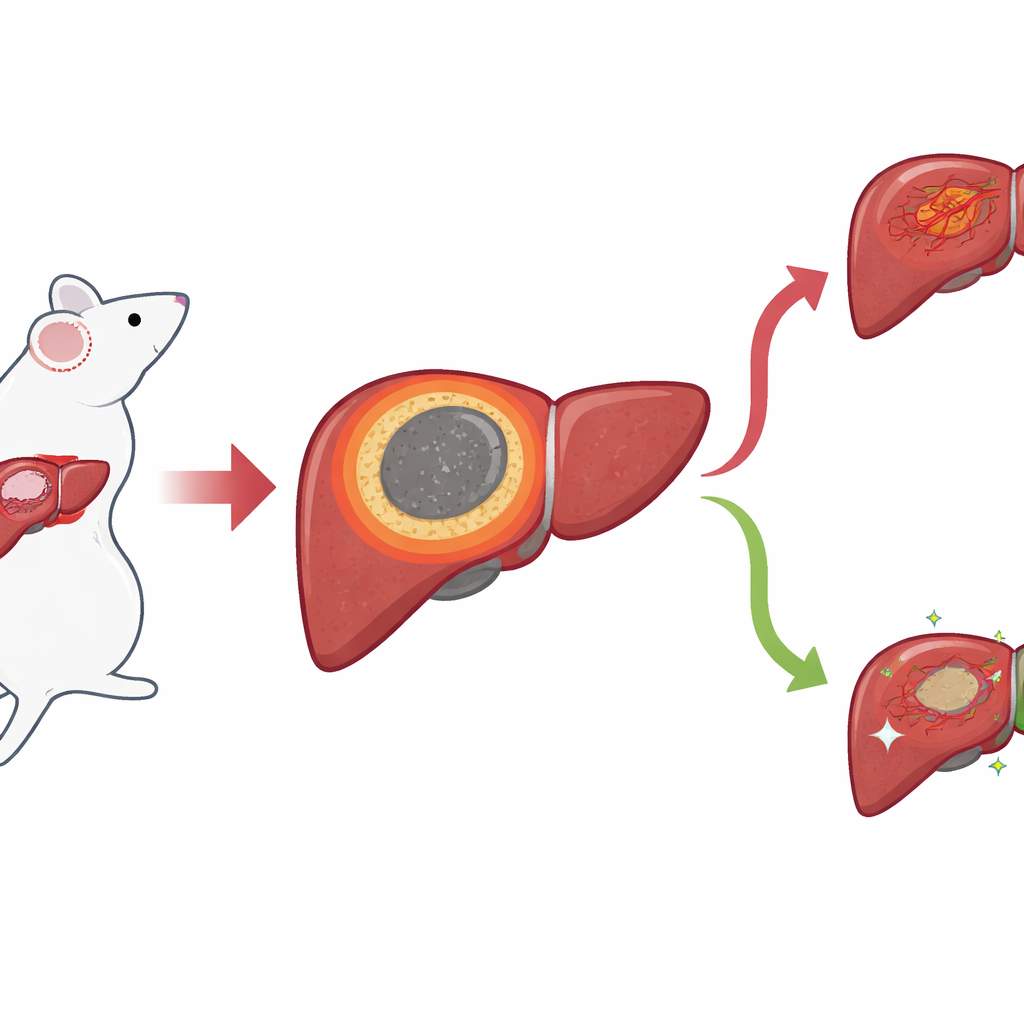
Büyük sonuçları olan dar bir sınır
Araştırmacılar, bir fare karaciğer kanseri modeli kullanarak, IRE sonrası ölü, ablasyon merkezi ile çevredeki sağlıklı karaciğer arasında oluşan ince doku halkasına odaklandılar. Buna iltihabi marj (IM) adını verdiler. Standart mikroskop görüntüleri, bu bölgenin yerel nükslerin tipik olarak ortaya çıktığı yerde oturduğunu gösterdi, ancak sınırlarını göze bakarak çizmek zordu. Daha net bir görünüm elde etmek için ekip, dokudaki konumu korunurken hangi genlerin ve küçük moleküllerin bulunduğunu okuyabilen “uzamsal” yöntemleri uyguladı. Uzamsal transkriptomik ile spot spot gen etkinliğini haritalandırdılar ve nekrotik merkezi normal karaciğer ve tümör alanlarından ayıran, IM ile tam olarak çakışan belirgin bir spot kümesi keşfettiler.
Bağışıklık hücreleri toplanıyor — ama çoğu saldırıyı frenliyor
Sonra bilim insanları tek hücre ve tek çekirdek RNA dizilemesiyle birlikte güçlü bir profilleme yöntemi olan CyTOF’u kullanarak karaciğer genelindeki bireysel hücre tiplerini katalogladılar. IM’nin makrofaj adlı bir bağışıklık hücresi türü tarafından domine edildiğini buldular. Özellikle, “lipid-ile ilişkili makrofajlar”a (LAM’lar) benzeyen bir altküme IRE’den birkaç gün sonra IM’ye akın etti. Bu hücreler, T hücresi yanıtlarını baskılamasıyla bilinen PD-L1 gibi yüksek düzeyde yüzey belirteçleri ve gen imzaları taşıyordu. Gen ifadesi analizleri, bu makrofajların yutma (fagositik) kapasite, kimyasal çekicilere yanıt verme ve kanser hücrelerini öldürmek için gereken T hücrelerini baskılayabilecek sinyaller gönderme konusunda yetenekli olduğunu öne sürdü. Görüntüleme, PD-L1 pozitif makrofajların IM’de yakındaki normal dokuya göre çok daha bol olduğunu doğruladı.
Değişmiş yağ kimyasının bir sıcak noktası
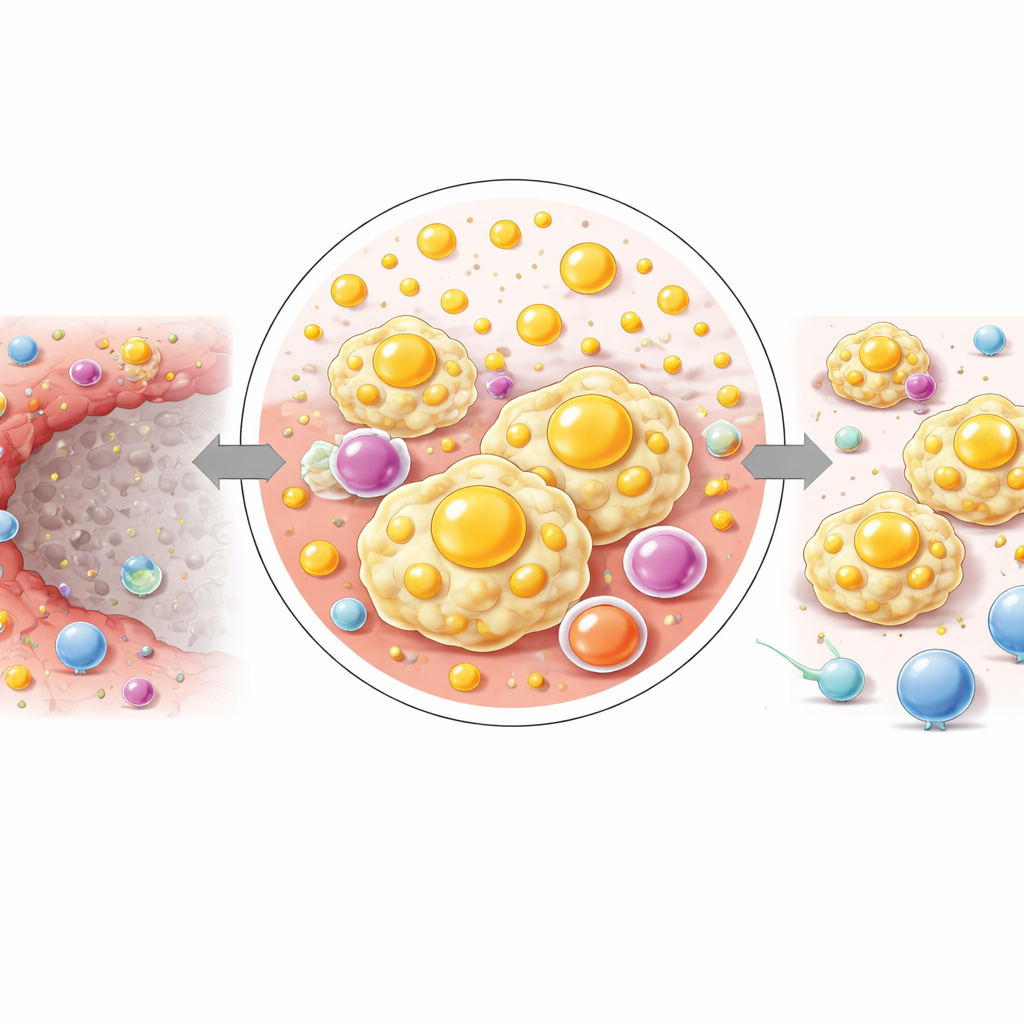
Dahası ekip, bu bağışıklık haritasını uzamsal metabolomikle üst üste koydu; bu, yüzlerce küçük molekülün dağılımını haritalayan bir kütle spektrometri görüntüleme yaklaşımı. IM’nin, ne ölü merkezinkine ne de çevre karaciğerkine benzeyen bir metabolik parmak izi olduğunu gösterdiler. Bu ince bantta birçok lipid (yağ ilişkili) yol güçlü şekilde artmıştı; doymamış yağ asitlerinin üretimi, arakidonik asit türevleri ve sfingolipidler dahil. Arakidonik asitten türeyen prostaglandinler ve lökotrienler gibi anahtar sinyal lipidleri IM’de zenginleşirken, aynı molekülü işleyen diğer enzim yolları nispeten sönüktü. Sfingolipid ailesinin bir başka grubuna ait seramidler ve sfingomiyelinler de toplandı; bunların yapımını ve yeniden düzenlenmesini sağlayan enzimlerin ifadesi artmıştı.
Hasardan yakıt açısından zengin bir nişe kademeli geçiş
Iltihabi marjı nekrotik merkezden dışa doğru üç ince katmana ayırarak araştırmacılar kimyada kademeli bir değişim gördüler. Ölü bölgeye en yakın olan tabakada karmaşık lipidler ve kolesterol ilişkili moleküller en yüksekti; daha dışa doğru, glukoz ve belirli amino asitler gibi küçük enerji ilişkili moleküller yükseldi. Bu desen, kısa bir mesafe içinde dokunun lipid yüklü, sinyalce zengin bir ortamdan hücre hayatta kalması ve büyümesini desteklemeye yönelik bir ortama geçtiğini gösteriyor. Yazarlar, bu kademeli yeniden programlamanın IM’yi domine eden lipid-aç makrofajları desteklemeye ve tümör hücrelerinin sessizce yeniden yerleşmesine zemin hazırlamaya yardımcı olabileceğini öne sürüyorlar.
Geleceğin karaciğer kanseri bakımında bunun anlamı
Basitçe söylemek gerekirse bu çalışma, IRE’nin sadece tümör hücrelerini öldürmekle kalmadığını; aynı zamanda bağışıklık hücreleri ve yağ kimyasının birlikte korunaklı, tümör-dostu bir mahalle yarattığı dar bir halka oluşturduğunu gösteriyor. Bu bölgedeki makrofajlar bol, lipid yüklü ve T hücrelerini devre dışı bırakmaya eğilimli. Bu değişiklikler belirli metabolik yolaklara sıkı sıkıya bağlı olduğundan yeni tedavi açıları öneriyor. Teorik olarak IRE’yi marjda lipid metabolizmasını hedef alan ilaçlarla veya PD-L1’i bloke eden ajanlarla birleştirmek, nüks eğilimli bir sınırı gerçekten kanserle mücadelede işi bitiren bir bölgeye dönüştürebilir.
Atıf: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Anahtar kelimeler: karaciğer kanseri, tümör ablasyonu, immün mikroçevre, makrofajlar, lipid metabolizması