Clear Sky Science · tr
NRF2 aktive edicileri ve nükleer ekport inhibitörü selinexor, ACE2, TMPRSS2 ve XPO1’i içeren bir ağı hedefleyerek NRF2-bağımsız bir mekanizma ile koronavirüsleri sınırlar
Hücrelerin Koronavirüslere “Hayır” Demesine Yardımcı Olan İlaçlar
Bugün çoğu koronavirüs tedavisi doğrudan virüsü hedef alıyor. Ancak virüsler değişime çok yatkın ve yeni varyantlar bu ilaçların etkisini hızla azaltabiliyor. Bu çalışma farklı bir stratejiyi araştırıyor: kendi hücrelerimizi tehlikeli SARS-CoV-2 gibi koronavirüslere ve daha hafif mevsimsel türlere karşı daha az konuksever hâle getirmek. Hücrelerin birkaç anahtar kapı mekanizmasını nasıl yönettiğini değiştirerek, araştırmacılar mevcut küçük moleküllerin laboratuvar modellerinde enfeksiyonu keskin şekilde azalttığını gösteriyor ve bunun, bu moleküllerin ünlü oldukları sıradan antiviral yolaklara dayanmadığı ortaya çıkıyor.
Koronavirüs Savunmasına Yeni Bir Açı
Takım, NRF2 adlı bir proteinin kontrol ettiği hücresel koruma programını aktive etmeleriyle bilinen bileşiklere odaklandı. Bu bileşikler—4-oktil itakonat (4OI), bardoksolon (BARD) ve sulforafan (SFN)—XPO1 adlı bir taşıyıcı proteini bloke eden selinexor (SEL) ile birlikte test edildi; XPO1, diğer proteinleri hücre çekirdeğinden dışarı taşımaya yardımcı olur. Akciğer ve böbrek hücre modellerinde, dört ilaç da hücrelere zarar vermeden SARS-CoV-2 düzeylerini azalttı. Ayrıca bir dizi endişe verici varyanta karşı da etkiliydiler. İlginç bir şekilde, NRF2 genetik olarak kaldırıldığında virüsler aslında daha iyi çoğalırken, NRF2’nin doğal olarak koruyucu olduğu kanıtlandı—ancak ilaçlar hâlâ iyi çalıştı; bu da antiviral güçlerinin farklı bir yoldan geldiğini gösteriyor. 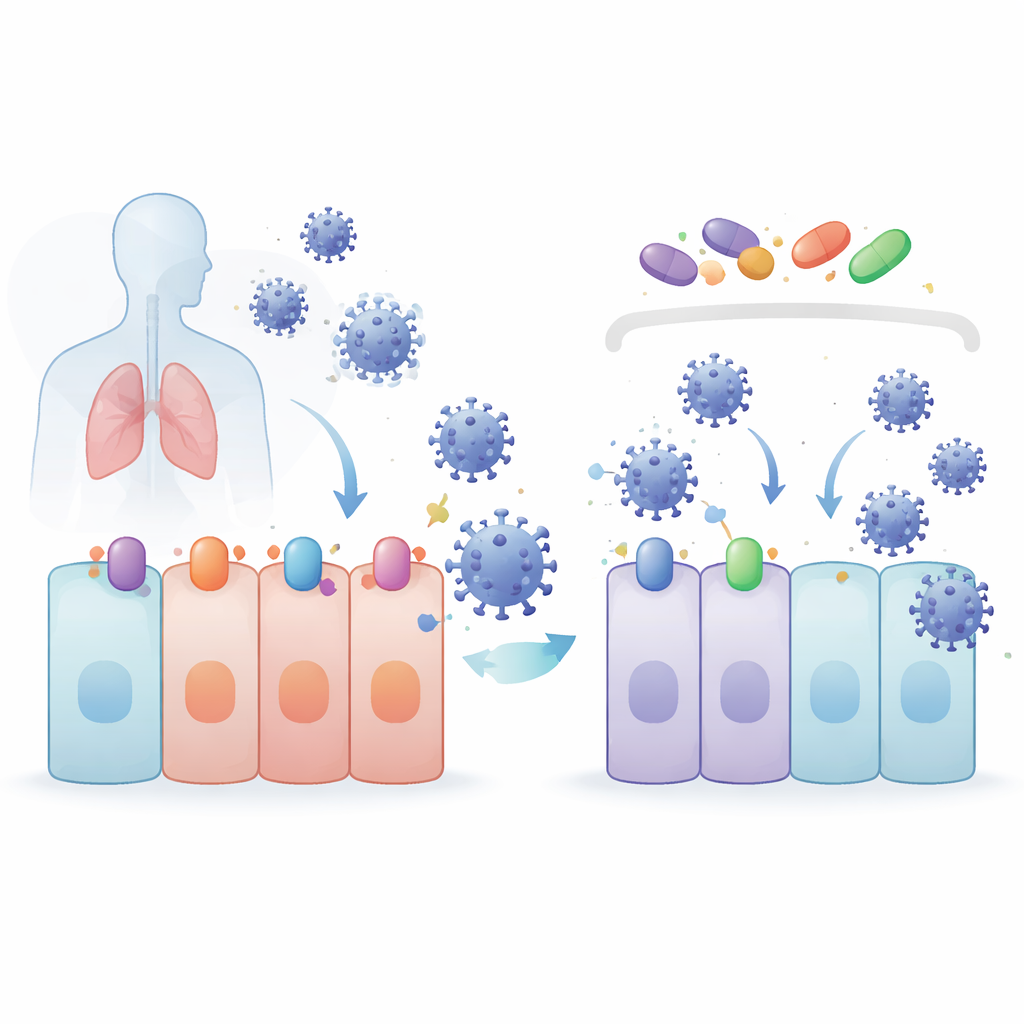
Viral Öndereyi Kapatmak
Koronavirüsler enfeksiyona, hücre yüzeyindeki reseptör proteinlerine tutunarak başlar. SARS-CoV-2 ve yakın akrabaları için ana kapı ACE2’dir ve bunu TMPRSS2 adlı bir kesici enzim yardım eder. İhracat proteini XPO1 de enfeksiyona katkıda bulunuyor gibi görünüyor. Araştırmacılar, 4OI, BARD, SFN ve SEL’in insan akciğer hücrelerinde ACE2, TMPRSS2 ve XPO1 miktarlarını azalttığını buldu. 4OI ve SEL özellikle enfeksiyon öncesinde var olduğunda güçlüydü ve koronavirüs spike proteinleriyle kaplı virüs benzeri partiküllerin girişini engellediler. Başka bir deyişle, bu ilaçlar virüs hücreye girdikten sonra yavaşlatmaktan öte—virüsün kapıyı açmak için ihtiyaç duyduğu kilitleri ve tutamakları ortadan kaldırmaya yardımcı oluyorlar.
Hücrelerin Temel Viral Yardımcılarını Nasıl Parçaladığı
Daha derine inen ekip, 4OI’nin ACE2 proteinini yıkımını hızlandırdığını gösterdi. Normal koşullarda ACE2 saatlerce dayanırken; 4OI ile hücre yüzeyinden çok daha kısa sürede kayboldu. Bu yıkım, proteinlere “imha et” işareti takan iki hücresel etiketleyici, NEDD4L ve MDM2 gerektiriyordu. Bu etiketleyicilerin bloke edilmesi 4OI’nin ACE2’yi ortadan kaldırma yeteneğini zayıflattı. Beklenmedik şekilde, olağan protein parçalama makinası olan proteazom ana yol değildi. Bunun yerine ACE2 hücrenin geri dönüşüm ve atık sistemi olan lizozoma yönlendirildi. İlaçlar ayrıca kısmen STAT3 aktivasyonunu azaltarak ACE2 ve XPO1 gen aktivitesini de düşürdü; STAT3 normalde ACE2 gen okumasını artıran bir proteindir. 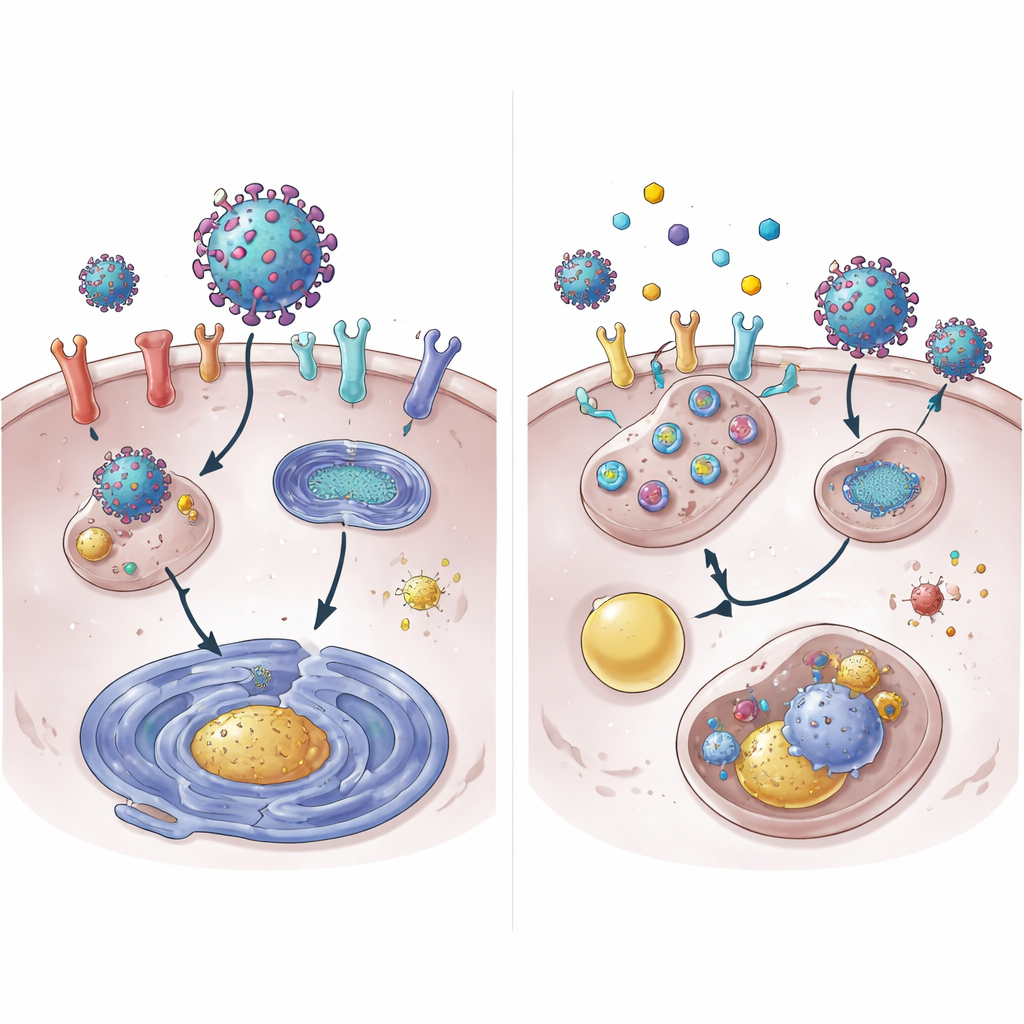
Mevsimsel Koronavirüsler ve XPO1 Bağlantısı
Bilim insanları daha sonra genellikle hafif soğuk algınlıklarına yol açan ancak bağışıklığı zayıf kişilerde tehlikeli olabilen hCoV-229E adlı mevsimsel koronavirüse yöneldi. Çoğaldıklarında parlayan mühendislik ürünü virüsleri kullanarak, dört bileşiğin de NRF2 olmasa bile akciğer ve kan damarı hücrelerinde 229E’yi güçlü şekilde bastırdığını gösterdiler. SARS-CoV-2’nin aksine, bu virüs farklı bir reseptör olan ANPEP’i kullanıyor ve ilaçlar ANPEP’i değiştirmedi. Bunun yerine etkileri, XPO1’i ne kadar güçlü azalttıklarıyla yakından ilişkiliydi. XPO1’in kendisini azaltmak 229E çoğalmasını keskin şekilde düşürdü ve selinexor’un etkisi bu XPO1 fakir hücrelerde neredeyse ortadan kayboldu. Bu sıralama—XPO1’e en çok bağımlı olan SEL, en az bağımlı olan BARD—her bileşiğin hedef karmasında küçük farklılıklar olduğunu ve XPO1’in antiviral etkilerinin merkezi bir düğümü olduğunu düşündürüyor.
Gelecekteki Tedaviler İçin Anlamı
Uzman olmayanlar için ana mesaj, koronavirüslerle mücadele etmenin sadece virüsü doğrudan saldırmakla sınırlı olmadığı, aynı zamanda hücrelerimizi kademeli olarak yeniden yapılandırarak onların enfekte olmasını daha zor hâle getirebileceğimizdir. Laboratuvarda yetiştirilmiş insan hücrelerinde incelenen bileşikler, SARS-CoV-2 ve yaygın bir soğuk algınlığı koronavirüsünün dayandığı hayati tutunma noktalarını ve yardımcı yolları ortadan kaldırdı ve bunu büyük ölçüde bunları ilk dikkat çekici kılan NRF2 yolundan bağımsız olarak gerçekleştirdi. Bu bulgular hâlâ preklinik aşamada olup doğrudan ilaçlara dönüşmemekle birlikte, viral girişi aynı anda azaltan, zararlı iltihabı hafifleten ve ACE2, TMPRSS2 ve XPO1 gibi paylaşılan konak protein ağlarını hedefleyerek dokuları koruyan ilaçlar için umut verici bir yol ortaya koyuyor.
Atıf: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Anahtar kelimeler: konak yönelimli antiviral ilaçlar, koronavirüs girişi, ACE2 ve TMPRSS2, NRF2 aktive edicileri, XPO1 inhibisyonu