Clear Sky Science · tr
Campylobacter jejuni’nin iki aşamalı aktin aracılı stratejisi, mitokondri kümelenmesini ve demir homeostazını teşvik ederek hücre içi hayatta kalma ve sürekliliği sağlar
Hücre içindeki bu küçük savaş neden önemli
Az pişmiş tavuktan kaynaklanan gıda zehirlenmeleri sıklıkla Campylobacter jejuni adlı bir bakteriye atfedilir. Çoğu insan iyileşir, ancak bu mikrop birçok ortamda şaşırtıcı derecede iyi hayatta kalır ve bu da çiftlikten sofraya yayılmasını kolaylaştırır. Bu çalışma, bakterinin serbest yaşayan bir amebanın—yaygın bir tatlı su mikrobu—içine gizlendiğinde neler olduğunu inceliyor ve hücrenin iç iskeletini yeniden şekillendirme, enerji üreten “güç paketleri” olan mitokondrileri kümelendirme ve demir ile zararlı oksijen kimyasını kontrol etme etrafında dönen beklenmedik derecede sofistike bir hayatta kalma hilesini ortaya koyuyor. Yaşam döngüsünün bu gizli evresini anlamak, bakterinin insanlara ulaşmadan önce kontaminasyonu azaltmaya yönelik yeni yollar gösterebilir.
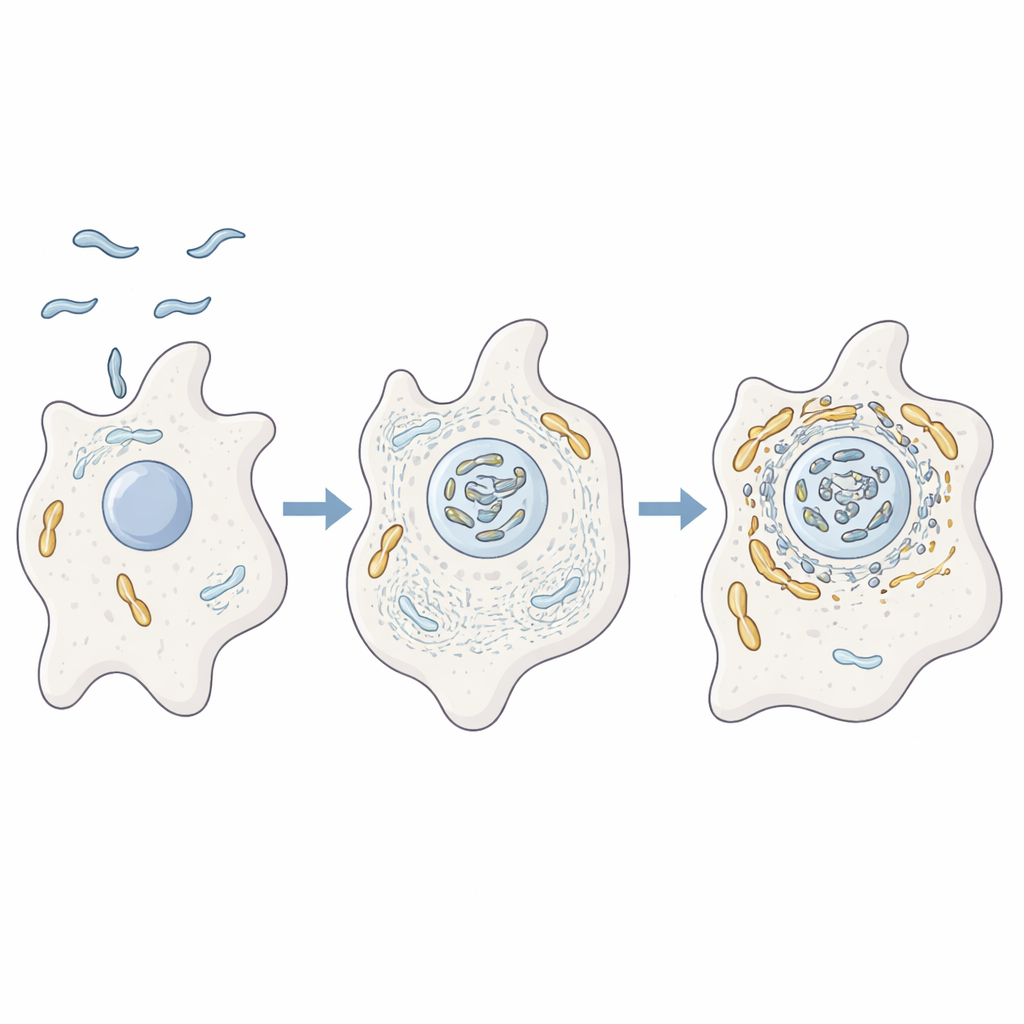
Amebalarda eğitim gören bir mikrop
Yazarlar, C. jejuninin toprak ve suda yaşayan tek hücreli organizma Acanthamoeba castellanii içindeki davranışını incelediler. Bu amebalar birçok hastalık yapıcı bakteri için eğitim alanı gibi davranır; zorlu koşullardan ve dezenfektanlardan koruma sağlarlar. Gelişmiş protein analizi, mikroskopi ve genetik mutantlar kullanarak araştırmacılar, C. jejuni amebayı enfekte ettiğinde bakterinin konakçının mitokondrileriyle yakından ilişkili hale geldiğini gösterdiler. Aynı zamanda, aktinden oluşan ameban hücre içi iskeleti ile hücre şekil ve hareketini düzenleyen proteinler bu mitokondrilerin yakınında güçlü bir şekilde zenginleşmişti; bu da bakterinin konak hücrenin iç mimarisini aktif olarak yeniden düzenlediğini düşündürüyor.
Güç paketlerini hareket ettirmek için hücre iskeletini bükmek
Aktinin gerçekten bu etkileşimi yönlendirip yönlendirmediğini test etmek için ekip, aktinin filament oluşturmasını veya ağlar halinde dallanmasını engelledi. Bu koşullarda, mitokondriler artık bakterilerin yakınında toplanmadı ve yerine dağınık noktalar halinde kaldı; bakterinin hayatta kalması düştü. Daha sonra, bakterinin kamçı benzeri kuyruğu aracılığıyla konak hücrelere enjekte edilen iki bakteri yardımcı proteini CiaD ve CiaI üzerine odaklandılar. CiaD, aktin büyümesini artırdı ve ameba yüzeyinde sivri projeksiyonları teşvik ederek hücrenin bakteriyi içeri almasına yardımcı oldu. İçeri girdikten sonra, mitokondrilerin aktin bağımlı bir şekilde bakteriyi içeren bölmenin etrafında kümelendikleri görüldü ve böylece bakteri konak enerji makinelerince zengin ayrıcalıklı bir bölgeye yerleşmiş oldu.
Mitokondrileri yeniden şekillendiren moleküler bir anahtar
CiaD giriş için anahtar olurken, CiaI sonrasında olanları kontrol ediyor. Araştırmacılar CiaI genini sildiklerinde, C. jejuni artık güçlü mitokondri kümelenmesi tetiklemedi ve amebalar içinde zayıf hayatta kaldı. Canlı bakteri olmadan, saflaştırılmış CiaI’in küçük boncuklara bağlanmış biçiminin uygulanması bile yakın mitokondrilerde füzyon ve kümelenmeye yol açmaya ve yerel olarak aktini gidermeye yeterliydi. Biyokimyasal testler, CiaI’in enerji taşıyan moleküllere işbirlikçi bir şekilde bağlandığını gösterdi; bu da konak içindeki koşullara bağlı olarak aktivitesini açıp kapatabilen moleküler bir anahtar gibi davrandığını düşündürüyor. Yazarlar, CiaD tarafından yönlendirilen aktin büyümesi mitokondrileri yaklaştırdıktan sonra CiaI’in yerel aktin yıkımını tetikleyip mitokondri ağını bakteriyi içeren bölmenin etrafında yoğun kümelere dönüştürdüğünü öneriyorlar.
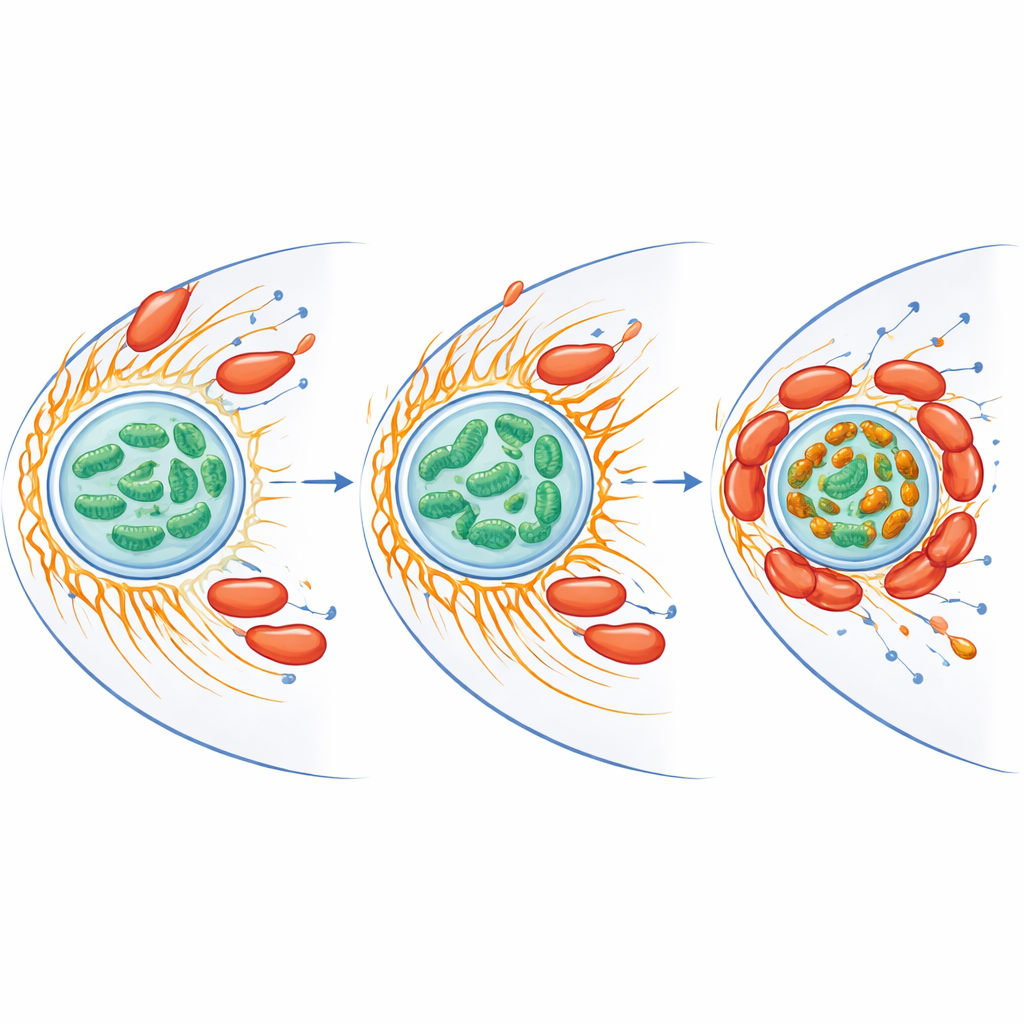
Konak hücre içinde demir ve stresin yeniden kablolanması
Mitokondriler sadece enerji üretmez—aynı zamanda demiri işler ve mikropları öldürebilecek reaktif oksijen türleri üretebilirler. Araştırmacılar, enfeksiyonun mitokondriler içindeki serbest demiri genel olarak azalttığını, ancak aynı zamanda mitokondrilerin bakterilerin etrafında kümelendiği parlak demir bakımından zengin kümeler oluşturduğunu buldular. Demir yönetimi ve oksidatif strese karşı savunmada görevli proteinler hem konakta hem de bakteride arttı. Ekip serbest demiri bir şelatlayıcı bileşikle uzaklaştırdığında, amebanın reaktif oksijen türleri patlaması düştü ve C. jejuninin hayatta kalması dramatik şekilde arttı. Enfekte hücrelerdeki mitokondriler ayrıca yükselmiş bir membran potansiyeli gösterdi; bu, artmış aktivitenin bir işareti olup bakterinin konak gücünü kendi sürekliliği lehine ayarladığını ve zarar verici oksijen kimyasını sınırladığını düşündürüyor.
Gıda güvenliği ve enfeksiyon için bunun anlamı
Bir araya getirildiğinde, sonuçlar iki aşamalı bir stratejiyi destekliyor: önce CiaD aktin büyümesini uyararak bakterinin amebalara girmesine ve mitokondrileri giriş noktasına çekmesine yardımcı olur; ikinci olarak CiaI yerel olarak aktini parçalar ve mitokondrileri bakteriyi içeren bölmenin etrafında demir bakımından zengin kümelere dönüştürürken konağın oksidatif savunmalarını köreltir. Hücre şekli, enerji kullanımı ve metal dengesinin bu ince ayarlı kontrolü C. jejuninin amebalar içinde hayatta kalmasına yardımcı olur ve muhtemelen çevrede kalma yeteneğine ve daha sonra insanları enfekte etme kapasitesine katkıda bulunur. Bu mikroskobik çekişmedeki kilit oyuncuları ortaya koyarak çalışma, Cia proteinleri, aktin‑mitokondri temasları veya demir işleme yolları gibi, kontaminasyonu ve hastalığı azaltmak için bozulabilecek yeni hedeflere işaret ediyor.
Atıf: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Anahtar kelimeler: Campylobacter, amebalar, mitokondriler, aktin sitoskeleti, demir homeostazı