Clear Sky Science · tr
Bağımlılık yapıcı ilaç kötüye kullanımı ve depresyon — epigenetiğe odaklanma
Bu araştırma günlük yaşam için neden önemlidir
Bağımlılık yapan ilaçlar ve depresyon genellikle ayrı sorunlar olarak ele alınır, oysa aynı kişide sıkça birlikte görülürler. Bu derleme, metamfetamin, kokain, opioidler ve esrar gibi ilaçların uzun süreli kullanımının beyinde kalıcı "moleküler izler" bırakabileceğini ve bunun depresyon riskini artırdığını açıklıyor. Bu gizli değişiklikleri açığa çıkararak, makale kimin daha savunmasız olduğunu önceden haber verebilecek testlere ve yalnızca semptomları örtmek yerine hasarı tersine çevirebilecek daha hassas tedavilere işaret ediyor.
Bağımlılık ve düşük ruh hâli nasıl iç içe geçer
Yazarlar, ilaç kötüye kullanımı ile depresyon arasındaki yakın klinik bağı özetleyerek başlıyor. Tekrarlayan şekilde bağımlılık yapıcı maddeler kullanan kişiler, daha kalıcı üzüntü, zevk kaybı, uyku sorunları ve intihar düşüncelerini bildirme olasılığı çok daha yüksektir. Ödül, motivasyon, hafıza ve karar verme süreçlerini kontrol eden ventral tegmental alan, nucleus accumbens, prefrontal korteks ve hipokampus gibi beyin bölgeleri her iki durum için de merkezi öneme sahiptir. Kronik ilaç maruziyeti dopamin ve serotonin gibi beyin kimyasallarını, hipotalamo-hipofiz-adrenal eksen tarafından kontrol edilen stres hormonlarını, bağışıklık sinyallerini ve nöronların enerji tedarikini bozuyor. Bu değişiklikler bir araya gelerek beyni strese karşı daha az dayanıklı ve depresif durumlara daha yatkın hâle getiriyor; üstelik bu etkiler son dozdan uzun süre sonra da devam edebiliyor.
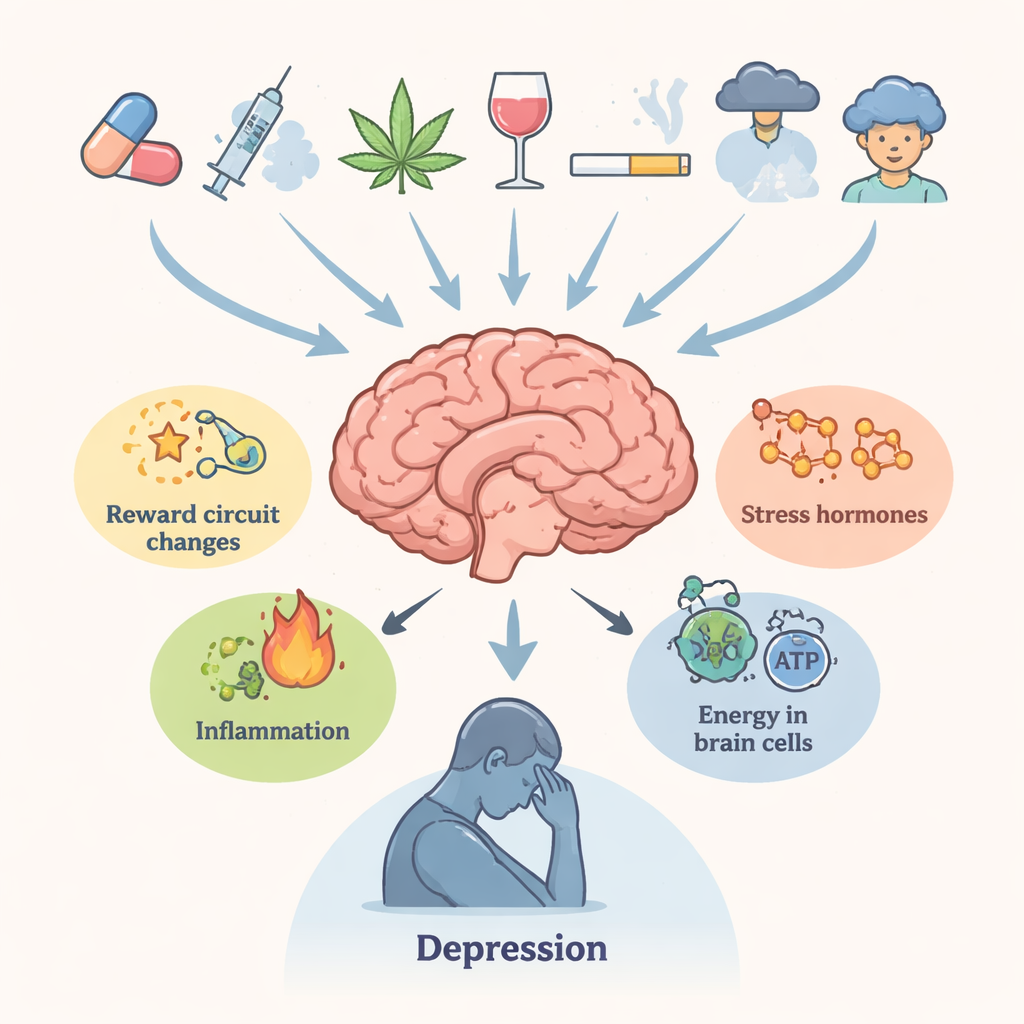
Beyninin kimyasını yeniden şekillendiren ilaçlar
Derleme birkaç ana ilaç sınıfını inceliyor. Amfetamin tipi uyarıcılar ve sentetik "banyo tuzları" da dahil yakın akrabaları, güçlü dopamin ve diğer ileticilerin ani yükselmelerine neden olur; zamanla bu durum sinir uçlarına zarar verir, glutamat dengesini bozar, endoplazmik retikulum üzerinde yük oluşturur ve hücreleri zararlı otofajiye yönlendirebilir. Ergenlikte esrar kullanımı, uzun süreli olarak kanabinoid reseptörlerinde, ak beyazı yapısında ve dopamin devrelerinin hassasiyetinde meydana gelen değişiklikler yoluyla ileriki dönemde depresyon ve intihar riskiyle ilişkilidir. Opioidler ağrıyı hafifletirken iltihaplanma, mitokondriyal yetmezlik ve BDNF gibi büyümeyi destekleyen sinyallerin azalmasını tetikleyebilir. Kokain stres sistemini tekrar tekrar aktifleştirir ve FKBP5 gibi önemli düzenleyicileri değiştirerek yoksunluk sırasında anksiyete ve düşük ruh hâline katkıda bulunur. Her durumda biyolojik bozulmalar sürme eğilimindedir ve bu da duygusal belirtilerin açık zehirlenmeyi aşarak devam etmesini açıklamada yardımcı olur.
Epigenetik: maruziyetin hafızası
İlaç etkilerinin neden kalıcı olduğunu anlamak için yazarlar epigenetiğe—DNA dizisini değiştirmeden gen aktivitesini ayarlayan kimyasal etiketler ve moleküler anahtarlara—odaklanıyor. Bağımlılık yapan ilaçlar DNA metilasyonunu (sitozin bazları üzerindeki bir işaret) değiştirir, DNA’yı paketleyen histon proteinleri üzerindeki kimyasal grupları değiştirir ve hangi proteinlerin üretileceğini ince ayar yapan kodlamayan RNA’ları etkiler. Örneğin metamfetamin ve kokain, ödülle ilgili beyin bölgelerinde metilasyon örüntülerini kaydırarak bu işaretleri ekleyen veya çıkaran enzimlerin düzeylerini değiştirir. Opioidler ve uyarıcılar, glutamat reseptörlerini, stres sinyalleşmesini ve sinaptik yapıyı kontrol eden genlerde histon asetilasyonu ve metilasyonunu yeniden düzenler. Onlarca mikroRNA, uzun kodlamayan RNA ve dairesel RNA, ilaç maruziyetiyle birlikte artar veya azalır; bunlar topluca iltihaplanma, nöron büyümesi ve sinapsların gücünü etkiler. Bu epigenetik değişiklikler ilaç geçmişinin moleküler bir "hafızası" gibi davranır.
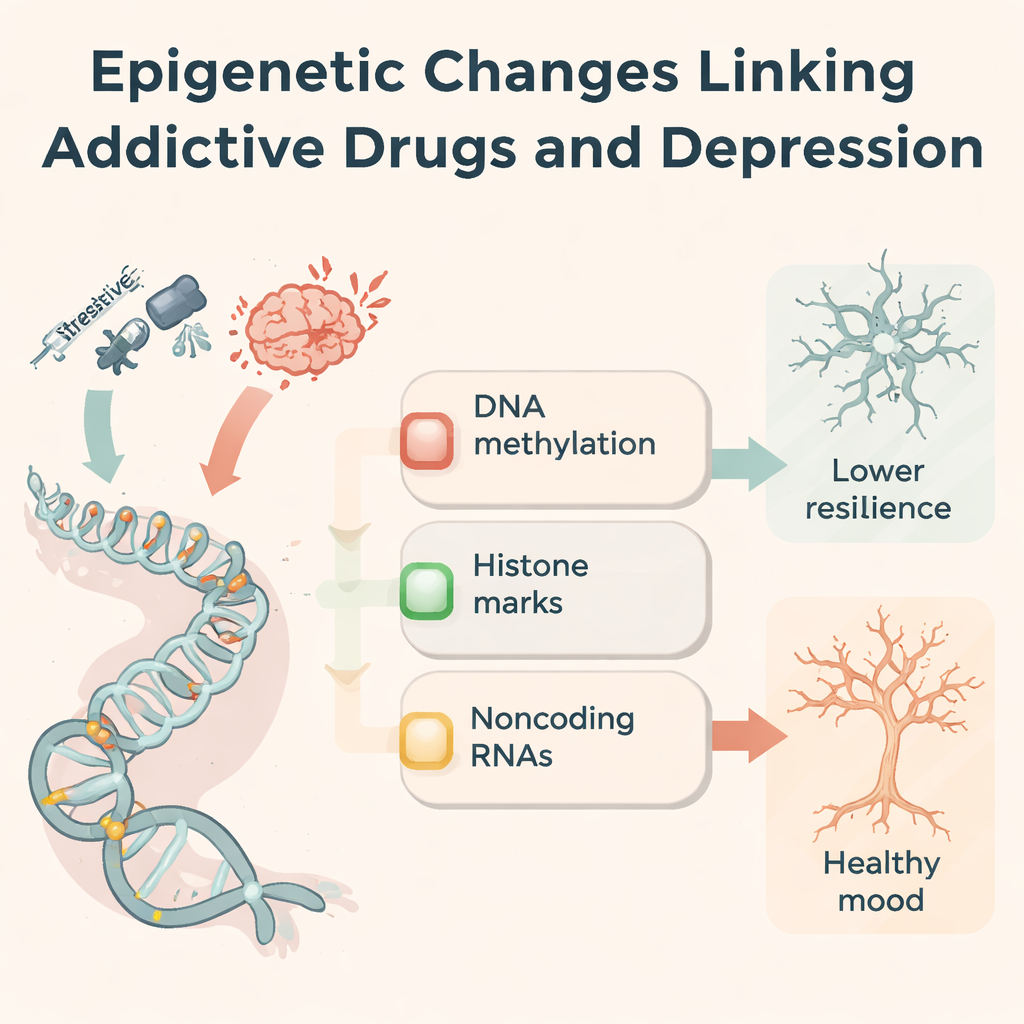
Depresyon ve bağımlılıkta paylaşılan moleküler yollar
Aynı epigenetik mekanizmalar, ilaç kullanmamış insanlar ve hayvanlarda görülen depresyonda da ortaya çıkıyor. Stresli deneyimler stres hormonu reseptörlerinin (NR3C1 ve FKBP5 gibi) metilasyonunu değiştirebilir, BDNF gibi yararlı büyüme faktörlerini azaltabilir ve bağışıklık ile glutamat yollarını yeniden kablolayabilir. İlaçlarla değişen pek çok kodlamayan RNA, depresyonda da yanlış düzenlenmiş olup yeni nöronların doğumunu, mikroglianın iltihaba yanıtını ve sinapsların bağlanma gücünü etkiler. Yazarlar üç parçalı bir çerçeve öneriyor: stres yanıtı düzenlemesi, ödül devresi yeniden şekillenmesi ve sinaptik plastisite. Bu eksenler boyunca bağımlılık ve depresyon, küçük bir gen ve işaret kümesi üzerinde tekrar tekrar birleşiyor; bu da iki bozukluğun sık birlikte görülmesine biyolojik bir gerekçe sunuyor.
Gelecekte korunma ve tedavi için anlamı
Kapanışta derleme, epigenetik değişikliklerin erken uyarı biyobelirteçleri ve gelecek nesil tedaviler için hedefler haline gelebileceğini savunuyor. Epigenetik işaretleri silen geniş etkili ilaçlar hayvanlarda bazı antidepresan benzeri etkiler göstermiş olsa da, rutin insan kullanımı için çok kaba müdahaleler. CRISPR tabanlı epigenom editörleri ve belirli mikroRNA’ları veya uzun RNA’ları düzenleyen terapiler gibi yeni araçlar bir gün belirli beyin hücrelerindeki problemli genleri diğerlerinden koruyarak ayarlayabilir. Yazarlar mevcut verilerin çoğunun kemirgenlerden ve karışık beyin dokusundan geldiği; insan biyolojisinin daha karmaşık olduğu konusunda uyarıda bulunuyor. Yine de, bağımlılık yapan ilaçların ve depresyonun aynı moleküler "not defterine" nasıl yazdığını ortaya koyarak, bu çalışma daha kişiselleştirilmiş ve kalıcı tedavilere doğru umut verici bir yol sunuyor.
Atıf: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Anahtar kelimeler: bağımlılık ve depresyon, epigenetik, ilaç kötüye kullanımı, DNA metilasyonu, kodlamayan RNA