Clear Sky Science · tr
Plexiform nörofibrom ksenograft fare modellerinde NF1 gen tedavisinin ilke kanıtı
Bu araştırma neden önemli
Genetik bir durum olan nörofibromatozis tip 1 (NF1) olan kişiler genellikle plexiform nörofibrom adı verilen büyük, biçim bozukluğu yaratan sinir tümörleri geliştirirler. Bu büyümeler ağrıya, hareket sorunlarına ve ciddi kozmetik kaygılara yol açabilir; oysa mevcut tedaviler sınırlıdır ve cerrahi genellikle mümkün değildir. NF1 tek bir gendeki değişikliklerden kaynaklandığından, birçok araştırmacı gen tedavisinin—bozuk geni düzeltme veya değiştirme—bir gün bu tümörleri küçültebileceği veya ortadan kaldırabileceği umudunu taşıdı. Bu çalışma, farelerde bu fikri erken ama güçlü bir testle sorguluyor; basit ama önemli bir soruyu yanıtlıyor: yerleşmiş tümörlerde eksik NF1 genini geri getirirseniz, tümörler kaybolur mu?
Farelerde gerçekçi bir tümör modeli kurmak
Araştırmacıların önce insan plexiform nörofibromlarını yakından taklit eden bir laboratuvar sistemine ihtiyacı vardı. Normalde sinirleri çevreleyen destek hücreleri olan insan Schwann hücrelerini, NF1 geninin her iki işleyen kopyasını kaybetmiş bir hastadan aldılar. Bu hücreler bağışıklığı baskılanmış farelerde yaralanmış siyatik sinirlerin yanına yerleştirildi. Haftalar içinde sinirler tutarlı şekilde kalınlaşmış, yoğun hücreli doku ve düzensiz yapı ile yoğun kollajen bantları geliştirdi—plexiform nörofibromların ayırt edici özellikleri. Bu NF1 eksik hücreler olmadan yapılan kontrol cerrahileri veya yalnızca tek bir bozuk NF1 kopyasına sahip hücrelerle tümörler güvenilir biçimde oluşmadı. Bu, NF1 kaybı tam olan insan hücrelerinin tümör büyümesini yönlendirdiğini ve hastalığın güçlü, hızlı bir modelini oluşturduğunu gösterdi.
Tümör hücrelerinde NF1’i yeniden açmak
Bu model hazır olduğunda ekip, tümör oluşturan Schwann hücrelerini farelerden alınan anahtar kontrollü bir NF1 genini taşıyacak şekilde mühendislik yaptı. Anahtar yaygın olarak kullanılan antibiyotik doksisikline yanıt veriyordu: fareler doksisiklin içeren su içtiğinde, eklenen NF1 geni implante hücrelerde aktive oluyordu. Farelere önce tümör geliştirmeleri için zaman tanındı ve ancak sonra gen açıldı. Sonuçlar çarpıcıydı. NF1 kapalı kalan hayvanlarda, siyatik sinirlerin çoğunda hâlâ nörofibromlar vardı. Buna karşılık, NF1 yeniden aktive edildiğinde, çoğu sinir mikroskop altında normal göründü ve aşırı aktif büyüme sinyalizasyonunun kimyasal belirteçleri büyük ölçüde azaldı. Özetle, NF1’i yeniden açmak tümör dokusunu sağlıklı bir sinir durumuna geri itiyordu.
NF1 kaybını ikinci bir yolla tersine çevirmek
Bu etkinin tek bir mühendislik numarasıyla sınırlı olmadığını göstermek için bilim insanları ikinci, tamamlayıcı bir model kurdu. Bu kez, başlangıç olarak yalnızca bir hasarlı NF1 kopyasına sahip olan—NF1’li kişilerin tüm hücrelerinde kalıtsal olarak taşıdığı duruma benzeyen—insan Schwann hücreleri kullanıldı. Doksisiklin varlığında kalan NF1 aktivitesini geçici olarak daha da azaltabilecek bir genetik anahtar eklendi. Fareler doksisiklin içtiğinde NF1 seviyeleri daha da düştü ve tümörler kolayca oluştu. Kritik olarak, tümörler geliştikten sonra doksisiklin çıkarıldığında NF1 seviyeleri yeniden yükseldi ve birçok sinir normal yapıya geri döndü. Tekrardan, normalleşen sinirlerde büyümeyle ilişkili sinyalizasyon ölçümleri azaldı. Bu iki zıt anahtarlama stratejisi—NF1’i açmak veya onun baskısını kaldırmak—aynı sonuca işaret ediyor: tümör hücrelerinde NF1’in geri kazandırılması yerleşmiş hastalığı geri alabiliyor.
Daha gerçekçi bir iletim yaklaşımını test etmek
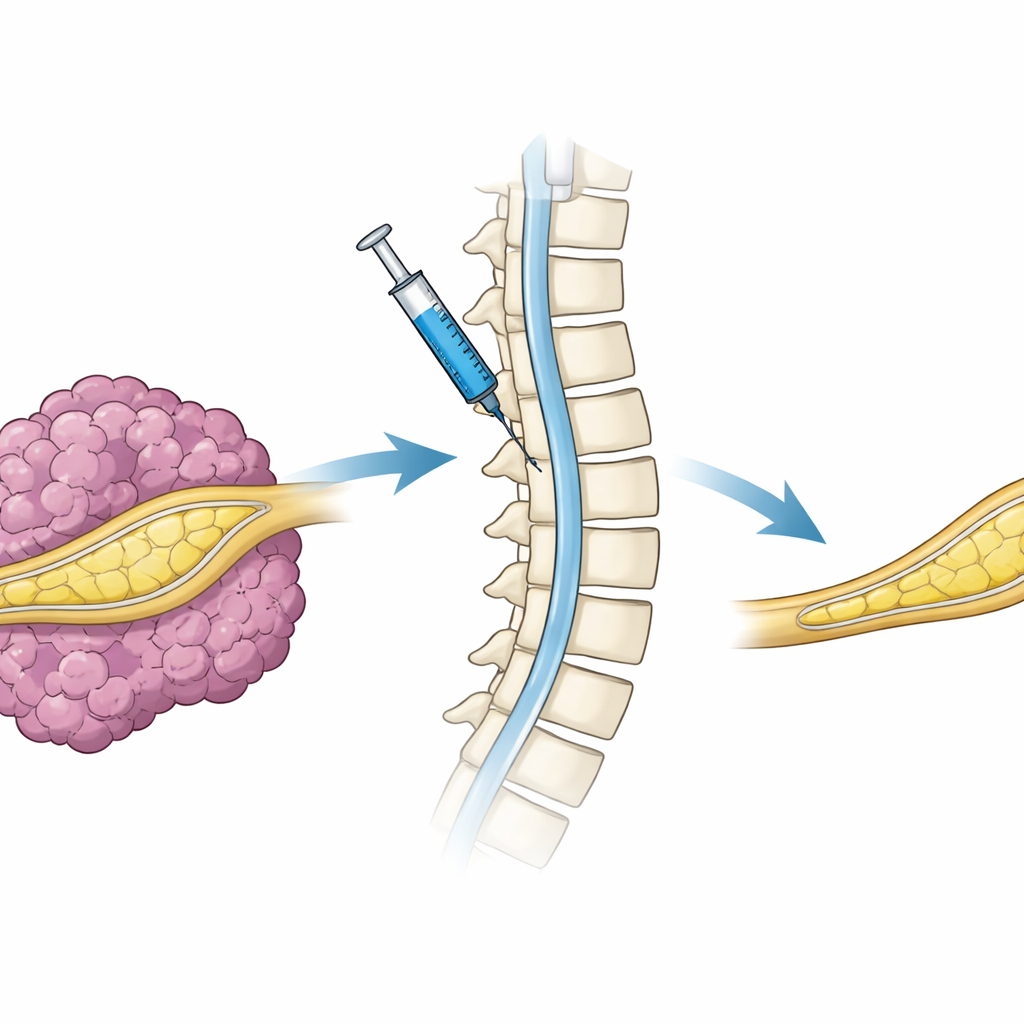
Laboratuvarda hücrelere yerleştirilmiş genetik anahtarların ötesinde, gerçek bir tedavi yaşayan bir hastanın sinir sistemine çalışan bir NF1 genini iletmek zorunda olacaktır. Bu adımı araştırmak için, araştırmacılar tam NF1 genini bir lentiviral vektöre paketleyip tümör taşıyan farelerin omurilik çevresindeki sıvı boşluğuna—intratekal iletim olarak bilinen yolla—injekte ettiler. Hayvanlar daha sonra iletilen genin açılması için doksisiklin aldı. Kontrol virüsü verilen farelerle karşılaştırıldığında, NF1 taşıyan virüsle tedavi edilenlerde anlamlı derecede daha az tümör gelişti ve sinir dokuları daha normal görünüyordu. Bu kısa, tek doz deney olmasına karşın, NF1 gen iletiminin omurilik sıvısı yoluyla periferik sinirlere ulaşabileceğini ve tümör yükünü anlamlı şekilde azaltabileceğini gösterdi.
Bu çalışma NF1’li kişiler için ne anlama geliyor
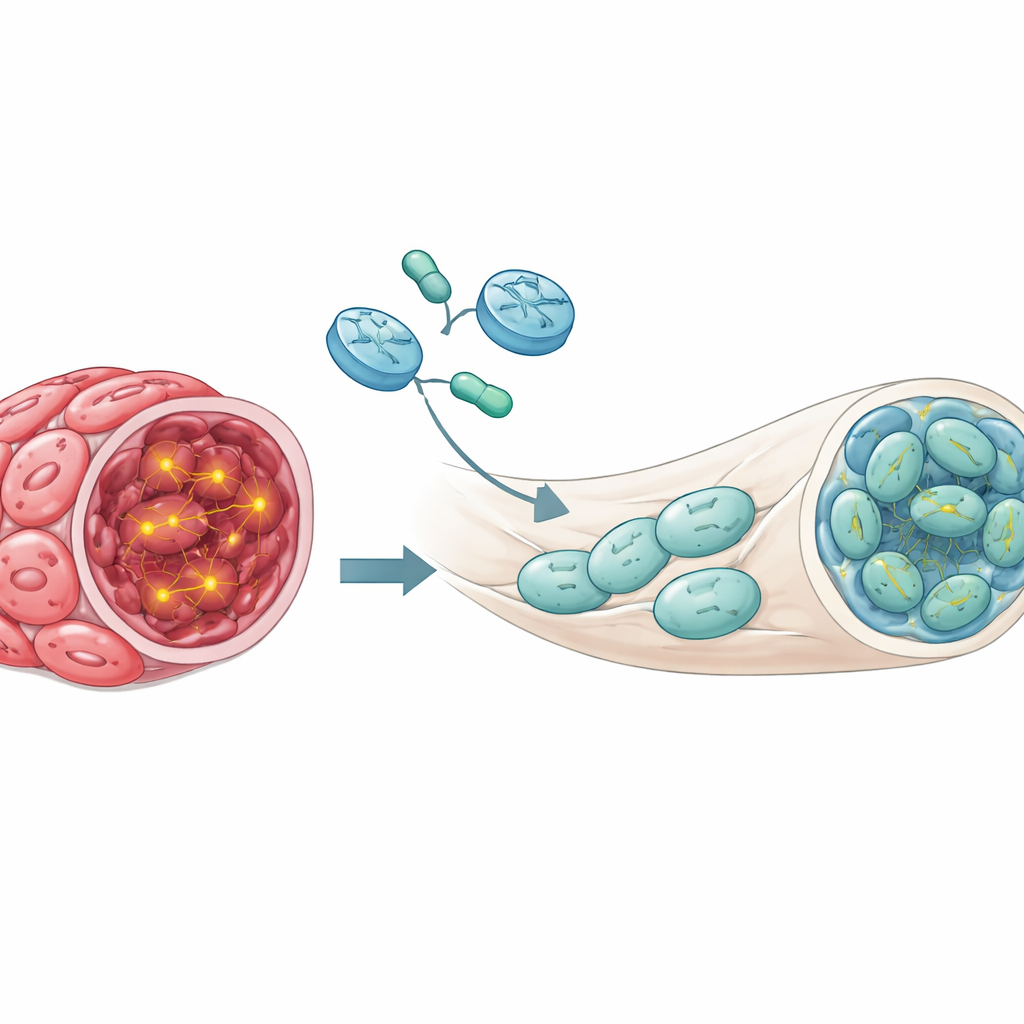
Bu çalışma henüz hastalar için hazır bir tedavi sunmuyor, ancak önemli bir soruyu yanıtlıyor: insan plexiform nörofibromlarına yakından benzeyen dikkatle tasarlanmış fare modellerinde, tümör hücrelerinde NF1’in geri kazandırılması yerleşmiş tümörleri küçültebilir veya normalleştirebilir. Çalışma, NF1 gen tedavisinin yalnızca teorik bir umut değil, ilke olarak uygulanabilir bir strateji olduğunu kanıtlıyor. Birçok zorluk devam ediyor—en güvenli ve en verimli iletim araçlarını bulmak, ne kadar NF1 aktivitesinin yeterli olduğunu belirlemek ve daha doğal modellerde uzun vadeli etkileri test etmek gibi. Yine de bu sonuçlar, NF1 ile yaşayan kişilerde plexiform nörofibromlardan kalıcı rahatlama sağlayabilecek gelecekteki gen tabanlı tedaviler için bilimsel bir temel oluşturuyor.
Atıf: Hewa Bostanthirige, D., Plante, C., Caron, M. et al. Proof-of-principle of NF1 gene therapy in plexiform neurofibroma xenograft mouse models. Commun Biol 9, 419 (2026). https://doi.org/10.1038/s42003-026-09695-8
Anahtar kelimeler: nörofibromatozis tip 1, gen tedavisi, plexiform nörofibrom, Schwann hücreleri, lentiviral iletim