Clear Sky Science · tr
FLVCR1 İlişkili Duyu Nöropatisinin Altında Yatan Mitokondriyal Enerji Yetmezliği
Ağrı Sinirleri Güçten Düştüğünde
Bazı insanlar neredeyse ağrı hissetmeyecek şekilde doğar. İlk bakışta bu bir nimet gibi görünse de hızla bir lanete dönüşür: ağrı bir uyarı sinyali olmadığında yanıklar, kırıklar, enfeksiyonlar ve hatta körlük birikir. Bu çalışma, böyle ağrı kaybı bozukluklarından nadir bir formu inceliyor ve şaşırtıcı bir suçlu ortaya çıkarıyor: sinir hücreleri içindeki küçük enerji santralleri—mitokondriler—enerji üretimlerinde ciddi şekilde aksıyor.
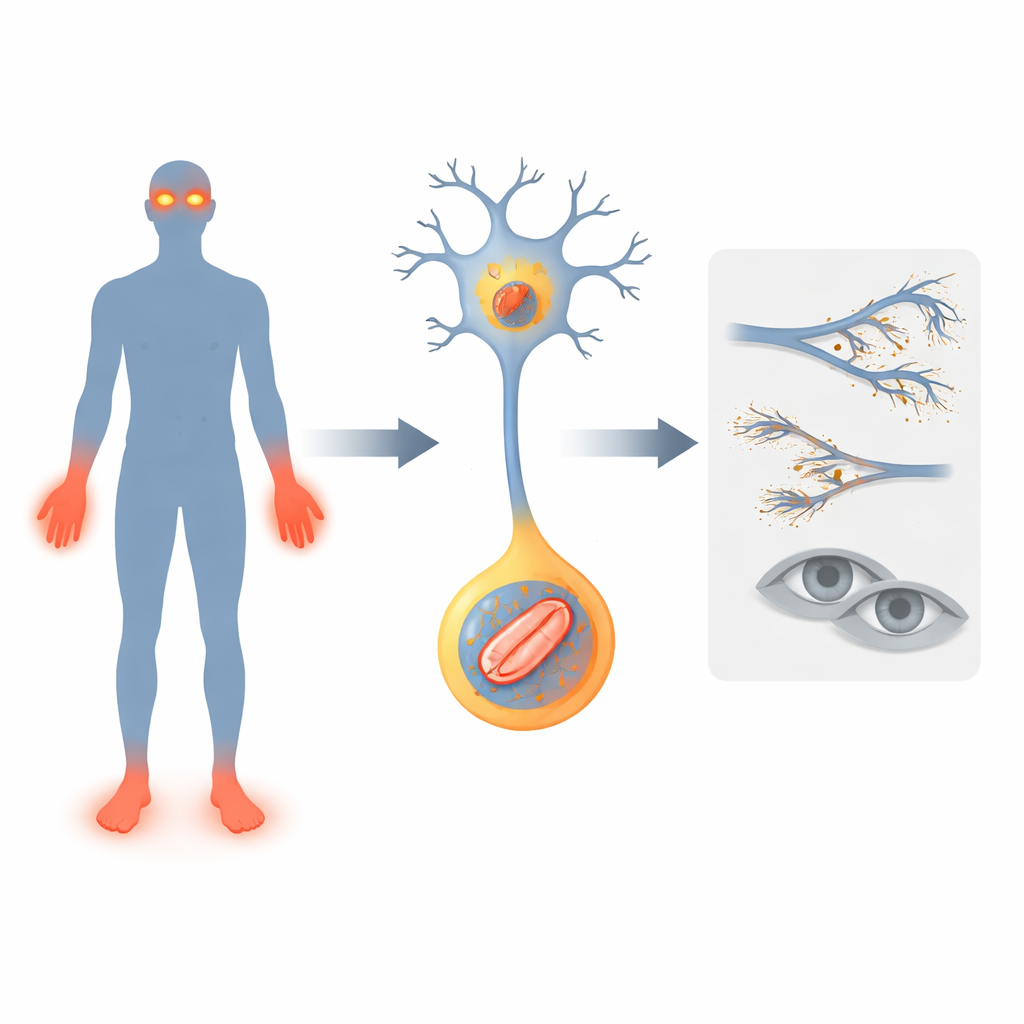
Alarm Zillerini Susturan Bir Gen
Araştırmacılar, daha önce ağrı duyusunu kaybetmeyle, dengesiz yürümeyle ve bazen ilerleyici görme kaybıyla ilişkilendirilen FLVCR1 adlı bir gene odaklanıyor. İki yeni hastada FLVCR1 değişikliklerini tanımlıyorlar. Her iki çocuk da erken dönemde sorunlar gösterdi: motor gelişim gecikmesi, sık düşmeler, derin enfeksiyonlar ve yaralanmalar fark edilmediği için parmak ve ayak parmaklarında sakatlanma. Birinde gece körlüğüne yol açan retinitis pigmentosa adı verilen dejeneratif bir göz hastalığı da gelişti. Bu olgular, FLVCR1 kusurlarının insanlarda nasıl ortaya çıkabileceğine dair tabloyu genişletiyor ve bu genin ağrı algılayan sinirleri ile retinadaki ışık algılayıcı hücreleri canlı tutmak için hayati olduğunu destekliyor.
Küçük Balıklarda Hastalığı Modellemede
FLVCR1’in gelişen duyu sinirlerini nasıl etkilediğini keşfetmek için ekip, şeffaf embriyoları sayesinde sinir hücrelerinin doğrudan gözlemlenebildiği zebrafish’e (zebra balığı) yöneldi. Genetik araçlarla balığın gen versiyonu olan flvcr1a’nın düzeylerini azalttılar. flvcr1a düzeyi düşürülen balıklarda omurga boyunca dokunma ve ağrıyı algılayan dorsal kök gangliyonlarının daha az olduğu görüldü. Davranış açısından bu balıklar kendi kendine daha az hareket ediyor ve kuyrukları hafifçe dokunulduğunda sadece kısa mesafeler yüzüyordu; bu, duyusal yanıtın azaldığını düşündürüyor. Daha önceki fare modelleri duyusal sinirleri analiz etmek için çok erken öldüğü için, bu zebrafish modeli FLVCR1 ilişkili sinir kusurlarının ve davranışın ayrıntılı şekilde takip edilebildiği ilk canlı sistemleri sunuyor.
Üç Sorun Yoldaşı Hücre Enerji Santrallerine Yöneliyor
FLVCR1 hücre zarında bulunur ve birkaç ana maddeyi yönetir. Önceki çalışmalar, kolin (zar lipitlerinin yapı taşı), hem (birçok enzimi çalıştıran demir içeren pigment) ve hücre bölümleri arasındaki kalsiyum akışını düzenlemede rollerini öne sürmüştü. Bilim insanları farklı FLVCR1 mutasyonları taşıyan dört hastadan deri hücreleri (fibroblast) topladı ve bunları sağlıklı kişiler ile semptomsuz taşıyıcılarla karşılaştırdı. Hasta hücrelerinde daha düşük kolin düzeyleri ve daha akışkan hücre zarları bulundu; bu değişiklikler mitokondriler için gerekli hassas lipid ortamı bozabilir. Ayrıca mitokondriler içinde hem üretimi için kritik bir enzim olan ALAS1’in daha az aktif olduğu keşfedildi, oysa toplam hem içeriği neredeyse normal görünüyordu. Aynı zamanda endoplazmik retikulum ile mitokondri arasındaki fiziksel temas noktaları—kalsiyumun normalde mitokondriye aktığı yerler—daha kısa ve daha seyrekti ve mitokondriye kalsiyum girişi azalmıştı. Kolin kıtlığı, durgun hem üretimi ve zayıflamış kalsiyum aktarımı olmak üzere üç problem, mitokondriyal performansın bozulduğuna işaret ediyordu.
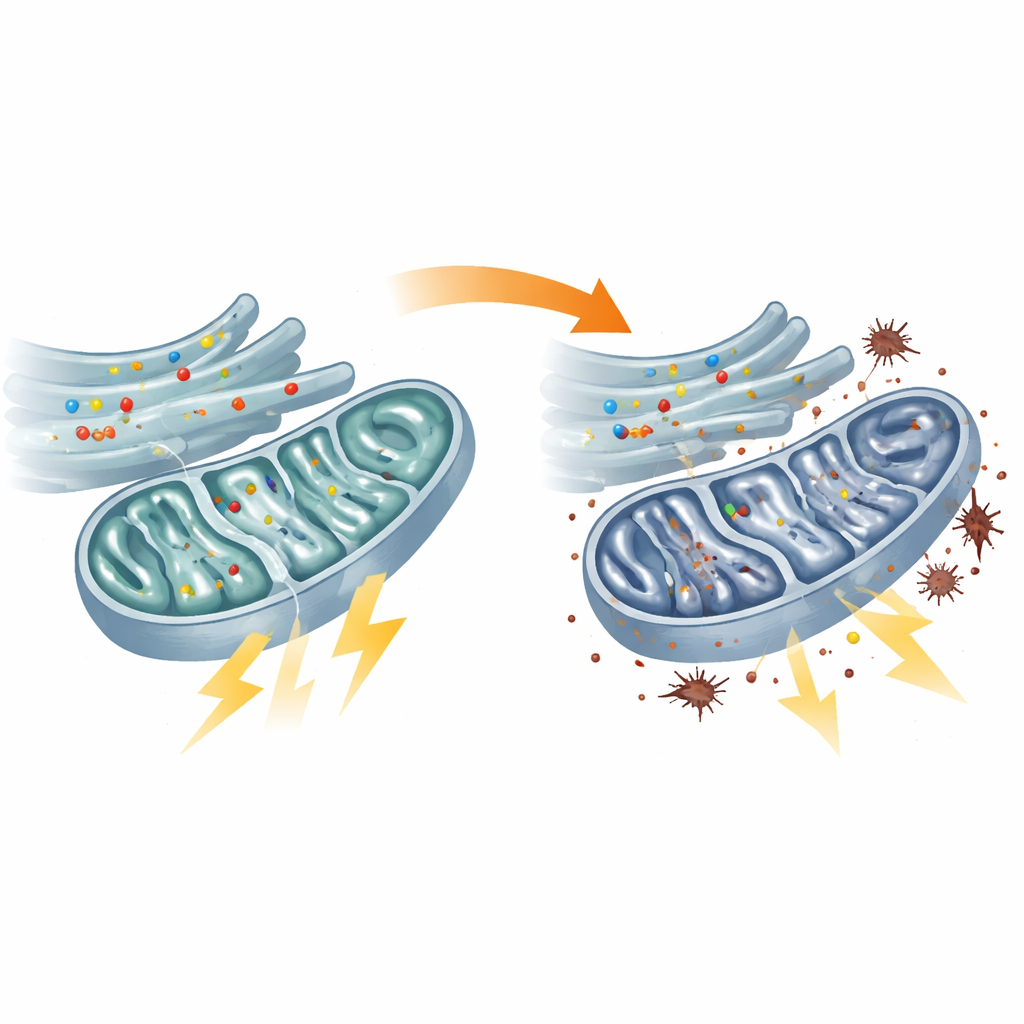
Aç Kalan Mitokondriler ve Fazla Yüklenen Yedek Sistemler
Enerji metabolizmasının doğrudan testleri, hasta fibroblastlarındaki mitokondrilerin düşük performans gösterdiğini doğruladı. TCA döngüsü olarak bilinen merkezi yakıt işleme merkezi daha yavaş çalışıyor, döngünün birkaç ana enzimi daha az aktifti ve yakıtı ATP’ye dönüştüren solunum zinciri zayıflamıştı. Sonuç olarak mitokondri içindeki ATP seviyeleri düştü. Hücreler, mitokondri dışındaki daha az verimli bir şeker yakma yolu olan glikolizi artırarak telafi etmeye çalıştı. Bu enerji stratejisi değişimi maliyetliydi: stres altındaki mitokondriyal makineleden elektron kaçışı oldu ve bunun sonucu olarak lipid peroksidasyonu adı verilen, hücre zarlarına yönelik oksidatif hasar arttı. Benzer kusurlar flvcr1a’sı azaltılmış zebrafish’te de görüldü ve mitokondriyal yetmezliği doğrudan duyu nöropatisi hayvan modeline bağladı.
Hücre Enerjisini Güçlendirerek Olası Tedavi İpuçları
Cesaret verici şekilde, bu kusurların bazıları laboratuvarda hafifletilebildi. Ekip, hasta hücrelerinde MCU adlı bir kanal proteinini fazla eksprese ederek mitokondriye kalsiyum girişini yapay olarak artırdığında enerji üretimi geri döndü ve oksidatif hasar işaretleri azaldı. Hücrelere hem öncüsü olan 5-aminolevülinik asit (ALA) sağlanması da TCA döngüsü aktivitesini, solunum zinciri fonksiyonunu ve ATP düzeylerini iyileştirdi; ancak önceki çalışmalarda uzun süreli ALA maruziyetinin zararlı olduğu gösterilmişti. Ek kolin, zar akışkanlığını normalize etti ve lipid hasarını azaltmaya yardımcı oldu, fakat enerji çıktısında yalnızca kısa vadeli, mütevazı iyileşmeler verdi. Bu kurtarma deneyleri, tek bir yolun yalnızca sorumlu olmadığını; bunun yerine kolin, hem ve kalsiyum yönetimindeki bozukluklar ağının mitokondrileri kronik düşük performansa zorladığını gösteriyor.
Bu Bulguların Hastalar İçin Önemi
FLVCR1 mutasyonlarının moleküllerden hücrelere ve tüm organizmalara kadar olan sonuçlarını izleyerek bu çalışma, mitokondrilerdeki enerji yetmezliğinin bu tür ağrı kaybı nöropatisinin ve ilişkili görme sorunlarının itici gücü olduğunu öne sürüyor. Duyu sinirleri ve fotoreseptörler, uzun aksonlarını korumak veya ışığa duyarlı yapıları sürekli yenilemek zorunda oldukları için olağandışı derecede enerji talep ederler; bu nedenle mitokondriyal çıktı düştüğünde özellikle savunmasızdırlar. Çalışmadaki zebrafish modeli ve hastalardan türetilen hücreler, şimdi mitokondriyal metabolizmayı güçlendirecek tedavilerin pratik test alanlarını sunuyor. Kolin takviyesi, kontrollü hem takviyesi veya mitokondriyal kalsiyum alımını artıran ilaçlar gibi yaklaşımlar hayvan modellerinde ve klinik denemelerde dikkatli değerlendirme gerektirse de temel mesaj açık: kırılgan nöronların enerji kaynağını yeniden sağlamak, doğanın en önemli uyarı sinyali olan ağrıdan yoksun doğan insanları bir gün korumaya yardımcı olabilir.
Atıf: Bertino, F., Zanin Venturini, D.I., Grasso, E. et al. Mitochondrial energetic failure underlies FLVCR1-related sensory neuropathy. Commun Biol 9, 429 (2026). https://doi.org/10.1038/s42003-026-09691-y
Anahtar kelimeler: duyu nöropatisi, mitokondriyal disfonksiyon, FLVCR1, ağrı hissizliği, sinir enerji metabolizması