Clear Sky Science · tr
SARS-CoV-2 ve yarasa SARS2-benzeri koronavirüslerinin yarasa reseptörünü tanıma yapısal temeli
Bu yarasa–virüs hikâyesi neden hâlâ önemli
COVID-19 pandemisi altı yıldan fazla önce başladı, ancak hastalığa yol açan virüs SARS-CoV-2’nin insanlara bu kadar iyi bulaşacak biçimde nasıl evrildiğini bilim insanları hâlâ ayrıntılı biçimde bir araya getiriyor. Temel bir muamma, bu virüs ile yarasalarda bulunan yakın akrabalarının hücre yüzeyindeki ACE2 adlı bir proteine nasıl tutunduğu—enfeksiyon için ilk ve kritik adım—oluyor. Bu mikroskobik kilit-ve-anahtar etkileşimlerini anlamak, virüsün nereden geldiğini, nasıl uyum sağladığını ve benzer virüsler gelecekte insanlara geçtiğinde neler olabileceğini aydınlatabilir. 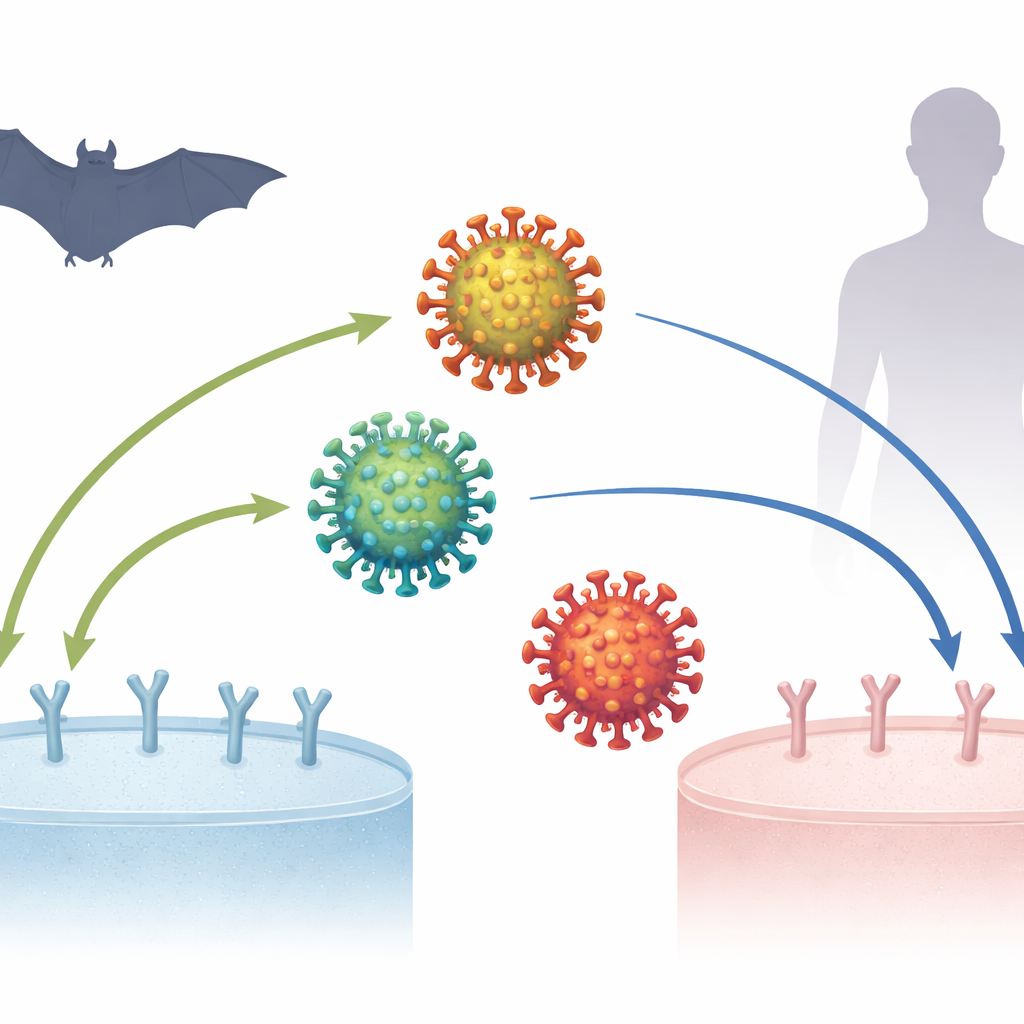
Viral tokalaşmaya bakmak
Çalışma, ACE2’yi kavrayan virüs yüzeyindeki taç benzeri yapı olan spike proteinine odaklanıyor. Spike’in küçük bir bölgesi, reseptör bağlanma domaini (RBD), ACE2 “kapı kolunu” kavrayan bir parmak ucu gibi davranır. Önceki çalışmalar, koronavirüsler türler arasında atladığında—örneğin yarasalardan sivete sonra insanlara—RBD’nin genellikle yeni konakta ACE2’ye tutunmayı geliştiren mutasyonlar edindiğini gösterdi. Ancak SARS-CoV-2 bir bilmece sundu: orijinal formu, uyum için çok zaman geçmeden önce bile insan ACE2’sine olağanüstü iyi bağlanıyordu ve SARS-CoV-2 ile ilişkili bazı yarasa virüsleri insan ACE2’sine yarasa ACE2’sinden daha iyi bağlanıyor gibi görünüyordu. Bu durum bazılarını, SARS-CoV-2’nin olağan evrimsel kurallara bir istisna olup olmadığı konusunda düşündürdü.
Yarasa ve insan reseptörlerini teste sokmak
Bu gizemi araştırmak için araştırmacılar, SARS-CoV-2’ye yakın iki yarasa koronavirüsü olan BANAL-52 ve BANAL-236’yı incelediler. Bu virüslerin ve SARS-CoV-2’nin RBD’lerinin insan ve birkaç yarasa türünden ACE2’ye ne kadar güçlü bağlandığını karşılaştırdılar. Hücre tabanlı bağlanma testleri, yüksek hassasiyetli biyosensör ölçümleri ve zararsız “psödovirüs” enfeksiyon testleri kullanarak açık bir desen buldular. BANAL-52’nin RBD’si en güçlü biçimde bir yarasa türü olan Rhinolophus sinicus’un ACE2’sine bağlandı ve insan ACE2’sine biraz daha zayıf bağlandı. Buna karşılık SARS-CoV-2’nin RBD’si insan ACE2’sini yarasa ACE2’sine göre mütevazı bir tercih gösterdi. Genel olarak, BANAL-52’nin RBD’si hem yarasa hem de insan reseptörlerini SARS-CoV-2’den daha sıkı kavradı, ancak en iyi ayarlandığı hedef o özgül yarasa ACE2’siydi. 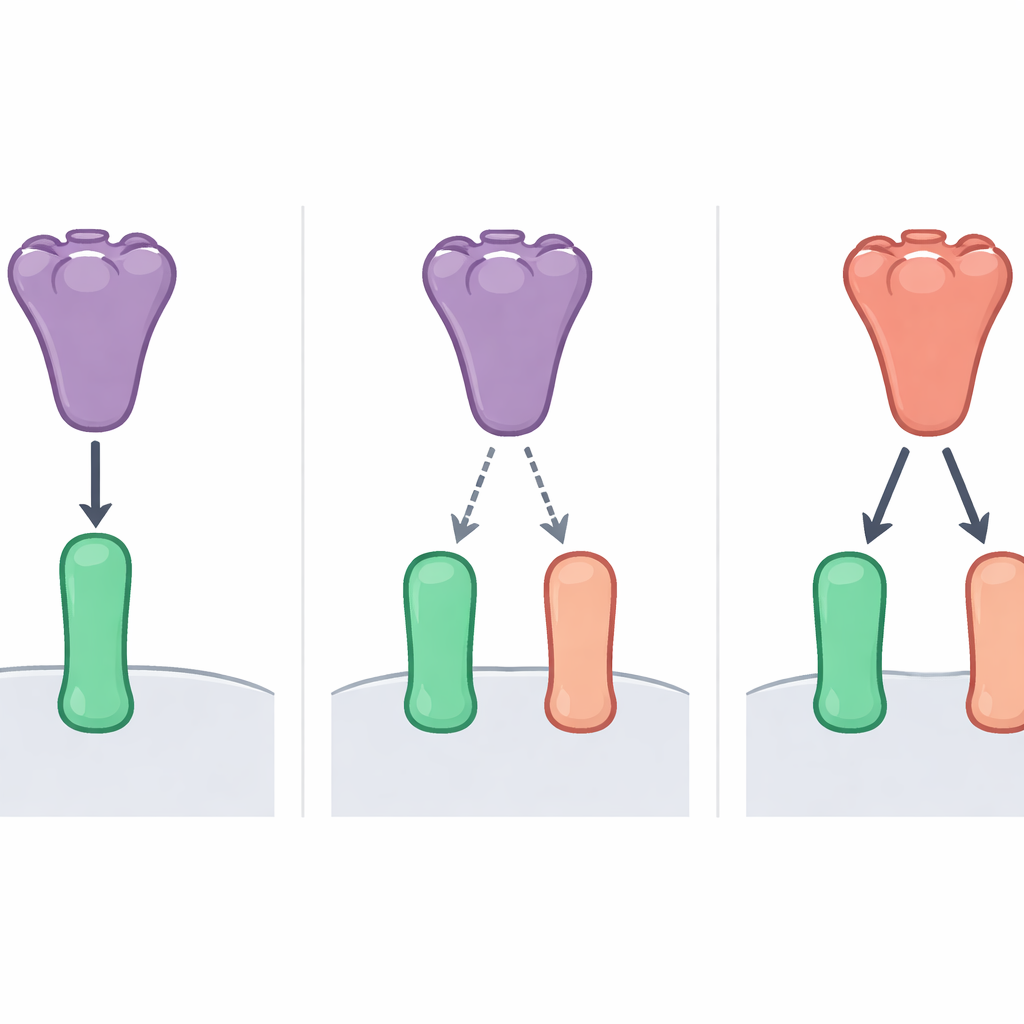
Tek bir atom ölçeğindeki ince ayarın teraziyi nasıl değiştirtiği
Ekip daha sonra viral “parmak” ile ACE2 “kapı kolu”nun atom düzeyinde nasıl temas ettiğini görmek için X-ışını kristalografisine yöneldi. İki kilit konuma odaklandılar: viral RBD üzerindeki bir konum (498 numaralı kalıntı) ve ACE2 üzerindeki bir konum (41 numaralı kalıntı). BANAL-52’de hem viral bölge hem de yarasa ACE2 bölgesi aynı yapı taşı olan histidini kullanıyor; bu da çok sıkı, katmanlı bir etkileşime izin veriyor—iki para gibi üst üste dizilme ve ayrıca bir hidrojen bağı oluşturma. İnsan ACE2’sinde aynı yerde benzer ama biraz farklı bir yapı taşı olan tiyrozin bulunuyor; tiyrozin BANAL-52’nin histidini ile iyi üst üste dizilme sağlasa da ekstra hidrojen bağından yoksun. SARS-CoV-2 ise bu viral pozisyonda glutamin kullanıyor; glutamin aynı şekilde üst üste dizilemediği için hem yarasa hem de insan ACE2’ye daha zayıf bağlanmayla sonuçlanıyor. Araştırmacılar yarasa ACE2’sindeki bu amino asitleri kasıtlı olarak değiştirerek, tek bir temas noktasının güçlendirilmesinin veya zayıflatılmasının hangi viris veya konağın tercih edildiğini değiştirebileceğini doğruladılar.
İnsan ACE2 neden bu kadar davetkâr bir kapı
Bu tek temastan öte, yazarlar genel olarak insan ACE2’nin neden koronavirüsler için bu kadar etkili bir kapı olduğu sorusunu sordular. Yarasa ve insan ACE2’lerini yan yana karşılaştırarak, viral tokalaşmayı iyileştiren birkaç insan özgü özelliği tespit ettiler. İnsan ACE2’deki iki pozisyon—34 numaralı yerde histidin ve 82 numaralı yerde metiyonin—daha güçlü hidrojen bağları ve viral RBD’nin daha sıkı yerleşmesine yardımcı olan yağlı “yama”lar oluşturuyor. Başka bir insan kalıntısı olan 27 numaralı pozisyondaki treonin, bağlanmayı yarasa versiyonuna göre biraz zayıflatıyor, ancak genel olarak ek olumlu temaslar üstün geliyor. Bu ayrıntılar, insan ACE2’nin çok çeşitli koronavirüsler için doğal olarak çekici bir reseptör olmasını sağlayan birden fazla “sıcak nokta”ya sahip olduğunu gösteren önceki çalışmalarla uyumlu.
Köken hikâyesini yeniden çerçevelemek
Tüm verileri bir araya koyduğunda çalışma, SARS-CoV-2 ile yarasa akrabalarının olağan evrimsel senaryoyu takip etmeye devam ettiğini savunuyor. BANAL-52’nin spike’i belirli yarasaların ACE2’sine en iyi şekilde uyum sağlamış görünürken, aynı zamanda insan ACE2’siyle de uyumlu. SARS-CoV-2’nin spike’i ise özel temas noktalarının yardımıyla yarasa ACE2’sinden ziyade insan ACE2’sine daha iyi ayarlı durumda. Sadece birkaç pozisyondaki küçük değişiklikler—özellikle viral 498 numaralı kalıntı ve komşu bölgelerde—hedeflenen konak lehine dengeyi kaydırabilir. Uzman olmayanlar için çıkarım, egzotik açıklamalara başvurmaya gerek olmadığıdır: protein–protein etkileşiminin standart, iyi anlaşılan yapısal ilkeleri bu virüslerin yarasa ve insan hücrelerini nasıl tanıdığını açıklamak için yeterlidir ve bu bulgular SARS-CoV-2 ile ilişkili yarasa koronavirüsleri arasında yakın bir evrimsel bağı destekler.
Atıf: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Anahtar kelimeler: SARS-CoV-2 evrimi, yarasa koronavirüsleri, ACE2 reseptörü, virüs konak aralığı, spike proteini bağlanması