Clear Sky Science · tr
Afrika domuzu vebası virüsü tarafından kodlanan MGF 505–3R proteini, MyD88’in ubiquitin aracılı yıkımı yoluyla doğuştan gelen bağışıklığı zayıflatıyor
Hayvan sağlığı ve ötesi için neden önemli
Afrika domuzu vebası, dünya çapında domuz çiftliklerini harap ederek gıda tedarikini tehdit etti ve büyük ekonomik kayıplara yol açtı. Hastalığa neden olan virüs, kısmen vücudun erken uyarı sistemlerini atlatması nedeniyle ölümcüldür. Bu çalışma, MGF 505–3R adı verilen bir viral proteinin hücre içindeki kritik bir alarm anahtarını nasıl sabote ettiğini ortaya koyuyor ve aynı proteinden türetilen küçük bir parçanın farelerde güçlü bir anti-inflamatuar araca dönüştürülebileceğini gösteriyor.
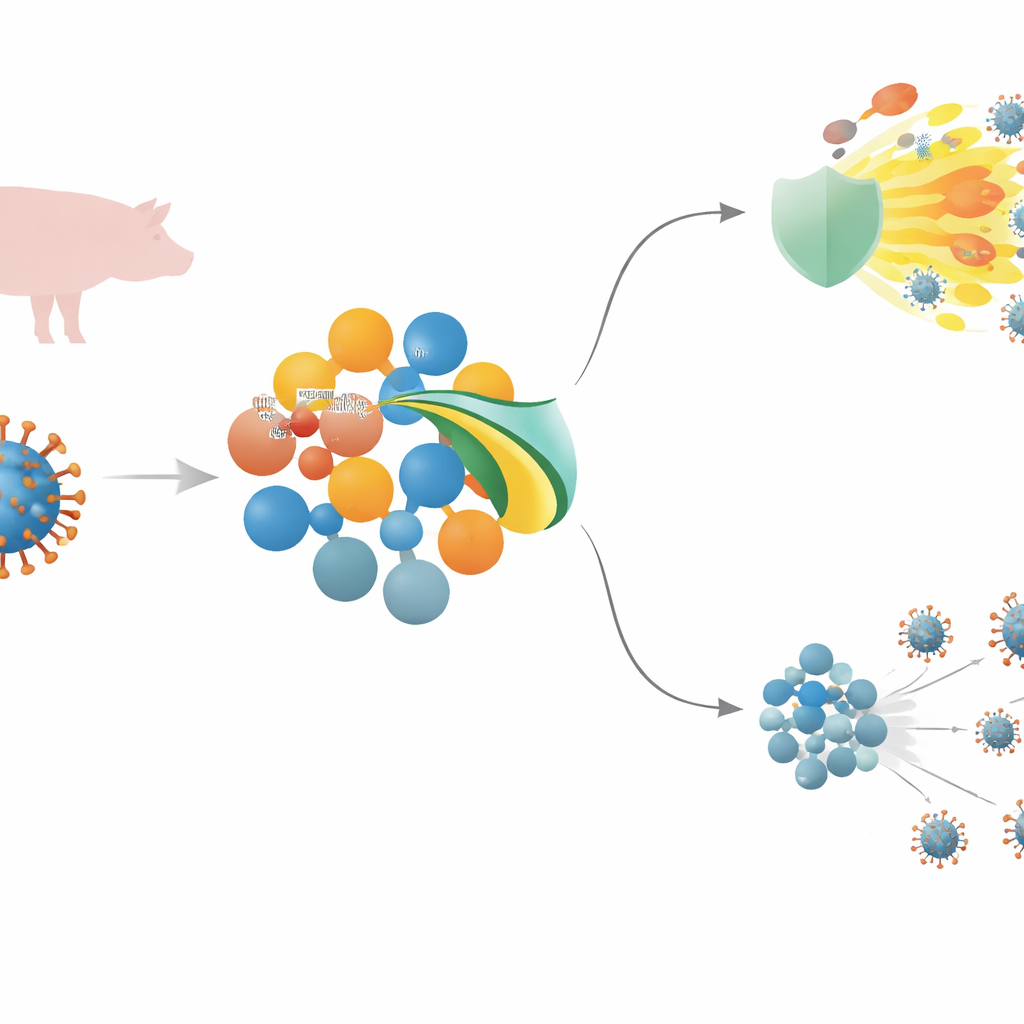
Ölümcül bir domuz virüsü ve vücudun ilk savunma hattı
Afrika domuzu vebası virüsü (ASFV), neredeyse enfekte olan tüm domuzları öldürebilen büyük bir DNA virüsüdür. Yerleşebilmek için, istilacıları algılayan ve iltihap ile antiviral molekülleri tetikleyen hızlı, ön cephe savunması olan doğuştan gelen bağışıklığı alt etmelidir. Bu yanıtın merkezinde, hücre yüzeyindeki algılayıcılardan MyD88 adlı bir ara proteine ve NF–κB olarak bilinen ana anahtara kadar uzanan bir sinyal zinciri vardır; bunlar birlikte inflamatuar habercilerin ve antiviral interferonların üretimini yönlendirir. ASFV, bu sinyalleri bozduğuna inanılan birçok gen taşır, ancak MGF 505–3R dahil bazıları için mekanizmalar tam olarak anlaşılmamıştı.
Virüsün bağışıklık alarmının kablolarını nasıl kestiği
Araştırmacılar, ASFV proteinlerini NF–κB aktivitesini azaltma yeteneklerine göre taradılar ve MGF 505–3R’nin özellikle güçlü bir inhibitör olduğunu buldular. Bu viral protein var olduğunda, farklı bağışıklık tetikleyicilerine maruz kalan hücreler çok daha az inflamatuar sitokin ve çok düşük düzeyde tip I ve tip III interferon üretti. Daha yakından incelendiğinde, MGF 505–3R’nin birçok bağışıklık algılayıcısını NF–κB’ye bağlayan merkezi adaptör MyD88 üzerinde doğrudan etki ettiği görüldü. MGF 505–3R, MyD88’e bağlanır ve onu K48-bağlantılı ubiquitinasyon adı verilen bir etiketleme yoluyla hücrenin protein parçalayıcı mekanizmasına işaretler. MyD88 yıkıma uğradıkça, NF–κB çekirdeğe geçip koruyucu genleri açamaz ve hücreler virüsün büyümesine daha elverişli hale gelir.
Küçük ama güçlü bir protein parçasına yakın plan
MGF 505–3R’nin kritik bölümünü belirlemek için ekip, proteinin kısaltılmış versiyonlarını üretti ve etkilerini test etti. Amino asit 89–277 aralığının MyD88’e bağlanmak, onun ubiquitinasyonunu teşvik etmek ve NF–κB aktivasyonunu engellemek için hem gerekli hem de yeterli olduğunu keşfettiler. Bilgisayar destekli protein yapı tahminleriyle yönlendirilerek, bu bölgeden iki kısa peptit çıkardılar. Bunlardan biri olan pep3R–1 öne çıktı: NF–κB aktivitesini keskin bir şekilde azalttı, NF–κB alt birimi p65’in fosforilasyonunu ve çekirdeğe geçişini engelledi ve farklı tehlike sinyalleriyle uyarılmış bağışıklık hücrelerinde inflamatuar sitokinlerin ve interferonların ifadesini düşürdü. Hücre kültüründe, hem tam uzunlukta MGF 505–3R hem de pep3R–1 antiviral sinyallemeyi zayıflatmakla kalmadı, aynı zamanda bir test virüsünün daha verimli çoğalmasına da izin vererek bu yolun enfeksiyonları kontrol etmede ne kadar güçlü olduğunu vurguladı.
Viral bir hileyi potansiyel bir ilaca dönüştürmek
Ekip daha sonra peptidin virüsleri desteklemek yerine zararlı inflamasyonu yatıştırmak için kullanılıp kullanılamayacağını sordu. DSS adlı bir kimyasal ile tetiklenen kolit fare modelinde, hayvanlar normalde kilo kaybeder, kanlı ishal geliştirir ve kolonda şiddetli doku hasarı ile bağışıklık hücresi istilası görülür. Pep3R–1 ile tedavi edilen fareler çok daha iyi durumda oldu: hastalık skorları daha düşüktü, kolonlar daha uzun ve sağlıklıydı ve mikroskopik inceleme korunan doku yapısı ve çok daha az inflamatuar hücre gösterdi. Kolon dokusu ve kanda TNF–α, IL–1β, IL–6 gibi önemli inflamatuar moleküller ile beyaz kan hücresi göçüyle ilişkili bir enzimin seviyeleri azaldı. Ayrı bir deneyde, pep3R–1 sistemik bir bakteriyel toksine karşı inflamatuar yanıtı da azalttı; bu da hem lokal hem de bütün vücut düzeyindeki inflamatuar fırtınaları yatıştırabildiğini gösteriyor.
Bu bulgunun domuzlar, insanlar ve gelecekteki tedaviler için anlamı
Bu çalışma, ASFV proteini MGF 505–3R’nin MyD88 adlı merkezi bir bağışıklık ara elemanını parçalayarak hem inflamatuar hem de interferon savunmalarını kapattığını ve böylece virüsün güçlenmesine yardımcı olduğunu gösteriyor. Aynı zamanda, bu viral proteinin küçük bir parçası olan pep3R–1’in farelerde aşırı inflamasyonu güvenli bir şekilde yatıştırmak için yeniden amaçlandırılabileceği, özellikle bağırsak hastalığı modelinde fayda sağlayabildiği gösterildi. Stabilite, taşıma ve daha fazla hastalık modelinde test etme gibi yapılması gereken çok şey olsa da, çalışma hem antiviral stratejilerin hedefleyebileceği kritik bir zayıf noktayı hem de viral bağışıklık kaçışından esinlenen yeni peptit tabanlı anti-inflamatuar ilaçların tasarımı için umut verici bir şablonu ortaya koyuyor.
Atıf: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Anahtar kelimeler: Afrika domuzu vebası, doğuştan gelen bağışıklık, NF-kappaB, MyD88, anti-inflamatuar peptit