Clear Sky Science · tr
Gprasp2 eksikliğine sahip farelerde anormal demir homeostazı koklea saç hücresi hasarını ve işitme kaybını kolaylaştırıyor
Günlük işitme için neden önemli
İşitme kaybı genellikle basit bir "aşınma" olarak düşünülse de birçok insan için temelinde genetik kusurlar yatar. Bu çalışma, nadiren incelenen bir gen olan GPRASP2’nin iç kulağın hassas ses algılayıcı hücrelerini demir kaynaklı hasardan nasıl koruduğunu ortaya koyuyor. Bu gen eksik olduğunda nelerin yanlış gittiğini göstererek kalıtsal işitme sorunları ve muhtemelen ilişkili duygudurum bozuklukları için daha kesin tanılar ve gelecekteki tedavilere kapı açıyor.
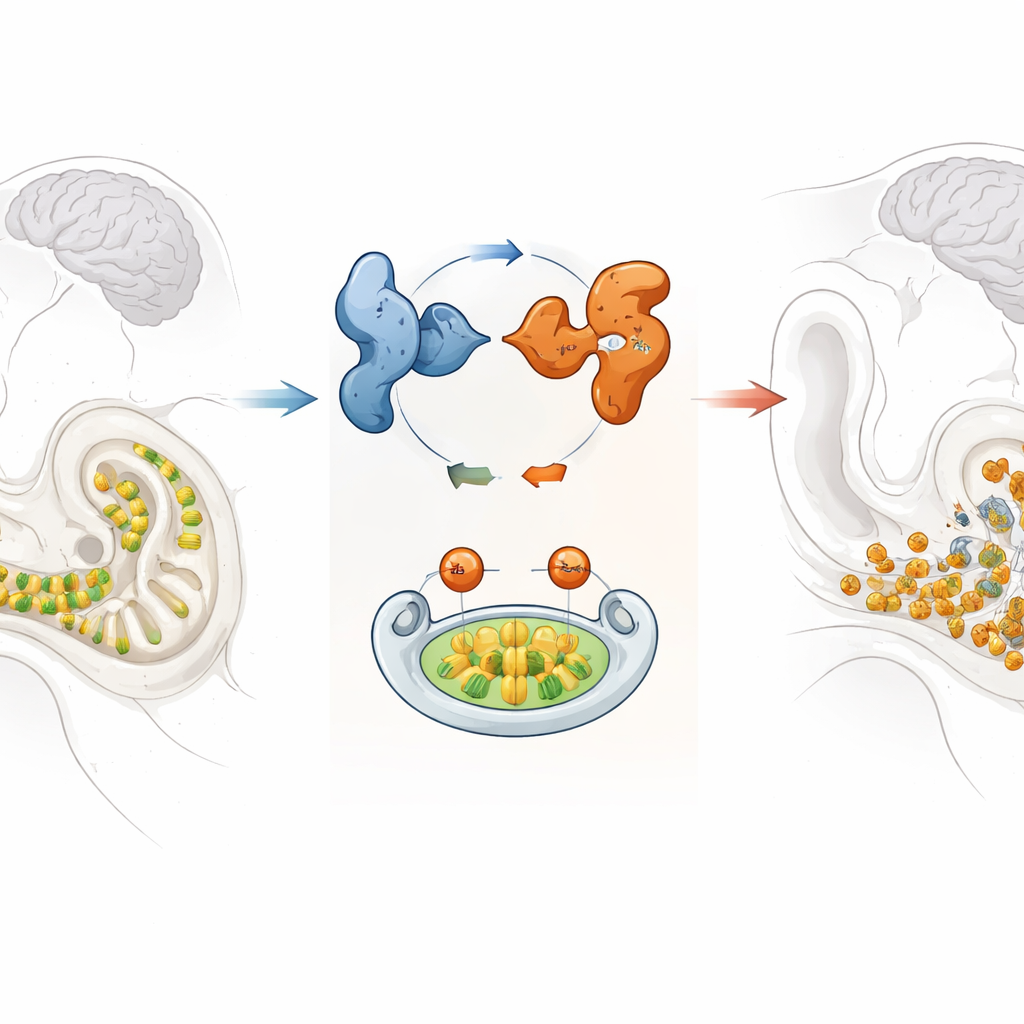
İç kulaktaki kırılgan bir ses algılayıcısı
Kıvrımlı kokleanın içinde, küçük titreşimleri beynin anlayabileceği elektrik sinyallerine çeviren sıralar halinde saç hücreleri bulunur. Bu saç hücreleri bir kez kaybolduğunda geri dönmezler; bu yüzden onları sağlıklı tutmak ömür boyu işitme için kritik öneme sahiptir. Araştırmacılar, X'e bağlı sendromik işitme kaybı olan bir ailede mutasyonlu bulunduğu daha önce saptanan GPRASP2 genine odaklandı; bu durum ağırlıklı olarak erkekleri etkiler ve ek semptomlarla birlikte olabilir. GPRASP2’nin beyin ve iç kulakta etkin olduğu bilinse de işitmedeki kesin rolü net değildi.
Gen yoksa ne oluyor
İnsan durumunu taklit etmek için ekip, CRISPR gen düzenleme kullanarak Gprasp2 geninin işleyen bir kopyasından yoksun fareler oluşturdu. Bu hayvanlar, işitsel sinirden hassas elektrik kayıtlarıyla test edildiğinde geniş bir frekans aralığında belirgin işitme kaybı gösterdi. Ani yüksek seslere yanıtları azalırken denge ve motor becerileri büyük ölçüde normal kaldı; bu, genel bir hareket bozukluğundan ziyade spesifik bir işitme problemini işaret ediyor. İlginç olarak, fareler birkaç standart testte depresyona benzer davranışlar da sergiledi; bu da bu genin kulak ve beyindeki etkileri yoluyla işitme ile ruh hali arasında bir bağlantı olduğunu düşündürüyor.
Kokleada görülen hasar
Araştırmacılar Gprasp2 eksik farelerin iç kulaklarını incelediklerinde birçok dış saç hücresinin eksik veya yerinden çıkmış olduğunu ve kalan hücrelerin sıklıkla normalde akort çatalı gibi davranan küçük çıkıntılarının bozulduğunu buldular. Ayrıca işitme için gereken özel sıvı ve elektrik ortamını koruyan çok aktif bir doku olan stria vascularis’te değişimler gözlendi. Mikroskobik düzeyde, dış saç hücreleri ve yakınlardaki sinir hücrelerinde hücre ölümü ve oksidatif stres belirteçleri yükselmişti; bu da bu yapıların reaktif moleküllerin yoğun saldırısı altında olduğunu ve ölme olasılıklarının arttığını gösteriyor.
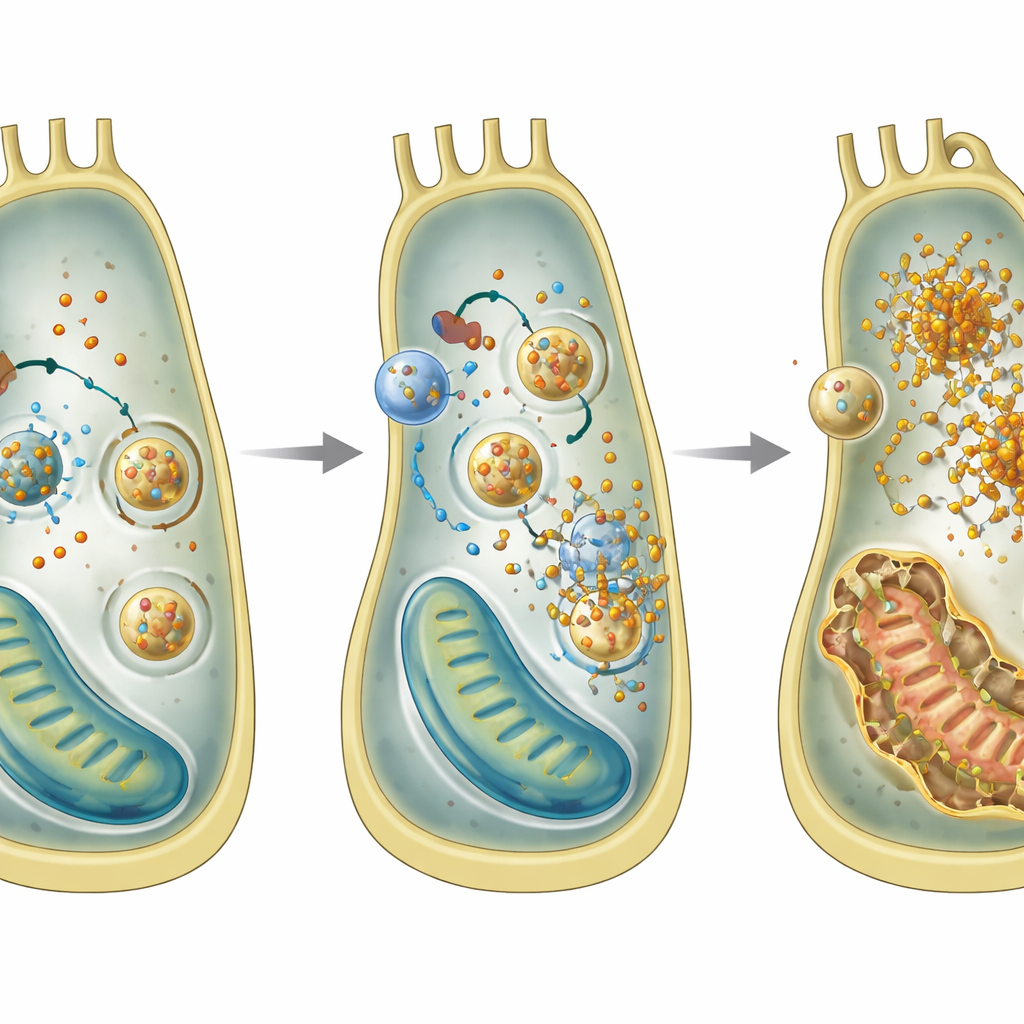
Demir birikimi ve kontrolsüz geri dönüşüm
Daha derine inerek ekip, GPRASP2 olmayan bireysel hücrelerde nelerin yanlış gittiğini araştırmak için bir iç kulak hücre hattı kullandı. Demir ve lipid peroksidasyonuyla tetiklenen bir hücre ölümü biçimi olan ferroptozu andıran bir desen keşfettiler. Gprasp2’den yoksun hücreler daha fazla ferroz demir biriktirdi, daha fazla reaktif oksijen türü üretti, antioksidan glutatyon seviyeleri düştü ve mitokondriler hasar gördü. Gen ve protein analizleri, demir depolayan partiküllerin geri dönüşüm veziküllerine aktarılıp parçalandığı ve hücre içine ekstra demir salındığı bir süreç olan ferritinofajide artışa işaret etti. Bu geri dönüşüm adımının engellenmesi demir birikimini azalttı; bu da aşırı ferritinofajinin hasarın merkezinde olduğu fikrini destekliyor.
Demiri dengeleyen önemli bir partner protein
Araştırmacılar daha sonra GPRASP2’nin bu demir yönetim mekanizmasını nasıl kontrol ettiğini sordular. GPRASP2 ile etkileşen proteinleri eşleyerek, öğrenme, hafıza ve ruh hali rollerleriyle en iyi bilinen hücre yapışma molekülü NCAM1’i tanımladılar. GPRASP2’nin fiziksel olarak NCAM1’e bağlandığını ve GPRASP2 kaybının saç hücrelerinde ve kültürdeki işitsel hücrelerde NCAM1 seviyelerinin düşmesine neden olduğunu gösterdiler. Düşük NCAM1 seviyesi ferritinofaji ve demir birikimi artışıyla ilişkilendirildi. Gprasp2-eksik hücrelerde NCAM1’i geri getirmek demir düzeylerini azalttı ve genel otofaji aktif olsa da başlıca ferritinofaji düzenleyicilerini baskıladı. Bu, GPRASP2’nin tüm geri dönüşüm sistemini açıp kapatmak yerine NCAM1 aracılığıyla belirli bir demir geri dönüşüm yolunu ince ayarladığı fikrine işaret ediyor.
İşitme ve ötesi için ne anlama geliyor
Basitçe ifade etmek gerekirse, bu çalışma GPRASP2’nin kokleanın saç hücreleri içinde demir için bir güvenlik yöneticisi gibi davrandığını gösteriyor. GPRASP2 varken, NCAM1 ile iş birliği yaparak depolanmış çok fazla demirin hücre içine geri dökülmesini engeller ve oksidatif hasarı kontrol altında tutar. Gen bozulduğunda demir dengesi bozulur, hücreler içten paslanır ve kritik saç hücreleri ölür; bu da işitme kaybına yol açar. GPRASP2 ve NCAM1’in beyinde de işlev göstermesi nedeniyle aynı yolak bazı hastalarda görülen ruh hali değişikliklerini de açıklayabilir. Bu demire dayalı arızayı anlamak, GPRASP2 ilişkili veya benzer genetik bozuklukları olan kişilerde işitmeyi korumaya yönelik ilaçlar veya gen terapileri için açık bir hedef sunuyor.
Atıf: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
Anahtar kelimeler: kalıtsal işitme kaybı, koklean saç hücreleri, demir homeostazı, ferroptoz, GPRASP2