Clear Sky Science · tr
Hedefe yönelik tek hücreli RNA dizileme teknolojilerine pratik bir rehber
Neden tek hücrelere bakmak önemli
Vücudunuzdaki her hücre aynı DNAya sahip olmasına rağmen, farklı hücreler çok farklı biçimlerde davranır. Bunu belirli genleri açıp kapatarak ve RNA moleküllerini ince düzenlemelerle değiştirerek yaparlar. Modern tek hücreli RNA dizileme yöntemleri binlerce hücrede hangi RNAların bulunduğunu okuyabiliyor, ancak şu anda mesajın çoğunu kaçırıyor. Bu derleme, günümüz tekniklerinin nerede bilgi kaybettiğini ve yeni "hedefe yönelik" yaklaşımların araştırma, tanı ve tedavi tasarımında RNA moleküllerinin en önemli bölümlerine nasıl odaklandığını açıklıyor.
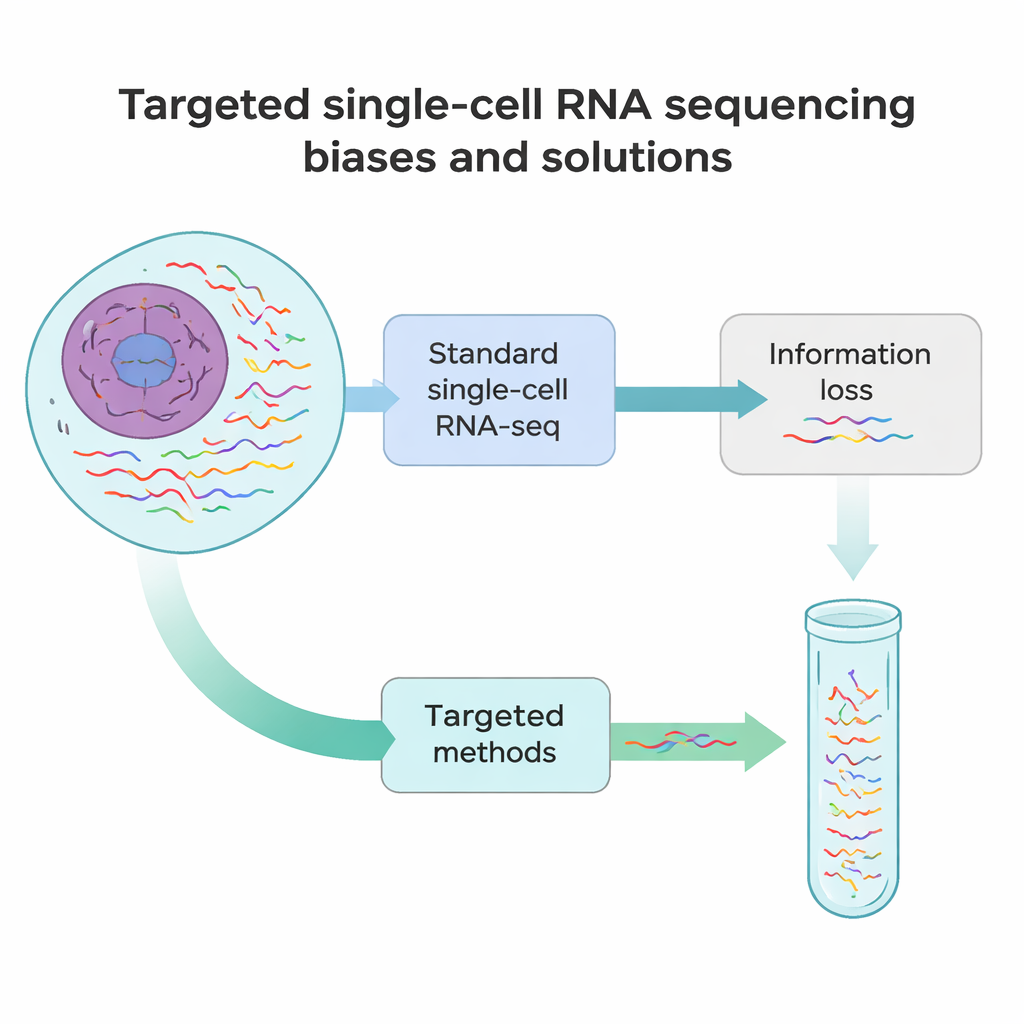
Günümüz yöntemlerinin eksikleri
Standart tek hücreli RNA dizileme, her mesajın tamamını izlemek yerine hızlı bir anlık fotoğrafını çekmeye benzer. Çoğu deneyde bir hücredeki tüm RNAların yalnızca yaklaşık %10–40ı tespit edilir ve genellikle yalnızca başlangıcı veya ucu okunur. Bu, bir hücrenin kimliğini belirleyen belirteçler ya da hastalık yapıcı mutasyonlar taşıyan gen versiyonları gibi nadir ama önemli birçok RNAun kolayca gözden kaçırılacağı anlamına gelir. Buna ek olarak, dokuları tek hücrelere ayırmaktan RNAyı DNAa kopyalamaya ve çoğaltmaya kadar birçok teknik adım sistematik yanlılıklar getirir. Bazı RNAlar erken kesilir, bazıları aşırı temsil edilir ve diğerleri verilerden tamamen kaybolur.
RNA iç detaylarının önemi
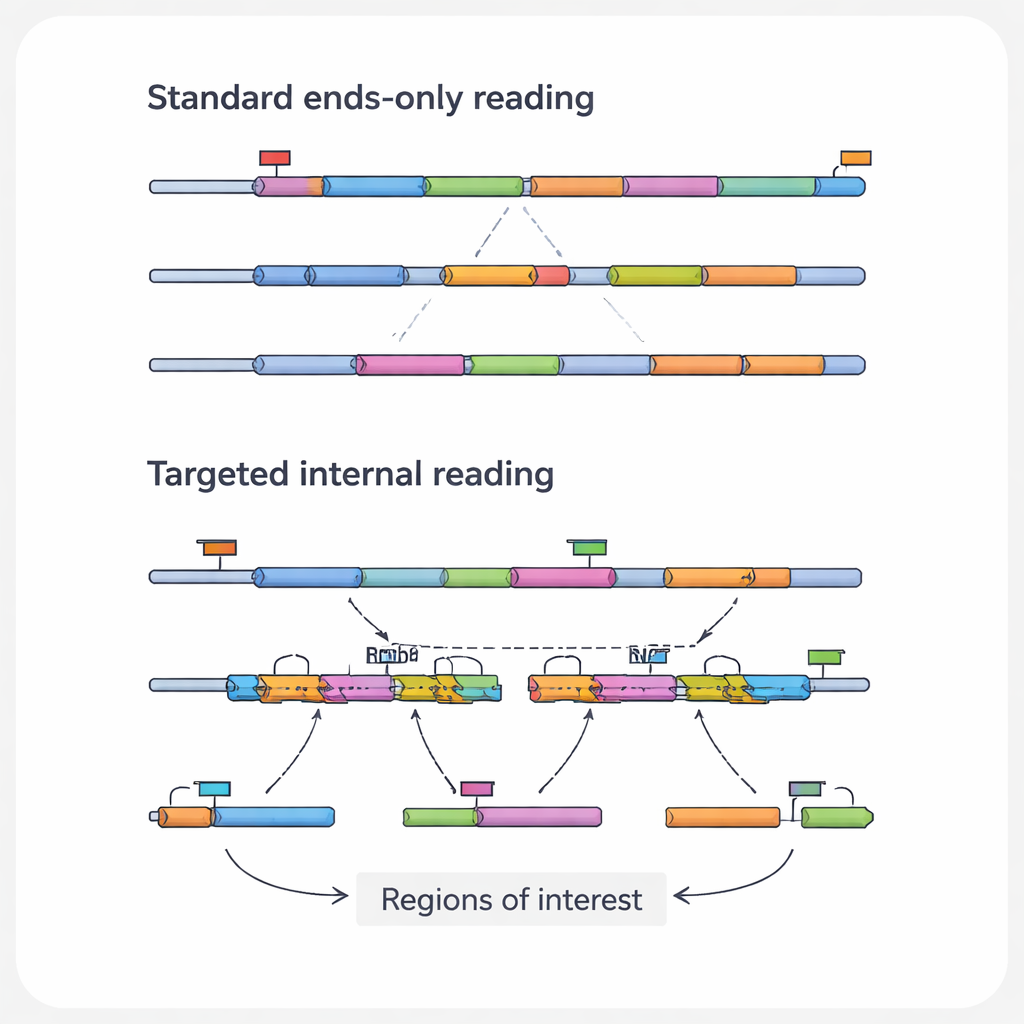
Bir RNA molekülündeki en tıbbi açıdan ilgili bilgi çoğunlukla standart yöntemlerin gördüğü uçlarda değil, iç bölgelerde yatar. Bu iç kısımlar kanseri yönlendiren nokta mutasyonlarını, iki genin anormal şekilde birleştirildiği füzyon noktalarını veya aynı genden farklı protein varyantları yaratan ekzon-birleştirme (splice) bağlantılarını içerebilir. Ayrıca CRISPR gibi gen düzenleme araçlarının izlerini de kaydedebilirler. Yazarlar bu özgül özelliklere "ilgi bölgeleri", bunları taşıyan RNAlara ise "ilgi transkriptleri" diyor. Yaygın yüksek verimli platformlar esasen RNAların uçlarını okuduğu için, özellikle uzun veya düşük bolluklu transkriptlerde bu kritik ayrıntıları rutin olarak göz ardı ederler.
Işık noktasını hedeflemeye dair yeni yollar
Bu kör noktaların üstesinden gelmek için araştırmacılar hedefe yönelik tek hücreli RNA dizileme yaklaşımlarından oluşan bir aile geliştirdi. Her RNAı eşit okumaya çalışmak yerine, bu yöntemler seçilmiş transkriptler veya bölgeler için bilerek zenginleştirme yapar. Bazı stratejiler, yakalama boncuklarını sadece kuyrukla değil iç RNA dizilerine de tutunacak şekilde yeniden tasarlayarak seçilmiş mesajları ilk adımdan itibaren kütüphaneye çeker. Diğerleri iç noktadan kopyalamaya başlayan özel primerler ekler veya mevcut bir kütüphaneden belli bir gen listesini özel olarak çoğaltan ek PCR adımları kullanır. Bir başka grup ise hedef RNAlara veya onların kopyalarına hibritleşen ve genellikle basit kimyasal etiketlerle bunları çeken DNA probları kullanır. Her kategori duyarlılık, hücre sayısı, hedef sayısı ve maliyet arasında takas yapar, ancak tümünün ortak amacı aynı veya daha az dizileme okumasından daha anlamlı ayrıntı elde etmektir.
Virüslerden tümörlere uygulamalar
Bu hedefe yönelik yöntemler biyoloji ve tıbbın birkaç alanını şimdiden yeniden şekillendiriyor. Enfeksiyonlarda, standart protokollerin beklediği poli(A) kuyruklarına sahip olmayan viral veya bakteriyel RNAları nihayet yakalayarak hangi konak hücrelerde bulunduklarını ve konak gen etkinliğini nasıl değiştirdiklerini ortaya koyabiliyorlar. Kanserde, hedefe yönelik tek hücre dizileme hangi hücre tiplerinin belirli mutasyonları veya füzyon genleri taşıdığını ve bunların değişmiş gen programlarıyla nasıl ilişkilendiğini tespit ederek bazı hücrelerin neden tedaviye dirençli hale geldiğini açıklamaya yardımcı olabiliyor. Diğer yöntemler alternatif ekzon kullanımına odaklanarak hangi hücre tiplerinin hangi izoformları kullandığını açığa çıkarıyor veya aksi takdirde tespit eşiğinin altında kalacak nadir hücre popülasyonları ve ince belirteçleri hedefliyor. Havuzlanmış CRISPR ekranlarında rehber RNAlyı daha iyi yakalamak, her genetik müdahaleyi onun kesin hücresel yanıtıyla ilişkilendirmeyi sağlıyor.
Doğru aracı seçmek ve gelecekte neler beklenmeli
Artık hedefe yönelik yaklaşımlardan oluşan kalabalık bir araç kutusu bulunduğundan, yazarlar araştırmacılara yöntem seçmede yardımcı olacak bir karar ağacı öneriyor. Temel sorular arasında tam transkriptom profilinin gerekip gerekmediği, kaç genin veya bölgenin hedeflenmesi gerektiği, bu bölgelerin RNA uçlarından ne kadar uzakta olduğu ve kaç hücrenin işlenebileceği yer alıyor. İleriye bakıldığında, en büyük kazançların ilk yakalama adımlarını iyileştirmekten, zeki prob tabanlı stratejileri genişletmekten ve hedeflemeyi yeni çıkan uzun-okuma ve doğrudan RNA dizileme platformlarıyla birleştirmekten geleceğini savunuyorlar. Her RNAın her hücrede uçtan uca okunmasının pratik olmadığı sürece, hedefe yönelik tek hücreli RNA dizileme biyoloji ve hastalık açısından en önemli hücresel mesaj parçalarını görmek için vazgeçilmez olmaya devam edecek.
Atıf: Moro, G., Brunner, E. & Basler, K. A practical guide to targeted single-cell RNA sequencing technologies. Commun Biol 9, 250 (2026). https://doi.org/10.1038/s42003-026-09675-y
Anahtar kelimeler: tek hücreli RNA dizilemesi, hedefe yönelik dizileme, transkriptomik, kanser mutasyonları, uzamsal transkriptomik