Clear Sky Science · tr
Optik fototermal kızılötesi spektroskopi kullanarak Salmonella biyofilmlerinin antibiyotik tedavisine yanıtlarının incelenmesi
Neden Yapışkan Mikrop Kentleri Önemli?
Hastalık yapan birçok bakteri, hücrelerin birbirine ve vücut içindeki yüzeylere veya tıbbi cihazlara yapıştığı, sıkı paketlenmiş topluluklar olan biyofilmlerde yaşamayı tercih eder. Bu sümüksü “kentler” içinde mikroplar normalde onları öldürecek antibiyotiklere karşı dayanma eğilimindedir. Bu çalışma, biyofilmlerin içini ince ayrıntıyla görmenin yeni bir yolunu sunuyor; hangi hücrelerin aktif olarak büyüdüğünü ve güçlü ilaçlar eklendiğinde nasıl tepki verdiklerini ortaya koyuyor. Bu görünmez aktivite desenlerini anlamak, hekimlerin biyofilmlerin inatçı savunmalarını nihayet kırabilecek tedaviler tasarlamasına yardımcı olabilir.
Bakteri Kentlerinin İçindeki Gizli Yaşam
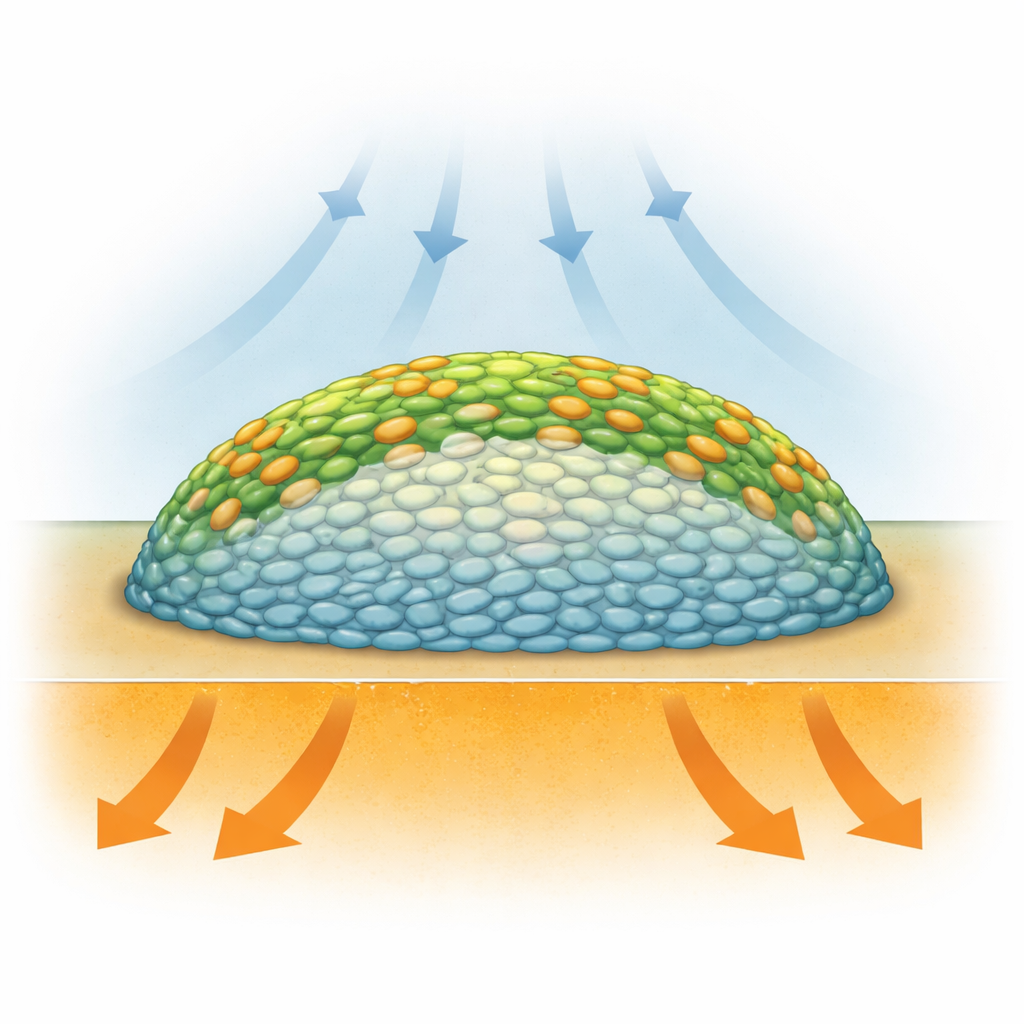
Biyofilmler sadece rastgele mikrop toplulukları değildir: konumlarına bağlı olarak bakterilerin çok farklı koşullarda yaşadığı katmanlı yapılardır. Dıştaki hücreler havadan daha fazla oksijene erişirken, merkezde gömülü olanlar oksijen kıtlığı yaşar ve yavaşlayabilir veya uykuda kalabilir. Floresan mikroskopi gibi önceki yöntemler yapıyı gösterebilir, ancak genellikle biyolojiyi bozabilecek boyalar veya genetik işaretleyiciler gerektirir ve hücrelerin kimyasal olarak ne yaptığını doğrudan ölçmez. Araştırmacılar, biyofilmleri parçalamadan veya ağır şekilde değiştirmeden, katman katman canlı biyofilmlerin kimyasını “görebilecek” bir yönteme ihtiyaç duydular.
Görünmez Işıkla Kimyayı Görmek
Araştırma ekibi, moleküllerdeki küçük titreşimleri algılamak için görünmez kızılötesi ışık atımları ve görünür bir lazer kullanan optik fototermal kızılötesi (O-PTIR) spektroskopisi adlı bir tekniğe yöneldi. Bu titreşimler, proteinler, yağlar ve DNA gibi önemli hücresel bileşenlerin parmak izleri gibi davranır. Metabolizmayı—besinlerin aktif kullanımını—izlemek için Salmonella Typhimurium biyofilmlerine karbon atomları olağandan biraz daha ağır olan özel bir şeker (karbon-13 olarak bilinen kararlı bir izotop) verildi. Hücreler aktif olarak büyüyüp yeni proteinler ürettiklerinde, bu daha ağır atomları kendi yapılarına dahil ederler; bu da kızılötesi sinyalde ince ama tespit edilebilir değişimlere yol açar. Biyofilmi kriyoseksiyonla kesitleyip ince enine kesitleri tarayarak, araştırmacılar bu ağır karbonun biyofilm içinde nerelere işlendiğini gösteren kimyasal haritalar üretti.
Aktivite Halkaları ve Sessiz Çekirdekler
Tedavi edilmemiş Salmonella biyofilmlerinin kızılötesi görüntülemesi çarpıcı bir desen ortaya koydu: dış bölgeler ve yüzey katmanları ağır karbonun güçlü entegrasyonunu gösterirken, büyük merkezi bir çekirdek çok az gösteriyordu. Başka bir deyişle, biyofilm aktif hücrelerden oluşan bir halka ile sessiz bir iç kısmın etrafında davrandı. Kızılötesi spektral verilerin istatistiksel analizi, proteinle ilişkili titreşim sinyallerinin merkezdekilere göre dış katmanlarda daha fazla kayma gösterdiğini doğruladı; bu da kenarlarda daha yüksek protein üretimine işaret ediyor. Bu bulgular, yüzeye en yakın yerde oksijen erişiminin—besinlerin alttan akmasına rağmen—bu koloni modelinde metabolik “sıcak bölgelerin” ana itici gücü olduğu fikrini destekliyor. Çalışma, bir biyofilm içinde metabolizmanın nasıl tabakalandığını şimdiye kadar görülmüş en açık, yüksek çözünürlüklü görünümlerden biriyle sundu.
Farklı Antibiyotiklerin Biyofilm Aktivitesini Nasıl Yeniden Şekillendirdiği
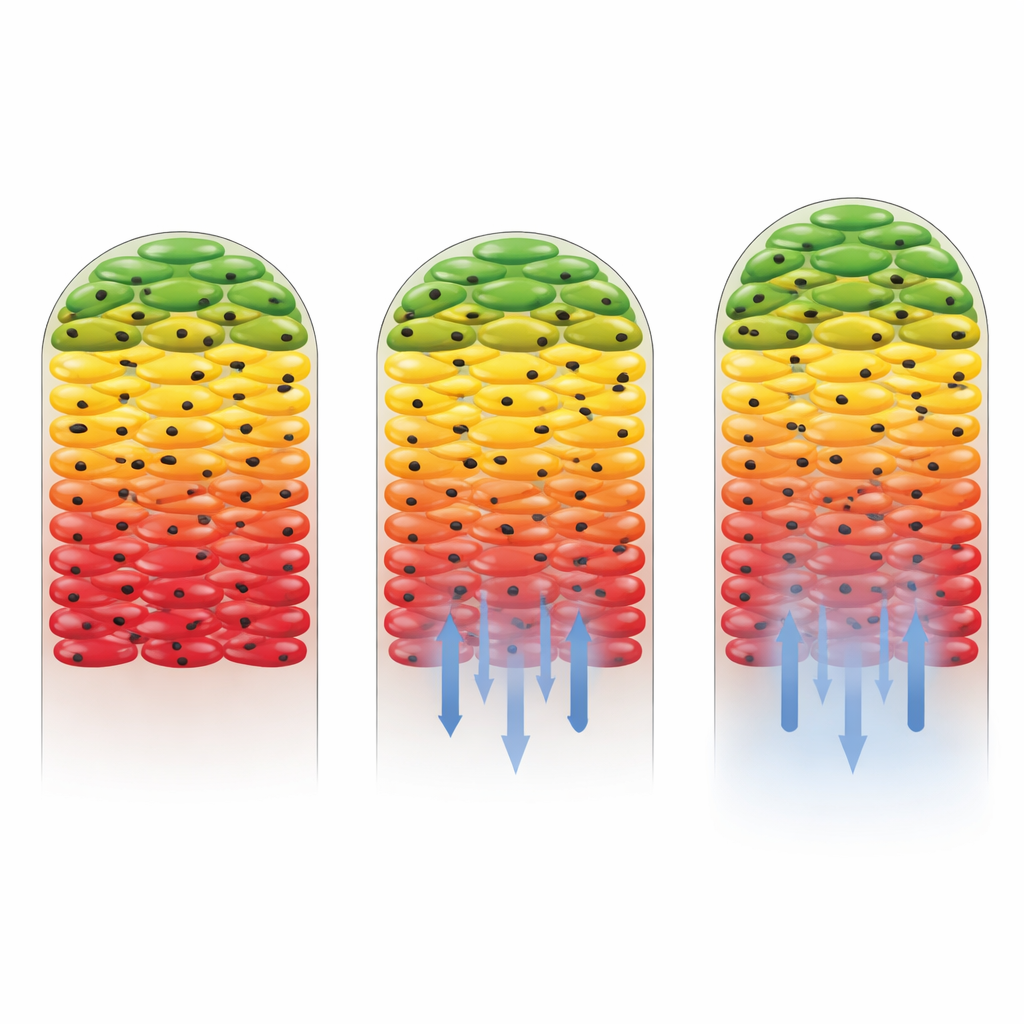
Araştırmacılar daha sonra antibiyotikler eklendiğinde ne olduğunu sordular. İki ilaç kullandılar: Salmonella suşunun duyarlı olduğu kanamisin (kanamisin yerine kanamisin benzeri bir aminoglikozid olan kanamisin olarak düşünülmüş olabilir) ve suşun büyük ölçüde duyarsız olacak şekilde genetik olarak düzenlendiği gentamisin. Gentamisin varlığında, aktif dış katmanlar ve sessiz çekirdek olan genel desen neredeyse değişmedi; bu, dirençli hücrelerin biyofilmin büyük bir bölümünde büyümeye ve ağır karbonu işlemeye devam ettiğini gösterdi. Buna karşılık, kanamisin metabolik aktiviteyi, özellikle ilacın konsantrasyonunun en yüksek olduğu biyofilmin alt kısmında dramatik biçimde azalttı. Antibiyotik kaynağından en uzaklardaki sadece ince bir hücre bandı hâlâ karbon alım belirtileri gösteriyordu. Bu, ilacın etkili olduğunu göstermesinin yanı sıra, biyofilm yapısının içe doğru difüze olurken bazı hücreleri zayıflatarak ilacı koruduğunu da ortaya koydu.
Zorlu Enfeksiyonları Tedavi Etmeye Yeni Pencereler
Halk açısından ana mesaj, bu çalışmanın bakteriyel toplulukların üç boyutta nasıl yaşadığını ve tedavi sırasında nasıl hayatta kaldığını izlemek için güçlü bir “kimyasal mikroskop” sunduğu. Tahribatsız bir kızılötesi görüntüleme yöntemi ile güvenli bir ağır karbon formunu birleştirerek araştırmacılar hangi bakterilerin aktif olarak büyüdüğünü ve bu aktivitenin farklı antibiyotikler altında nasıl kaydığını kesin olarak saptayabildiler. Sonuçları, biyofilmlerin meşgul ve neredeyse uykuda hücrelerin bir karışımını barındırdığını ve etkili ilaçların bile biyofilmin fiziksel bariyeri tarafından etkisizleştirilebileceğini doğruluyor. Gelecekte bu yaklaşım yeni tedavileri test etmek, farklı türlerin karışık biyofilmler içinde nasıl işbirliği yaptığını veya direnci nasıl paylaştığını keşfetmek ve nihayetinde kalıcı enfeksiyonları temizlemek için daha akıllı stratejiler tasarlamaya yardımcı olmak için kullanılabilir.
Atıf: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Anahtar kelimeler: biyofilmler, Salmonella, antibiyotik direnci, kızılötesi görüntüleme, kararlı izotop izleme