Clear Sky Science · tr
Preklinik nükleik asit terapilerinde model seçimi
Genleri İlaçlara Dönüştürmek
Nükleik asit terapileri, çoğu ilacın yaptığı gibi proteinleri engellemek yerine bir adım geriye, genetik iletişimlerimizin düzeyine müdahale eden yeni bir ilaç türüdür. Bu derleme, bilim insanlarının bu RNA hedefli ilaçları hastalara ulaşmadan önce test etmek için doğru laboratuvar ve hayvan modellerini nasıl seçtiğini açıklar. Genel okuyucu için bunun önemi şudur: akıllıca model seçimleri, nadir çocuk hastalıkları ve kalp hastalığı gibi daha yaygın durumlar da dahil olmak üzere genetik hastalıklar için daha hızlı, daha güvenli ve daha etkili tedaviler anlamına gelebilir.
Bu Genetik İlaçları Farklı Kılan Nedir?
Nükleik asit terapileri (NAT’ler), antisens oligonükleotitler (ASO’lar) ve küçük enterferan RNA’lar (siRNA’lar) gibi kısa dizilerden oluşur. Hedeflerini proteinlerin şekil ve kimyasına dayanarak tanımak yerine, DNA’yı altında yatan aynı A‑T ve G‑C eşleşmesi kurallarına benzeyen baz eşleşmesi kurallarıyla tanırlar. Bu onları programlanabilir yapar: değiştirmek istediğiniz RNA dizisini bildiğinizde, yıllarca süren geleneksel kimya süreçleri olmadan genellikle birçok aday ilacı hızla tasarlayabilirsiniz. Zor olan artık “Etkili bir bileşik yapabilir miyiz?” değil, “Gerçekçi bir biyolojik ortamda gerçekten işe yarayıp yaramadığını nasıl ölçeriz?” sorusudur. Çünkü dizideki tek bir harf farkı bile etkiyi sağlayabilir veya ortadan kaldırabilir; bu nedenle doğru test sistemlerinin seçimi kritik hale gelir.
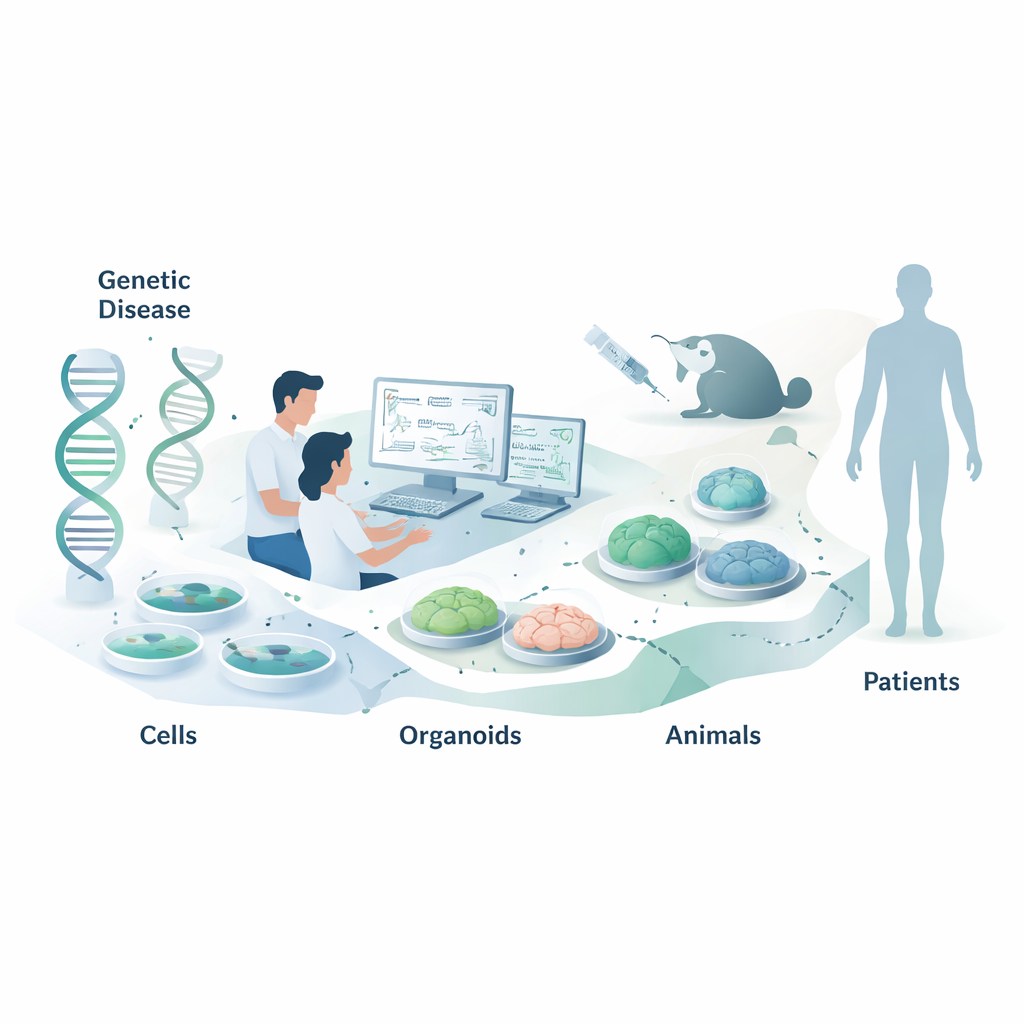
Basit Hücre Testleri: Hızlı ama Tam Hikâye Değil
Çoğu NAT için ilk durak, hedef RNA’yı zaten üreten HeLa veya HEK293 gibi nispeten kolay yetiştirilen hücre hatlarından oluşan panellerdir. Araştırmacılar geniş ASO veya siRNA aday kütüphaneleri ekleyip ardından hedef RNA ve proteinin ne kadar düştüğünü PCR ve Western blot gibi tekniklerle ölçer. Ayrıca hastalardan alınan hücrelerle de çalışılabilir; bunlar kişinin tam genetik arka planını daha iyi yakalar ve yalnızca hatalı gen kopyasını susturan “alel-selektif” ilaçların testine izin verir. Doğal gen uygun şekilde ifade edilmiyorsa, bilim insanları bazen RNA kesildiğinde veya doğru şekilde eksonlanma gerçekleştiğinde parlayan yapay mini-genler veya raporlayıcı plazmitler kullanır. Bu sistemler birçok tasarımı hızlıca karşılaştırmak için güçlüdür, ancak doğal RNA yapısı veya hücre tipi‑spesifik işlemleme gibi önemli ayrıntıları kaçırabilir; bu nedenle sonuçlar daha gerçekçi bağlamlarda doğrulanmalıdır.
Moleküler Düzeltmelerden Gerçek Hücresel Davranışa
Birçok NAT yalnızca hatalı RNA’yı yok etmeyi amaçlamaz; eksonları birleştiren splicing sürecini değiştirerek onarmayı hedefler. Özenle tasarlanmış ASO’lar, hücrelerin zararlı bir eksonu atlamasına, eksik bir parçayı geri getirmesine veya kodu bozan bir “pseudo‑ekson”un eklenmesini engellemesine neden olabilir. Bu tür değişikliklerin gerçekten hücre işlevini iyileştirip iyileştirmediğini görmek için araştırmacılar RNA ve protein seviyelerinin basit okumalarının ötesine geçer. Hasta kaynaklı hücrelerde enzim aktivitesinin geri dönüp dönmediği, akciğer hücrelerinde iyon taşınımının normalleşip normalleşmediği veya bağışıklık hücrelerinde sinyal yollarının doğru yanıt verip vermediği test edilir. Artan şekilde, hastalardan alınan kök hücrelerden yetiştirilen kalp atışlarını, beyin ağ aktivitesini veya diğer karmaşık davranışları taklit edebilen üç boyutlu organoid’ler kullanılır. Bu 3‑D modeller gerçek organlara daha yakındır ancak çalıştırılması daha zor, daha yavaş ve daha pahalıdır; bu nedenle ekipler gerçekçilik ile verim arasında denge kurmak zorundadır.
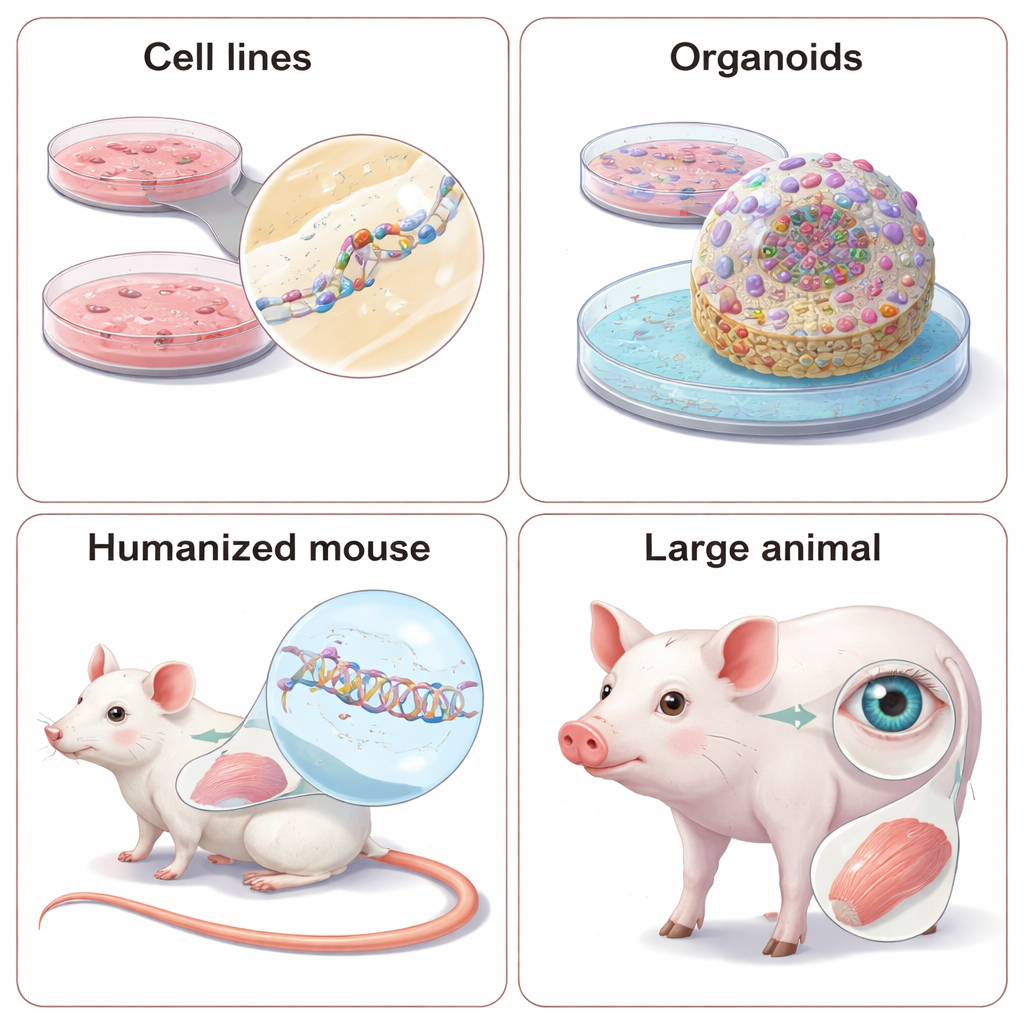
Neden Hayvanlar Hâlâ Önemli—ve Nasıl İnsansılaştırılırlar
Tüm vücut metabolizması, organlar arası etkileşimler veya davranış gibi bazı hastalık özellikleri kaplarda yakalanamaz. Bunun için NAT’ler canlı hayvanlarda test edilir. Bu ilaçlar kesin RNA dizileriyle ilgilendiğinden, bilim insanları iki seçenekle karşılaşır: hayvanın gen versiyonuna uyan “yerine geçen” ilaçlar tasarlamak veya hayvanı insan genetik dizilerini taşıyacak şekilde yeniden mühendislik yapmak. Yerine geçen ASO ve siRNA’lar, iyi kurulmuş fare modellerinde bir genin azaltılmasının semptomları iyileştirip iyileştirmediğini gösterebilir, ancak insan hedefli ilacı mükemmel şekilde taklit etmezler. İnsansı modeller—insan genlerinin bölümlerini veya tüm kopyalarını taşıyan fareler veya hatta mini‑domuzlar—gerçek klinik adayı üzerinde test yapılmasına olanak sağlar, ancak önemli zaman ve maliyet gerektirir ve türler arasındaki gen düzenlemesindeki ince farklılıklar hâlâ sürprizlere yol açabilir. Derleme ayrıca özellikle göz ve kas hastalıklarında anatominin insanlara daha çok benzediği büyük hayvanların kullanımının arttığını vurgular.
İleriye Bakış: Daha Akıllı Modeller ve Daha Az Tahmin
Yazarlar, nükleik asit ilaçlar için tek bir “en iyi” model olmadığını; bunun yerine her projenin hızlı, basit testlerle başlayıp daha karmaşık, insanla daha ilgili sistemlere doğru ilerleyen özel bir yol gerektirdiğini sonucuna varıyorlar. Düzenleyiciler ve fon sağlayıcılar hayvan kullanımını azaltmaya ittikçe, sofistike organoid’ler, organ‑on‑a‑chip cihazları ve bilgisayar modellerinin özellikle hangi dizilerin ve kimyaların en iyi çalışacağını öngören makine öğrenimi araçlarıyla birleştiğinde işin daha fazlasını üstleneceği bekleniyor. Sonuçta, her modelin güçlü ve kör noktalarını anlayarak—ve alandaki en iyi uygulamaları ve verileri paylaşarak—araştırmacılar programlanabilir genetik fikirleri hastalar için güvenli, etkili ilaçlara dönüştürme konusunda daha güvenilir bir yol izleyebilirler.
Atıf: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Anahtar kelimeler: nükleik asit terapileri, antisens oligonükleotitler, siRNA, preklinik modeller, gen terapisi