Clear Sky Science · tr
Tbr2 bağımlı paralel yollar, farklı ipRGC alt tiplerinin gelişimini düzenler
Gözlerimiz Zamanı ve Şekli Nasıl Anlatır
Görüntü oluşturmaktan öte, gözlerimiz sessizce vücut saatimizi düzenler, gözbebeklerimizin açıklığını kontrol eder ve genel parlaklığı algılamamıza yardımcı olur. İntrinsik olarak ışığa duyarlı retinal ganglion hücreleri (ipRGC'ler) adı verilen küçük bir özel retinada bulunan sinir hücresi nüfusu bu işlerin çoğunu üstlenir. Bu hücreler melanopsin adlı bir pigmentle ışığa yanıt verir ve sinyalleri beynin derin bölgelerine gönderir. Bu çalışma temel ama büyük çıkarımları olan bir soruyu sorar: Gelişimin erken bir dönemindeki sinir hücreleri grubu, her biri farklı bir işle bağlı olan birkaç ayrı ipRGC türüne nasıl ayrılır?
Bir Ana Anahtar, Birçok Işık Algılayıcı Hücre Türü
Fare retinasında bilinen altı ipRGC alt tipi, Tbr2 adlı bir geni açan erken bir ganglion hücreleri popülasyonundan köken alır. Bu gen, ipRGC oluşumu için gerekli programları ve melanopsin geninin (Opn4) etkin kalmasını sağlayan bir ana anahtar gibi davranır. Ancak tek bir ana anahtar, benzersiz şekiller, ışık yanıtları ve beyin hedeflerine sahip altı farklı ipRGC çeşidinin nasıl ortaya çıktığını tek başına açıklayamaz. Yazarlar, gelişen fare retina dokularının RNA dizilemesini kullanarak aktivitesi Tbr2'ye bağlı olan genleri aradılar. Küçük bir aday kümesi arasında iki gen öne çıktı: Irx1 ve Tbx20; her ikisi de vücudun diğer bölgelerinde hücre kimliğini düzenleyen bilinen faktörlerdir. 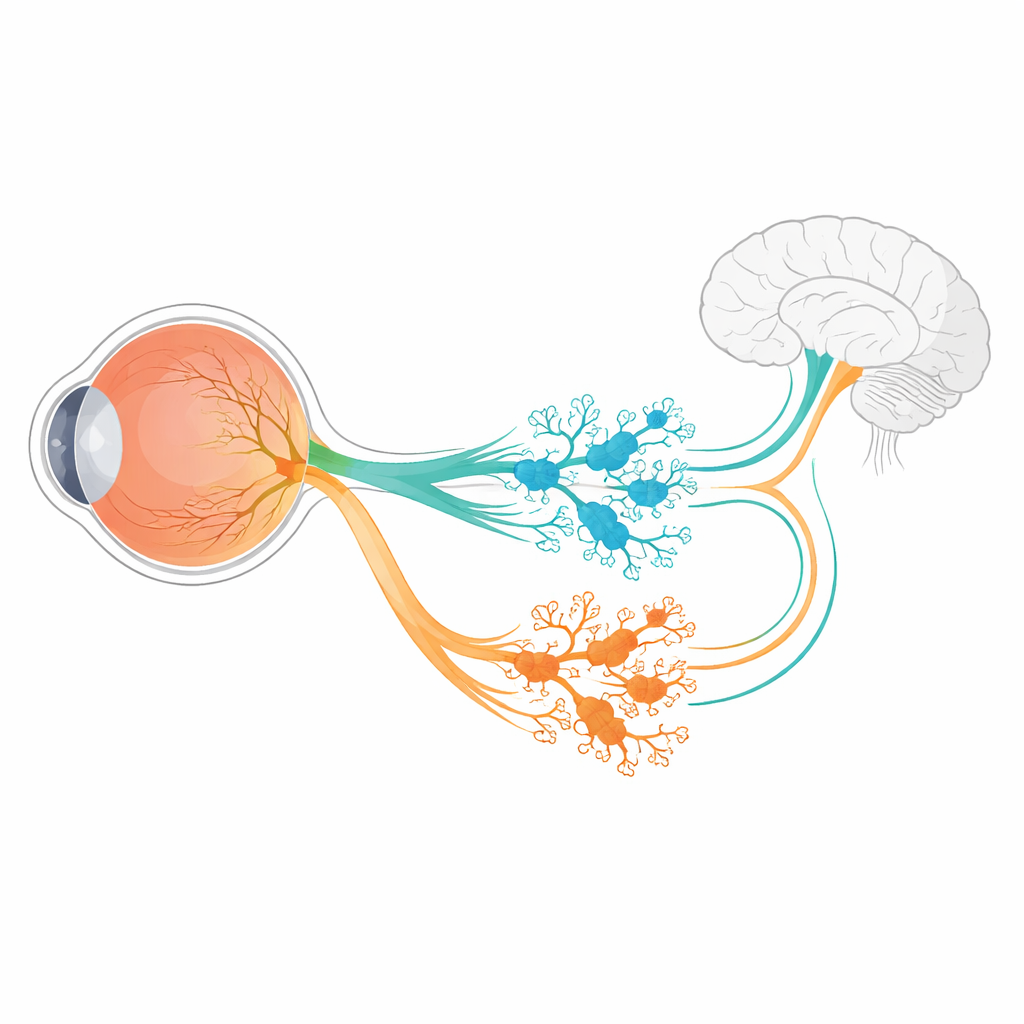
Retinada İki Ayrışan Yol
Irx1 ve Tbx20 üreten hücreleri flüoresan veya enzim belirteçleriyle işaretleyen yeni tasarlanmış fare hatlarını kullanarak araştırmacılar bu faktörlerin nerede ve ne zaman açıldığını izlediler. Irx1 ve Tbx20'nin orta gebelik döneminde genç retinal ganglion hücrelerinin örtüşen gruplarında göründüğünü, ancak erişkinlikte neredeyse tamamen ayrı kümelere ayrıldıklarını buldular. Irx1 ağırlıklı olarak M3, M4 ve M5 etiketli üç ipRGC tipinde bulunurken, Tbx20 M1, M2 ve M6 hücrelerinde yoğunlaşmıştı; bazı M3 ve M5 hücrelerinde ise yalnızca küçük bir örtüşme vardı. Ayrıntılı görüntüleme, elektrik kayıtları ve beyin izleme, her bir faktörün dendritik düzenleri, ışık yanıtları ve zamanlayıcı ayarlama, refleksler ve görsel işlemeyle ilişkili belirli beyin bölgelerine projeksiyon desenleriyle karakterize edilen ayrı bir ipRGC koleksiyonunu işaret ettiğini gösterdi.
Işık Duyarlılığını ve Hücre Hayatta Kalımını Ayarlayan Anahtarlar
Ardından ekip her bir faktör kaldırıldığında ne olduğunu sordu. Gelişen retinada Irx1 yok edildiğinde, Irx1 ile işaretli ipRGC'lerin sayısı ve temel yapısı büyük ölçüde korunmuş, ancak melanopsin düzeyleri keskin şekilde düşmüştü. Başka bir deyişle Irx1, M3, M4 ve M5 hücrelerinde Opn4 ışık algılama programını tam olarak etkinleştirmek için gerekliydi, ancak bu hücrelerin ilk oluşumu için şart değildi. Tbx20 farklı davrandı. Tbx20'nin silinmesi yalnızca Opn4 ekspresyonunu düşürmekle kalmadı, aynı zamanda Tbx20-pozitif ipRGC sayısını yaklaşık yarıya indirdi ve daha sonra bu hücrelerin hayatta kalmasını azalttı. Bu, Tbx20'nin özellikle M1, M2 ve M6 alt tiplerini hem oluşturmasına hem de sürdürmesine yardımcı olduğunu ve aynı zamanda bu hücrelerin melanopsin tabanlı ışık duyarlılığını desteklediğini gösterir. 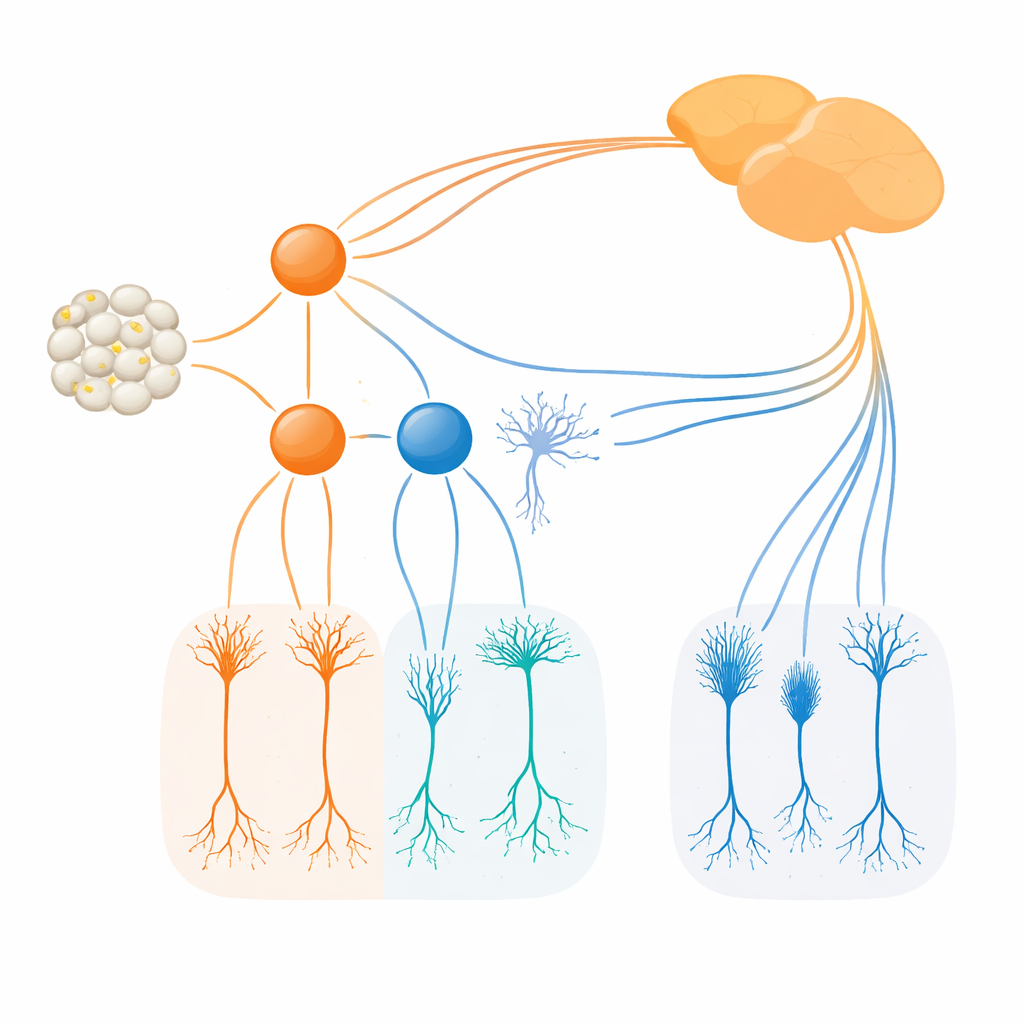
Ayrı Hücre Ailelerine Ayrılmanın Zamanlaması
Yazarlar genetik raporlayıcıları belirli embriyonik günlerde kısa süreli etkinleştirerek Irx1 veya Tbx20 ifade eden hücreleri “zaman damgalayabildiler” ve bunların erişkinlikteki kaderlerini izlediler. Bu deneyler Tbx20 ile işaretli hücrelerin, Irx1 ile işaretli hücrelerden biraz daha erken nihai ipRGC kimliklerine karar verdiklerini ve çoğu kararlılığın doğumdan hemen önce kilitlendiğini gösterdi. Kısa bir pencere içinde bazı hücrelerde hem Irx1 hem de Tbx20 eşzamanlı olarak ifade edilebiliyor ve her iki geni de kaybeden çift mutant fareler, tek mutantlardan çok daha güçlü bir melanopsin-pozitif ipRGC kaybı gösterdi. Bu, iki yolun geçici olarak birlikte çalıştığını, ardından farklı ipRGC alt kümelerini ayrı gelişim yollarına yönlendirmek için ayrıldıklarını öne sürer.
Görme ve Sağlık Anlayışımız İçin Anlamı
Uzman olmayan bir okuyucu için ana mesaj şudur: Tek bir erken gen olan Tbr2 tek başına hareket etmez. Bunun yerine iki paralel kontrol yoluna beslenir; biri Irx1 merkezli, diğeri Tbx20 merkezlidir. Bu yollar genç bir hücrenin hangi ipRGC türüne dönüşeceğine, ışığı ne kadar güçlü algılayacağını ince ayarına ve vücut saati düzenleme, gözbebekleri refleksi veya diğer görsel rollere hizmet eden beyin bölgelerine bağlanıp bağlanmayacağını belirler. Çalışma, içsel “ışık ölçerlerimizin” nasıl inşa edildiğine dair daha net bir devre şeması sunar ve bu hücrelerin kaybı veya işlev bozukluğunda rol oynayabilecek belirli genetik adımları vurgular; bu da uyku bozuklukları, mevsimsel ruh hali değişimleri ve retinayı hasara uğratan hastalıklarla ilgili olası çıkarımlara işaret eder.
Atıf: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
Anahtar kelimeler: retinal ganglion hücreleri, melanopsin, sinirsel gelişim, sirkadiyen ritimler, transkripsiyon faktörleri