Clear Sky Science · tr
PTBP1, Sertoli hücrelerinde mTORC2–PKCα yoluyla sitoskeletal organizasyonu kolaylaştırarak farelerde spermiyogenezi destekler
Bu çalışma erkek kısırlığı açısından neden önemli
Erkek kısırlığı çoğunlukla gizemli görünse de, özünde gelişen spermler ile onlara destek olan “bakıcı” hücreler arasındaki ince ayarlı bir ortaklığa dayanır. Bu çalışma, bu bakıcı hücrelerin içinde yer alan gizli moleküler yardımcılarından birini inceliyor ve onun işlev bozukluğunun sperm üretimini nasıl durdurabileceğini gösteriyor. Bu gizli kontrol katmanını anlamak, belirli erkek kısırlığı formları için yeni tanı veya tedavi yollarına işaret edebilir.
Sperm üretimini mümkün kılan destek hücreleri
Spermler testiste seminifer tübüller adı verilen uzun, kıvrımlı kanallarda üretilir. Bu kanalların iç yüzünü döşeyen Sertoli hücreleri, gelişen germ hücrelerini sarıp besleyen ve bölünerek olgunlaşıp sperme dönüşürken onları yönlendiren özel bir destek hücre türüdür. Sertoli hücreleri ayrıca erken evre hücreleri bağışıklık sisteminden ayıran kan–testis bariyerini oluşturur. Tüm bunları yapmak için, tübüller boyunca hareket eden germ hücre dalgalarıyla sürekli yeniden düzenlenen aktin filamentleri ve mikrotübüllerden oluşan içsel bir iskelete güvenirler. Bu iskelet bozulursa bariyer sızdırır ve olgunlaşan germ hücreleri kopabilir veya ölebilir; bu da üremeyi tehlikeye atar.
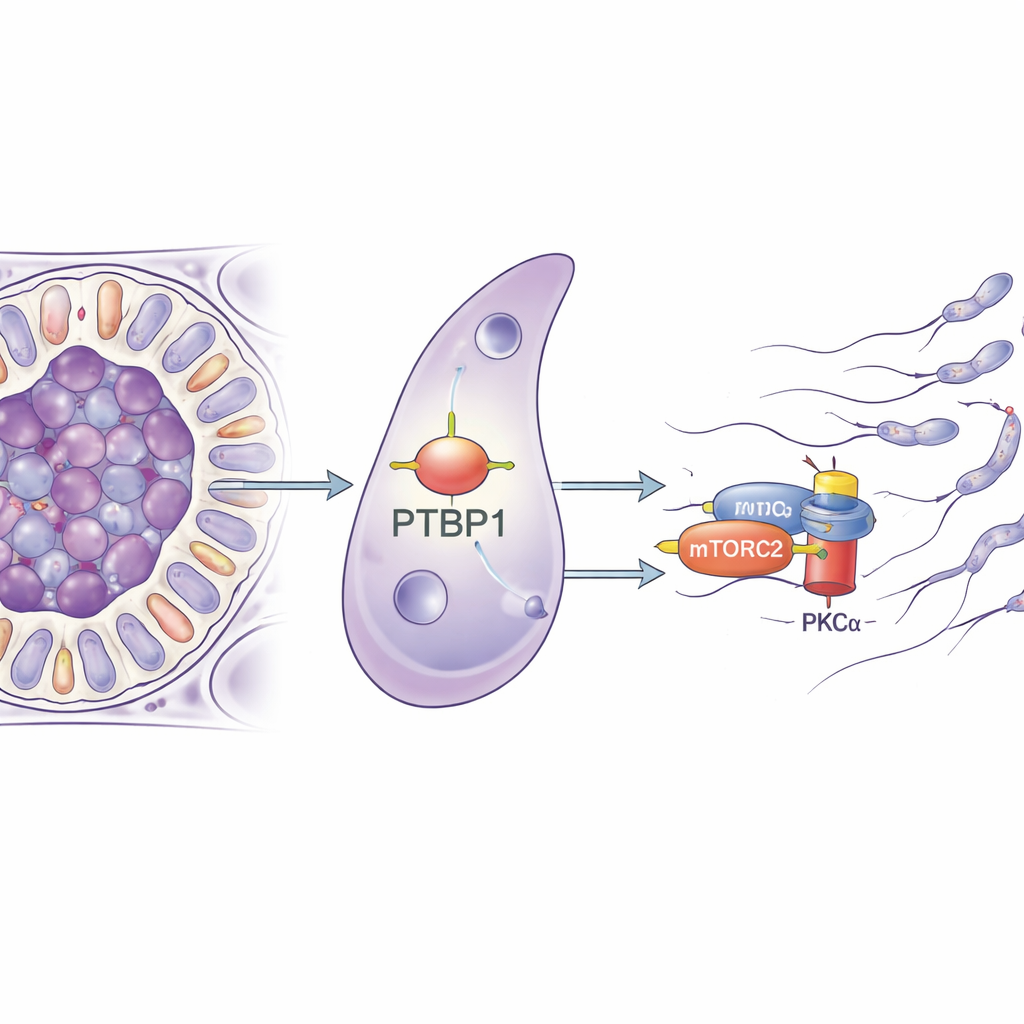
Küçük ama önemli bir RNA yöneticisi
Araştırmacılar, hücre içindeki RNA moleküllerini yönetmedeki rolüyle tanınan PTBP1 adlı bir proteine odaklandı—genlerin nasıl sentezlendiği, mesajlarının ne kadar kararlı olduğu ve ne kadar verimli proteine dönüştürüldükleri üzerinde etkisi vardır. PTBP1 hem germ hücrelerinde hem de Sertoli hücrelerinde bol bulunur ve önceki çalışmalar, onu germ hücrelerinden kaldırmanın sperm üretimini aksattığını göstermişti. Bu çalışmada ekip, farelerde PTBP1’i yalnızca Sertoli hücrelerinden sildi. İlk bakışta genç fareler normal görünse de cinsel olgunluğa erişince testisleri küçüldü, epididimisteki sperm sayısı düşüş gösterdi ve erkeklerin hiçbiri yavru sahibi olamadı; bu da tamamen kaybolmuş bir üreme yeteneğini ortaya koydu.
Hücresel iskelet çöktüğünde
Bu farelerin testislerinin mikroskobik incelemesi, spermatogenezin yarıda takıldığını gösterdi. Birçok tübül boşluklar içeriyor, anormal şekilde füzyona uğramış germ hücre çekirdekleri kümeleri ve tam uzamış sperm eksikliği gözleniyordu. Normalde tübüllerin dış duvarına yaslanan Sertoli hücre çekirdekleri sık sık merkeze doğru kaymıştı; bu durum bu destek hücrelerinin çevreye tutunma yetisini kaybettiğine işaret ediyordu. Temel bağlantı bileşenleri ve yapı proteinleri için yapılan boyamalar, kan–testis bariyerinin zayıfladığını ve tipik sıkı aktin demetlerinin tübülün tabanından merkezine uzanan düzensiz, aşırı yoğun tellerle yer değiştirdiğini doğruladı. Normalde bariyerin “kan tarafında” kalan bir izleyici molekül, bunun yerine tübüllerin derinliklerine sızdı; bu da bariyerın çöküşünü doğrudan gösteriyordu.
Başarısızlığı bir sinyal merkezine kadar izlemek
Bir RNA-bağlayıcı proteinin böyle mekanik sorunlara nasıl yol açtığını anlamak için ekip, Sertoli hücrelerini saflaştırdı ve PTBP1 eksik olduğunda hangi genlerin etkinliğinin değiştiğini analiz etti. Etkilenen genlerin birçoğu hücrenin iskeletini kontrol etmekle ve hücrelerin birbirine nasıl yapıştığıyla ilgiliydi; bu, geniş kapsamlı bir yeniden düzenleme bozukluğuna işaret ediyordu. Ardından araştırmacılar PTBP1’e fiziksel olarak bağlanan RNA moleküllerini çekti ve bunun mTORC2 adlı bir sinyal kompleksinin çekirdek parçası olan Rictor’un mesajına tutunduğunu buldular. Bu kompleks, sırayla aktin filamentlerini şekillendiren PKCα adlı bir enzimi aktive eder. PTBP1 eksik Sertoli hücrelerinde RICTOR proteini azaldı ve PKCα çok daha az aktifti; oysa Rictor için temel RNA düzeyi neredeyse değişmemişti. Bu, PTBP1’in Sertoli hücrelerinin RICTOR proteinini RNA mesajından yeterince üretmesine yardımcı olarak mTORC2–PKCα yolunun çalışmasını sürdürdüğünü kuvvetle düşündürüyor.
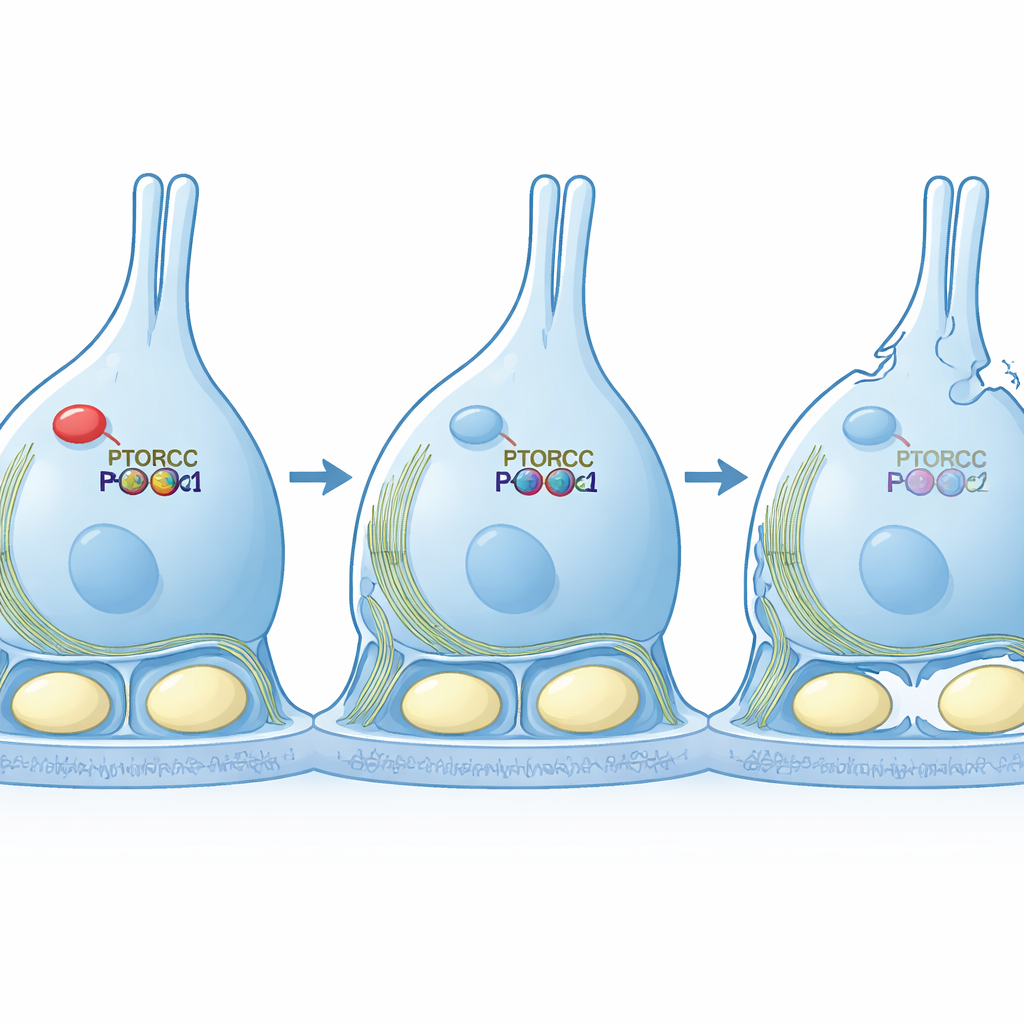
Sinyali geri getirerek iskelaeti kurtarmak
Ekip daha sonra nedenselliği test etmek için hücre kültürü modellerine geçti. Bir Sertoli benzeri hücre hattında PTBP1’i azalttıklarında, hücreler uzun ince şekillere uzandı ve düzensiz bir aktin ağı sergiledi—zayıflamış mTORC2 sinyallemesinin belirtisi. Önemli olarak, bu hücrelere sürekli etkin bir PKCα versiyonu ürettirildiğinde, hücreler normal, kompakt şekillerini ve daha düzenli aktin yapılarını geri kazandı; RICTOR hâlâ düşük olsa bile. Bu kurtarma deneyi, bu bağlamda PTBP1’in esas görevinin hücrenin iç iskeletini düzenlemek için mTORC2–PKCα yolunu yeterince güçlü tutmak olduğunu gösteriyor.
Kısırlığı anlamak açısından ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma testiste bir bağımlılık zincirini ortaya koyuyor: PTBP1 Sertoli hücrelerinin önemli bir sinyal merkezini kurmasına yardımcı olur; bu merkez iç iskeletlerini düzenler; sağlam bir iskelet de gelişen spermlere tutunup onları korumalarını sağlar. Zinciri PTBP1’de kırarsanız, Sertoli hücreleri yapısını kaybeder, koruyucu bariyer çöker ve sperm gelişimi çökerek erkek kısırlığına yol açar. Bu araştırma farelerde yapılmış olsa da aynı moleküller insanlarda da mevcut; bu da Sertoli hücrelerinde RNA kontrolündeki ince kusurların açıklanamayan bazı erkek kısırlığı vakalarının altında yatan neden olabileceği olasılığını gündeme getiriyor ve gelecekte çalışılacak yeni moleküler hedefler sunuyor.
Atıf: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
Anahtar kelimeler: erkek üreme yeteneği, Sertoli hücreleri, spermatogenez, sitoskeleton, RNA-bağlayıcı proteinler