Clear Sky Science · tr
Endoteliyal TRIM47, farelerde KEAP1/NRF2 sinyal yoluyla kan-beyin bariyerinin bütünlüğünü ve bilişi düzenler
Neden küçük beyin damarlarını korumak önemli
Serebral küçük damar hastalığı, beyinde sessiz bir bozucu unsurdur. En küçük kan damarlarını zedeler, inme riskini artırır ve hafıza ile düşünmeyi yavaşça aşındırır; buna karşın doktorların hastalığın kökensel biyolojik nedenlerine yönelik etkili tedavileri hâlâ sınırlıdır. Bu çalışma, beyin kan damarlarının içini döşeyen hücrelerde bulunan TRIM47 adlı belirli bir proteini inceledi ve basit ama kritik bir soruyu gündeme getirdi: Bu protein kan–beyin bariyerinin bütünlüğünü korumaya yardımcı oluyor mu ve bunun biliş için önemi nedir?
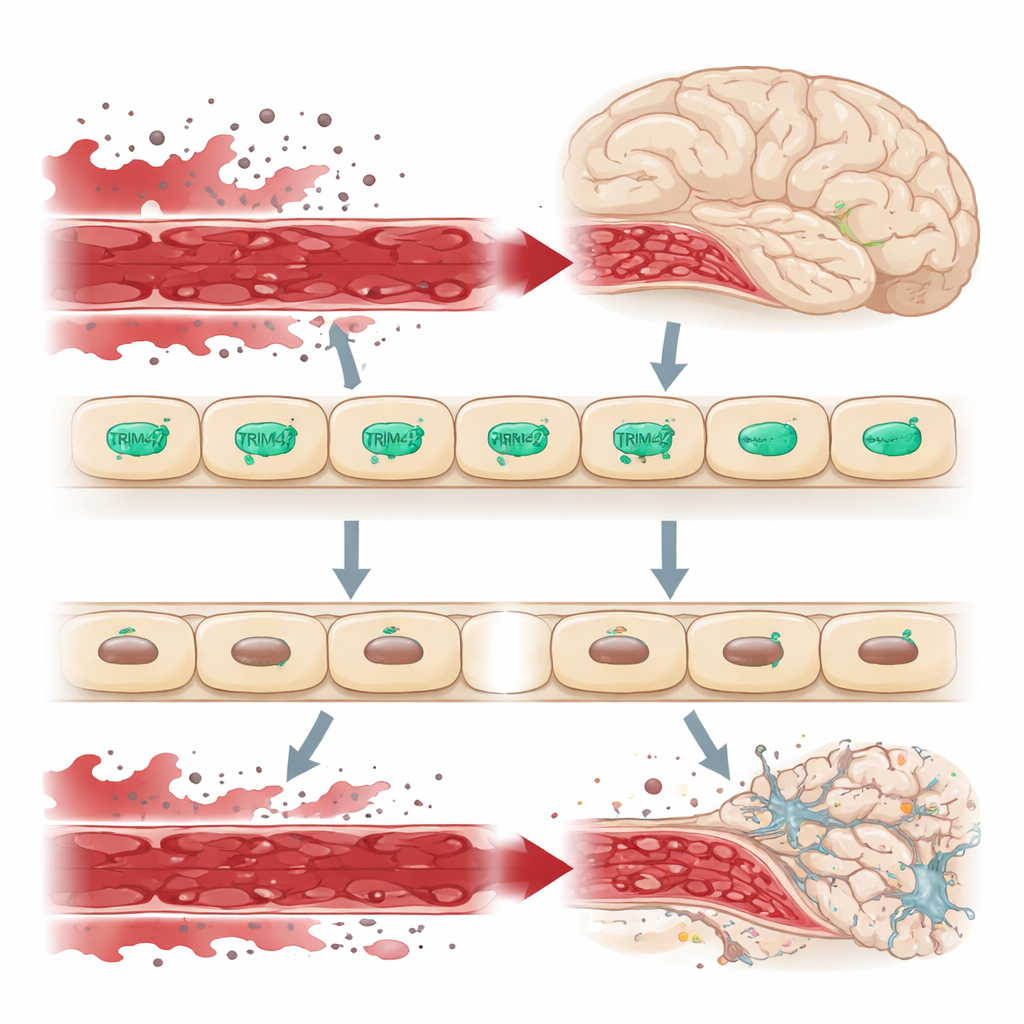
Beynin sınırındaki bir bekçi
Beyin, kan–beyin bariyeri tarafından vücudun dolaşımından korunur; bu bariyer, beyin dokusuna nelerin girebileceğini sıkı biçimde kontrol eden sıkı kapalı bir endotel hücre dizisidir. Bu bariyer sızdığında, kandan gelen zararlı moleküller beyne sızar, nöronları ve destek hücrelerini zorlar ve demans gibi durumlara katkıda bulunur. Büyük insan popülasyonlarında yapılan genetik çalışmalar, TRIM47 genini içeren bir DNA bölgesinin serebral küçük damar hastalığı için risk bölgesi olabileceğini işaret etmişti. TRIM47 özellikle beyin endotel hücrelerinde aktiftir; bu da onun bu bariyerin önemli bir koruyucusu olabileceğine dair ipucu verir.
TRIM47’nin hücreleri oksidatif strese karşı nasıl donattığı
Yazarlar önce laboratuvarda büyütülen insan beyin endotel hücrelerini inceleyip RNA interferansı kullanarak TRIM47 düzeylerini azalttılar. Bu, gen aktivitesinde geniş çaplı değişiklikleri tetikledi ve en çok etkilenen ağ NRF2 çevresinde yoğunlaştı; NRF2, hücrenin antioksidan savunmalarının baş düzenleyicisidir. Normal koşullarda NRF2, KEAP1 adlı başka bir protein tarafından kontrol altında tutulur; KEAP1 NRF2’yi yıkıma yönlendirir. Ekip, TRIM47’nin KEAP1 ile bağlandığını ve NRF2’nin parçalanmasını engellemeye yardımcı olduğunu gösterdi. TRIM47 bulunduğunda NRF2 birikir, çekirdeğe geçer ve reaktif oksijen türlerini detoksifiye eden genleri açar. TRIM47 kaybolduğunda NRF2 seviyeleri düşer, antioksidan genler daha az aktif olur ve endotel hücreleri oksidatif strese karşı daha savunmasız hale gelir.
Sızan damarlardan farelerde hafıza sorunlarına
Bu mekanizmanın canlı bir beyinde nasıl işlediğini görmek için araştırmacılar tüm vücutta Trim47 geninden yoksun fareler ve yalnızca endotel hücrelerinde Trim47’nin silinebildiği bir başka hat ürettiler. Her iki modelin erişkin hayvanlarında mekânsal öğrenme ve hafıza alanında belirgin sorunlar gelişti; hareketleri normal olmasına rağmen Y-labirent ve Morris su labirenti gibi görevlerde başarısız oldular. Beyinleri incelendiğinde kan–beyin bariyerinin sızdığı görüldü: küçük floresan izleyiciler ve kan proteinleri damarlardan çevre dokuya kaçmıştı. Endotel hücreleri arasında sıkı ve adezin bağlantıları oluşturan belirgin “mühür” proteinleri, özellikle Claudin-5 ve Occludin azalmıştı. Yakınlardaki astroglia (yıldız biçimli destek hücreleri) hızla aktive olmuştu; buna karşın bu aşamada geniş çaplı inflamasyon veya nöron kaybı belirtileri çok azdı.
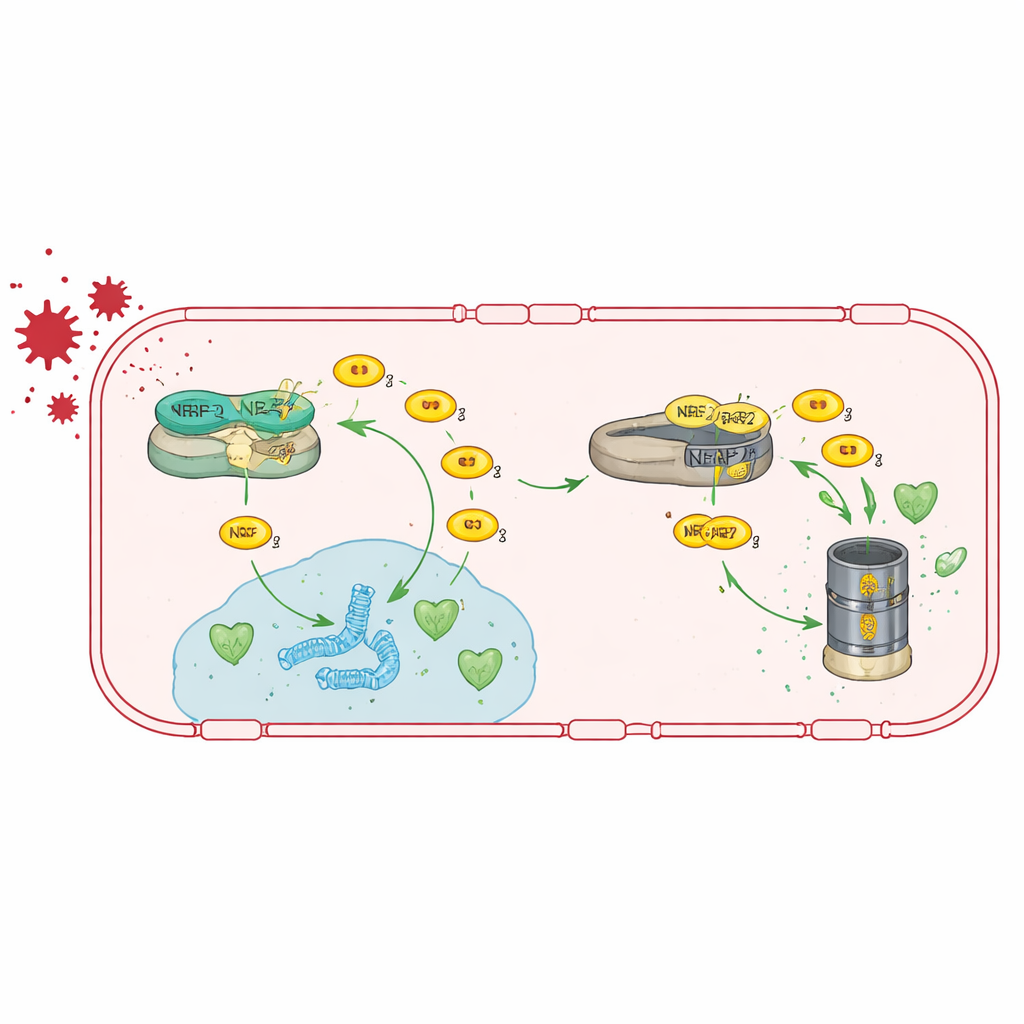
Antioksidan yolu yeniden açmak
TRIM47’nin esas olarak NRF2 aktivitesini güçlendirerek çalışması nedeniyle ekip, kaybını doğrudan NRF2’yi uyararak atlayıp atlayamayacaklarını test etti. Trim47 eksik farelere, NRF2’yi stabilize ettiği ve hedef genlerini açtığı bilinen tert-butilhidrokinon (tBHQ) içeren bir diyet verildi. Bu tedavi beyin endotel hücrelerinde antioksidan gen aktivitesini geri getirdi, sıkı bağlantı genlerinin ekspresyonunu normale yaklaştırdı ve kan–beyin bariyeri sızıntısını azalttı. Etkileyici biçimde, astroglia aktivasyonu da normalleşti ve hayvanların hafıza testlerindeki performansı kurtarıldı; bu, bu antioksidan yolun güçlendirilmesinin en azından farelerde vasküler ve bilişsel sorunları tersine çevirebileceğini gösteriyor.
İnsandan alınan kan ipuçları ve izlenecek yollar
Fare deneylerini insan hastalığıyla bağlamak için araştırmacılar, beyin MR görüntüleri olan binlerce kişinin kan örneklerinde NRF2 yoluyla ilişkili proteinleri analiz ettiler. Birkaç NRF2 düzenlemeli proteinin düzeyleri, perivasküler boşlukların genişlemesi ve beyaz cevher değişiklikleri gibi küçük damar hastalığının görüntüleme belirteçleriyle ilişkili bulundu. Bu, değişmiş TRIM47–NRF2 sinyalinin yalnızca deneysel hayvanlarda değil, insanlarda da anlamlı olabileceğini ve bu proteinlerin hastalık şiddeti veya ilerlemesinin biyobelirteçleri olarak hizmet edebileceğini destekliyor.
Beyin sağlığı için bunun anlamı
Birlikte ele alındığında bu çalışma, TRIM47’yi NRF2 antioksidan sistemini stabilize ederek beyin kan damarlarının oksidatif hasara dayanmasına yardımcı olan moleküler bir koruyucu olarak tanımlıyor. TRIM47 eksik veya işlevsiz olduğunda kan–beyin bariyeri zayıflar, ince beyin hasarı birikir ve hafıza bozulmaya başlar. NRF2 yolunu yeniden etkinleştirmek, farelerde bariyeri onarabilir ve bilişi geri getirebilir; bu sinyal eksenini vasküler demans türleri için umut vadeden bir terapötik hedef olarak öne çıkarır. tBHQ’nin kendisi insanlar için uygun bir ilaç olmasa da, daha güvenli NRF2 artırıcı bileşikler veya TRIM47’nin koruyucu rolunu taklit eden stratejiler bir gün en küçük, en kırılgan damarları güçlendirerek beyin sağlığını korumaya yardımcı olabilir.
Atıf: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Anahtar kelimeler: serebral küçük damar hastalığı, kan–beyin bariyeri, TRIM47, NRF2 yolu, vasküler demans