Clear Sky Science · tr
HCN2 kanalında siklik nükleotidlerin entropik olarak yönlendirilen ve negatif kooperatif bağlanması için altüniteler arası bir yol gereklidir
Kalbin küçük pacemaker anahtarları kimyasal sinyalleri nasıl algılıyor
Her kalp atışı ve birçok beyin ritmi, hücre zarlarımızdaki açılıp kapanan mikroskobik kanallara dayanır. HCN pacemaker kanalları olarak adlandırılan bu kanallar yalnızca elektriksel voltajla değil aynı zamanda siklik nükleotidler olarak bilinen küçük haberci moleküller tarafından da kontrol edilir. Bu çalışma, görünüşte basit ama sonuçları geniş olan bir soruyu ortaya koyuyor: bu küçük moleküller HCN2 kanalına nasıl koordineli şekilde bağlanır ve bu süreçteki ince hatalar epilepsi gibi bozukluklara nasıl katkıda bulunabilir?
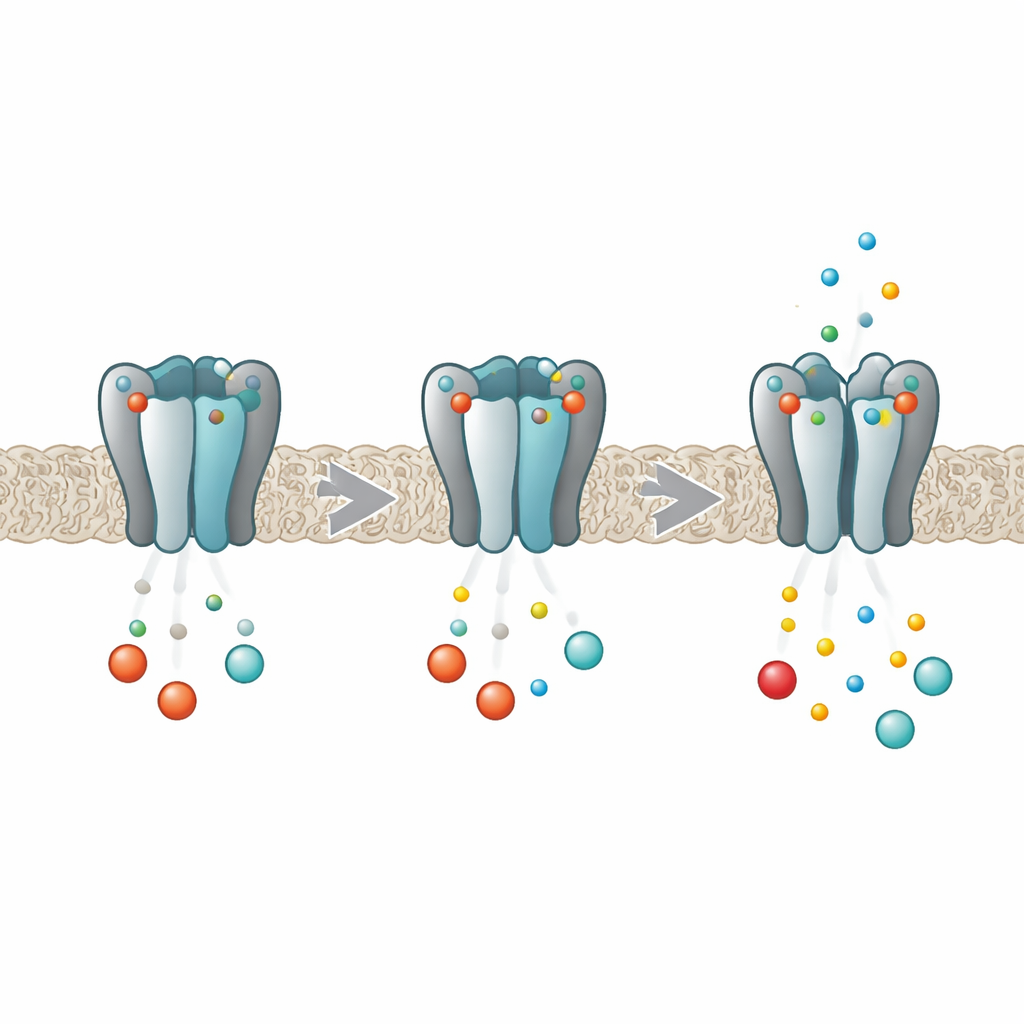
Vücudun ritimleri için moleküler bir karartıcı
HCN kanalları kalp ve beyin hücrelerindeki elektriksel aktivite için bir tür karartıcı anahtar görevi görür. Her kanal, birlikte iyonların aktığı merkezi bir gözenek oluşturan dört özdeş protein altünitesinden oluşur. Her altünitede, cAMP ve cGMP gibi siklik nükleotidleri yakalayabilen bir cep bulunur. Bu haberciler bağlandığında gözenek açılmasını kolaylaştırır ve pacemaker akımını artırır. Önceki çalışmalar, HCN2 varyantında bağlanmanın her cepte bağımsız olarak gerçekleşmediğini; bunun yerine dört sitenin birbirini etkilediğini, ilk molekülün daha kolay bağlandığı ve sonraki moleküllerin bağlanmasının daha güçleştiği — negatif kooperativite olarak bilinen bir davranış sergilendiğini göstermişti. Yeni çalışma, dört altünitenin bu süreç sırasında birbirleriyle tam olarak nasıl iletişim kurduğunu ortaya çıkarmayı amaçladı.
Komşularını hisseden altüniteler
Araştırmacılar HCN2 kanalının izole parçaları üzerinde laboratuvar ölçümlerini bilgisayar simülasyonlarıyla birleştirdi. Uzun moleküler dinamik simülasyonlar kullanarak, kanalın kuyruk bölgesinin — siklik nükleotid ceplerini ve gözenekle bağlantı kuran C-bağlayıcı (C-linker) kısmını içeren bölümün — farklı sayıda cAMP veya cGMP bağlıyken nasıl esnediğini ve sallandığını izlediler. Bir haberci bir altüniteye kilitlendiğinde sadece o altüniteyi stabilize etmediğini gördüler. Bunun yerine, komşularının kararlılığını ince bir şekilde değiştirdi; bazen onları daha sert, bazen daha esnek hale getirdi; oysa genel protein şekli neredeyse hiç değişmedi. Bu komşudan-komşuya etkiler, kaç sitenin dolu olduğuna ve bu sitelerin halka etrafındaki konumlarına bağlıydı ve negatif kooperativiteden beklenenle uyumluydu.
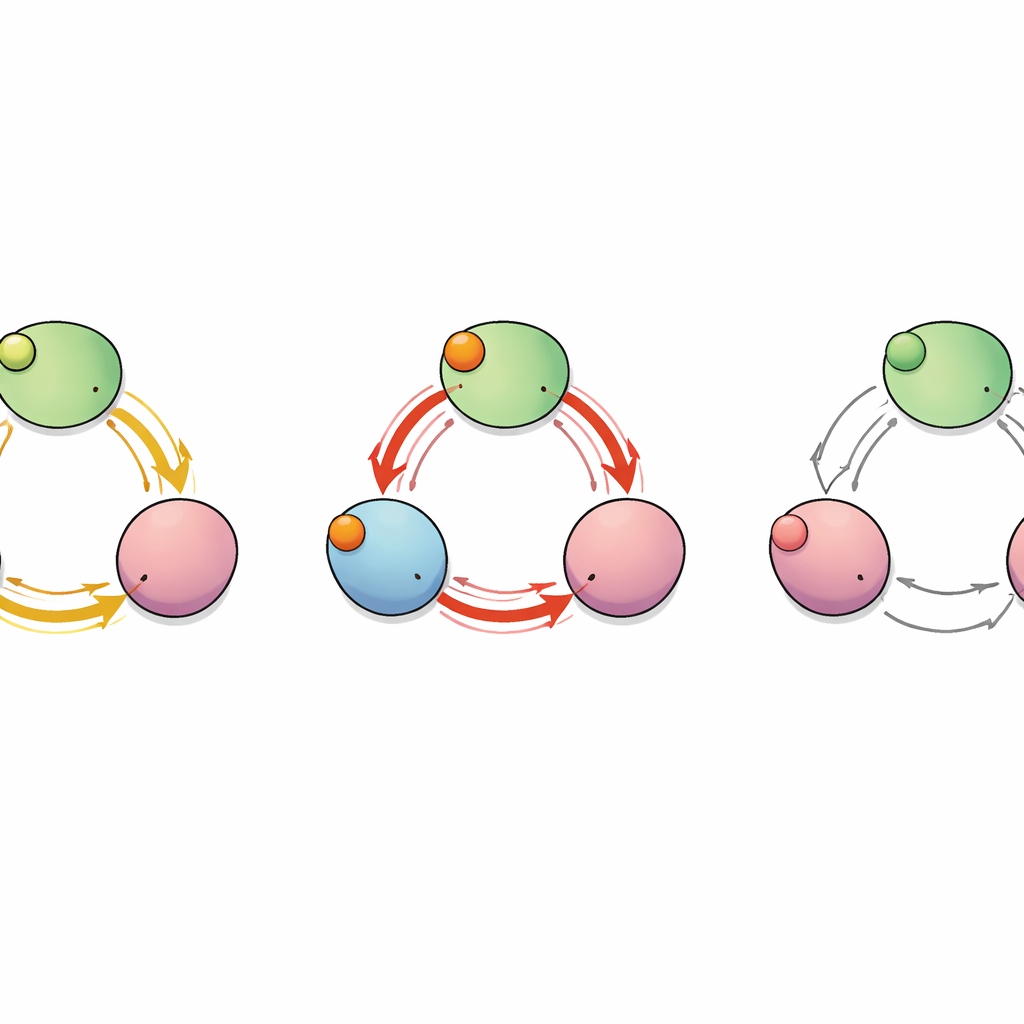
Altüniteler arasında gizli bir yol
Bağlanma “sinyalinin” proteinin içinde nasıl yayıldığını haritalamak için ekip kanalı etkileşen amino asitlerden oluşan bir ağ olarak ele aldı. Simülasyonlar sırasında hangi kalıntıların eşgüdümlü hareket ettiğini hesapladılar ve bağlanma ceplerinden gözeneci kontrol eden C-linker segmentlerine en kısa ve en verimli iletişim yollarını belirlemek için grafik kuramı araçlarını kullandılar. Bu analiz birkaç olası güzergâh ortaya çıkardı, ancak iki tanesi öne çıktı: biri tek bir altünite içinde kalan yol, diğeri ise bir altüniteden komşusuna atlayan yol. Bu altüniteler arası güzergâhta, 488. pozisyondaki glutamat (E488) adlı tek bir kalıntı, birçok en kısa yolun geçtiği kritik bir merkez olarak davrandı; bu da onun kooperatif bağlanma için kilit bir röle noktası olabileceğini düşündürdü.
Sohbeti bozan mutasyonlar
Yazarlar ardından bu yolun önemini test etmek için saflaştırılmış kanal kuyruklarıyla deneylere yöneldiler. Yolu alan E488'i ve yolun ulaştığı komşu altünitede yer alan tirosin 459 (Y459) çevresini değiştirdiler. Dinamik ışık saçılması kullanarak mutant proteinlerin hâlâ dört altünite kompleksleri oluşturduğunu doğruladılar, ancak normal proteinde görülen ligand kaynaklı altüniteler arası sıkışma artık yoktu. Bağlanmanın küçük ısılarını izleyen izotermal titrasyon kalorimetrisi, daha da büyük bir değişiklik ortaya koydu: vahşi tip HCN2, esas olarak entropideki artışla (içsel hareketliliğin artması) yönlendirilen yüksek afiniteli bir adımı izleyen iki ayrı bağlanma olayı gösterirken, ardından üç daha düşük afiniteli adım geliyordu. Buna karşılık E488 veya Y459 mutantları sadece bu elverişli entropik artışı göstermeyen tek, ılımlı afiniteli bir bağlanma modu sergiledi ve karakteristik negatif kooperativiteyi kaybetti.
Neden ince entropi değişiklikleri önemli
Bu parçaları birleştirdiğinizde, çalışma HCN2 kanalını belirli “konuşma yolları” ile birbirine bağlı dinamik bir dört altünite halkası olarak resmediyor. İlk siklik nükleotid bağlandığında, E488 ve Y459 aracılığıyla halkanın uzak kısımlarının hareketlerini incelikle değiştirir; bu da sonraki bağlanma olaylarını daha az elverişli kılar ve gözenek tepkisini ayarlar. Bu etki büyük yapısal yeniden düzenlemelerle değil, içsel esneklikteki — statik fotoğraflarda görünmeyen ancak işlev için kritik olan — entropi değişimleriyle yönlendirilir. Bu altüniteler arası yol boyunca kilit kalıntıları bozan mutasyonlar konuşmayı susturur, negatif kooperativiteyi ortadan kaldırır ve idiyopatik jeneralize epilepsi gibi hastalıklarla ilişkilidir. Genel okuyucu için çıkarım şudur: kalp ve beyindeki yaşam için kritik anahtarlar protein altüniteleri arasındaki son derece uyumlu moleküler “fısıltılara” dayanır ve bu fısıltıları anlamak normal ritimleri ve bozulduklarında neler olduğunu açıklamaya yardımcı olur.
Atıf: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Anahtar kelimeler: HCN2 iyon kanalı, siklik nükleotid bağlanması, negatif kooperativite, allosterik iletişim, epilepsi mutasyonu