Clear Sky Science · tr
Küçük bir molekül, SecA bağımlı salgıyı allosterik olarak aktive eder
Bakterilerin Yükleme Rıhtımını Aşırı Hıza Almak
Bakteriler, zarlarındaki küçük geçitler aracılığıyla sürekli olarak proteinler ihraç ederek hayatta kalır. Bu ihracatlar, hücre duvarı oluşturma, toksin salgılama ve strese uyum sağlama gibi, birçok enfeksiyonun merkezinde yer alan süreçlere hizmet eder. Bu çalışma, HSI#6 adında küçük bir kimyasalın sıra dışı bir etki yaptığını bildiriyor: bu molekül, ihracat makinesini engellemek yerine onu hiperaraktif, daha az seçici bir moda geçiriyor. Bu anahtarın nasıl çalıştığını anlamak hem yeni antibakteriyel stratejiler ortaya koyabilir hem de biyoteknolojiye talep üzerine protein salgısını artırma yolu sunabilir.
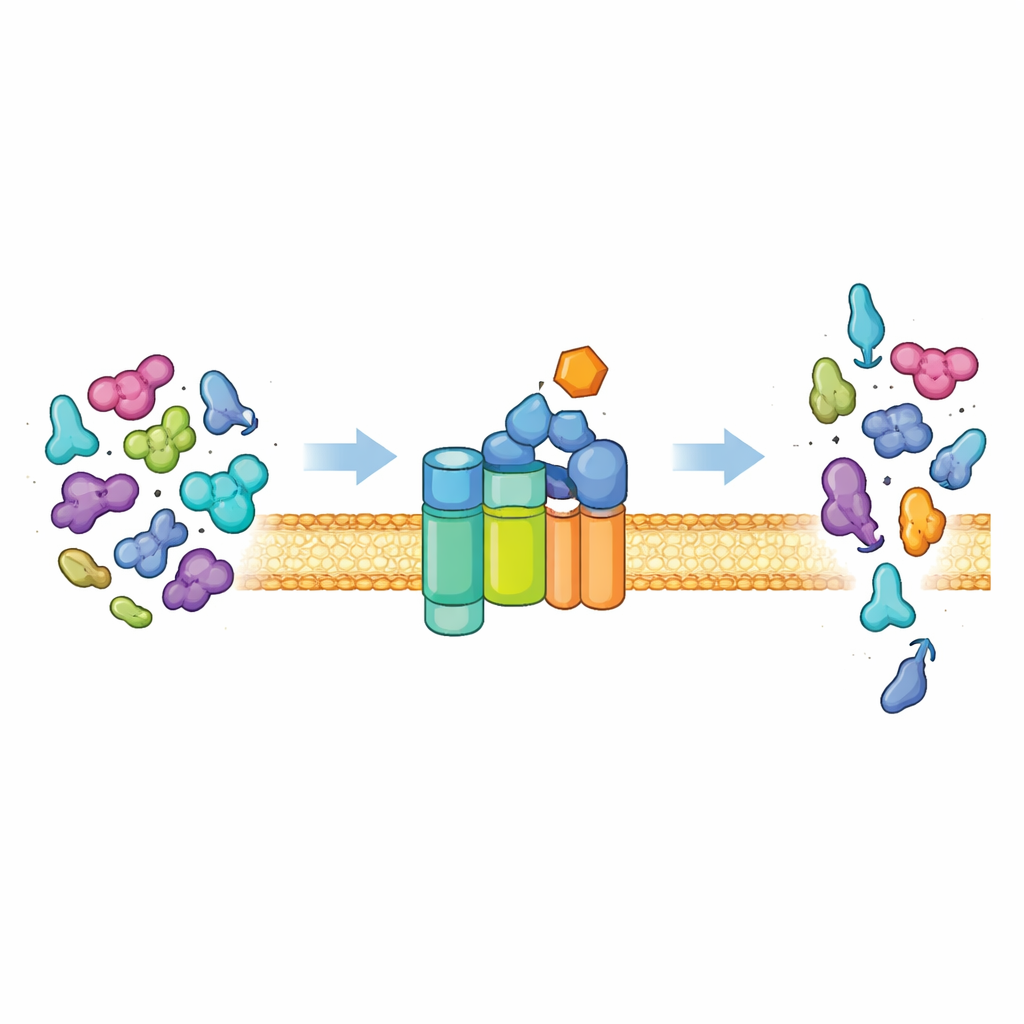
Hücrenin Protein Çıkış Kapısı
Çoğu bakteri, proteinleri hücre dışına taşımak için Sec sistemi olarak bilinen evrensel bir yol kullanır. Bunun özünde bir membran kanalı (SecYEG) ve açılmamış protein zincirlerini kanaldan itmek için hücresel yakıt (ATP) kullanan bir motor proteini (SecA) bulunur. Normal koşullarda bu sistem seçicidir. Öncelikle sinyal peptitleri olarak bilinen özel adres etiketleri taşıyan “preproteinleri” ve ayrıca ana gövdelerinde ek özellikleri ihraç eder. Bu özellikler, SecA’yı sessiz, düşük aktiviteli bir halden güçlü bir motora geçirmek için gereklidir. Sadece doğru sinyal kombinasyonunu sunan proteinler tam aktivasyonu açabilir, böylece hücre doğru yükü dışarı gönderir ve sıradan sitoplazmik proteinleri içeride güvenli tutar.
Motoru Uyandıran Küçük Bir Molekül
Araştırmacılar, bakteriyel protein salgısını ve büyümeyi etkileyen bileşikleri tararken HSI#6’yı keşfettiler. Biyokimyasal testler, HSI#6’nın SecA’ya mikromolar kuvvette doğrudan bağlandığını ve ATP kullanım verimliliğini değiştirdiğini gösterdi. Çözelti içinde HSI#6, SecA’nın ATP’yi daha sıkı tutmasını sağlıyor; SecA kanalına bağlıyken HSI#6 hem ATP bağlanmasını iyileştiriyor hem de ATP dönüşümünü hızlandırıyor. Bu desen, bir yerde bağlanıp başka, uzak bir yerde aktiviteyi değiştiren bir molekülün işareti olan allosterik bir aktive edicinin ayırt edici özelliğidir. Doğal protein müşterilerinin aksine HSI#6, motoru uyarmak için bir yük rolü üstlenmek zorunda değil—sadece SecA’nın iç dinamiklerini ayarlayarak tüm translokazı katalitik olarak hazırlıyor.
Seçici Filtreden Gelişigüzel Nanomakineye
HSI#6 bağlandığında, Sec sistemi artık olağan ihracat etiketleri üzerinde ısrar etmiyor. Deney tüpü deneylerinde bileşik, standart bir preproteinin salgılanmasını yaklaşık iki kat artırdı ve kompleksi bilinen bir SecA inhibitörü olan sodyum azide karşı daha dirençli hale getirdi. Daha dikkat çekeni, HSI#6’nın normal, “vahşi tip” makineye sinyal peptidi tamamen eksik olan proteinleri ve normalde sitoplazmada bulunan proteinleri hareket ettirme olanağı sağlamasıydı. Canlı bakteri hücrelerinde aynı etki alkalin fosfataz tabanlı raporlayıcılarla gözlendi: sitoplazmik proteinler sekresyona uygun bir enzimle füzyonlandığında HSI#6 varlığı, üretilen protein miktarını değiştirmeden salgılanan aktivitede keskin bir artışa neden oldu. Başka bir deyişle, HSI#6 ihracatı olağan müşteri kimliği kontrollerinden fiilen ayırıyor ve Sec sistemini yeterince açığa çıkmış herhangi bir protein için geniş kapsamlı bir dışa aktarma pompasına çeviriyor.
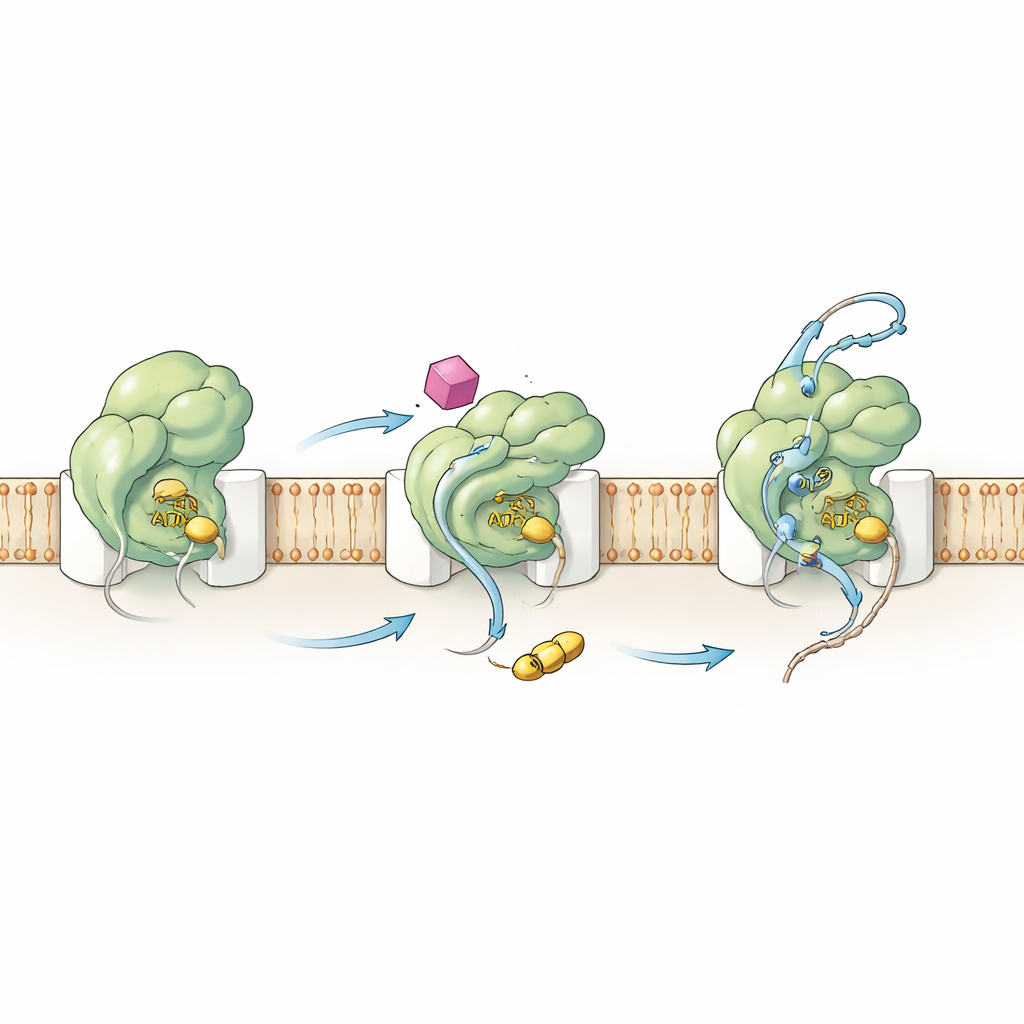
Motoru İçten Yeniden Kabllandırmak
HSI#6’nın bu davranışı nasıl tetiklediğini anlamak için ekip hem SecA’nın kimyasını hem de hareketlerini inceledi. Kinetik ölçümler, bileşiğin anahtar aktivasyon adımını yukarı kaydırdığını gösterdi: SecA–kanal kompleksi, bir protein müşteri bağlanmadan önce bile katalitik olarak aktif hale geliyor. HSI#6 ayrıca SecA’nın harcanmış yakıtı (ADP) bırakmasına yardımcı oluyor; bu normalde yavaş, hız sınırlayıcı bir adım ve böylece daha hızlı ATP döngüsünü destekliyor. Hidrojen–deuteryum değişim kütle spektrometrisi kullanılarak yazarlar HSI#6’nın SecA’nın farklı bölgelerinin esnekliğini nasıl yeniden şekillendirdiğini haritaladılar. Bileşik, müşterileri algılayan ve kanala bağlanan bölgeleri seçici olarak gevşetirken, muhtemelen bağlanma bölgesine ev sahipliği yapan iskelet bölgeyi katılaştırıyor. Ortaya çıkan hareket deseni, zaten devreye girmiş bir translokazın “açık” durumunu andırıyor; bu da HSI#6’nın etkinleşmiş bir formu stabilize ettiğini—muhtemelen kanalına bağlı monomerik bir SecA’yı bile tercih ederek—mümkün kıldığını düşündürüyor, tüm bunlar herhangi bir müşteri bulunmadan gerçekleşiyor.
Tıp ve Biyoteknoloji İçin Neden Önemli
Küçük bir molekülün SecA’yı allosterik olarak aktive edebildiğini ve normal müşteri seçiciliğini ortadan kaldırabildiğini göstererek bu çalışma, merkezi bir bakteriyel makineyi kontrol etmenin yeni bir yolunu ortaya koyuyor. Enfeksiyon hastalıkları açısından, böyle zorlanmış, kontrolsüz salgı patojenleri enerji bakımından zayıflatabilir ve hassas şekilde ayarlanmış dışa aktarma programlarını bozarak HSI#6 benzeri aktive edicileri antibiyotik tasarımı için çekici başlangıç noktaları haline getirebilir—veya aynı düzenleyici özellikleri bloke eden gelecekteki inhibitörlerin tasarımına rehberlik edebilir. Biyoteknoloji için ise aynı prensip, mühendislikli sinyal peptitlerine veya karmaşık genetik düzenlemelere gerek kalmadan yararlı rekombinant proteinlerin salgılanmasını artırmak amacıyla yeniden kullanılabilir. Özetle, çalışma bakteriyel protein “yükleme rıhtımının” kimyasal olarak yeniden programlanabileceğini gösteriyor ve hem mikroplarla mücadele hem de onları mikroskobik fabrikalar olarak kullanma için yeni yollar açıyor.
Atıf: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Anahtar kelimeler: bakteriyel protein salgısı, SecA translokaz, allosterik aktivasyon, küçük molekül düzenleyiciler, antibakteriyel ilaç keşfi