Clear Sky Science · tr
LncRNA P4HA2-AS1, TRIM32 aracılı K63 ubiquitinasyonuyla ULK1 ve otofajik düzensizliği etkileyerek renal interstisyel fibrozisi tetikler
Neden Böbrek Yarası (Skarlaşması) Önemli?
Kronik böbrek hastalığı dünya genelinde yüz milyonlarca kişiyi etkiler ve genellikle diyaliz veya nakil gerektirecek kadar ilerleyene dek sessizce ilerler. Bu gerilemenin merkezinde, normal böbrek dokusunun giderek sert, işlevsiz bir maddeyle değiştirildiği skarlaşma (fibroz) adı verilen bir süreç vardır. Bu çalışma basit ama kritik bir soruyu gündeme getiriyor: böbrek hücreleri içinde onları bu zararlı skarlaşmaya iten moleküler anahtarlar nelerdir ve bu anahtarlar geri çevrilebilir mi?
Böbrek Hücrelerinde Gizli Bir RNA Anahtarı
Böbreklerimiz kanı karmaşık bir tübül ağı aracılığıyla süzer. Bu tübüller, idrar akışının tıkanması, yüksek kan şekeri veya ani kan akımı kaybı gibi hasarlara maruz kaldığında, hücreler arasına skar dokusu biriktirerek yanıt verebilir. Araştırmacılar, birkaç tip yaralanma modellenmiş farelerin böbreklerini sağlıklı böbreklerle RNA dizileme yöntemiyle karşılaştırdı; bu yöntem hangi genlerin aktif olduğunu gösterir. Proteine çevrilmeyen uzun kodlayıcı olmayan P4HA2-AS1 adlı az bilinen bir molekülün, hasarlı ve skarlaşma yapan böbreklerde ve laboratuvarda strese alınmış insan böbrek hücrelerinde sürekli olarak yükseldiğini keşfettiler. Bu RNA ağırlıklı olarak hücrelerin sıvı dolu bölgesinde bulundu; bu da oradaki diğer proteinleri kontrol etme olasılığına işaret ediyor. 
RNA’yı Azaltmak Böbreği Koruyor
P4HA2-AS1’in sadece bir belirteç mi yoksa hasarın aktif sürücüsü mü olduğunu test etmek için ekip, hem farelerde hem de kültürdeki insan böbrek hücrelerinde bu RNA düzeylerini düşürdü. Uzun süreli obstrüksiyon oluşturmak için bir üreterin bağlandığı yerleşik bir fare modelinde, hedeflenmiş viral dağıtımla bu RNA’yı azaltmak skarlaşmanın birçok belirtisini hafifletti: tübüller daha fazla bütün kaldı, hücreler arasındaki kollajen ve diğer skar proteinleri azaldı ve kanda böbrek işlevi göstergeleri iyileşti. İnsan böbrek hücreleri içeren kültürlerde P4HA2-AS1 düzeylerinin düşürülmesi, güçlü bir skarlaşma sinyali olan TGF-β’ye verilen yanıtı da azalttı; buna fibronectin, kollajen ve diğer pro-fibrotik faktörlerin daha az üretilmesi dahildi. Bu deneyler gösterdi ki bu RNA yalnızca hasarın bir göstergesi değil; skarlaşma sürecini aktif olarak besliyor.
Otofaji: Ev işleri yapan sistemden Zarara
Araştırmacılar sonra bu RNA’nın nasıl zarar verdiğini inceledi. Gen ifade ve görüntüleme verileri otofajiyi, yani hücrenin yıpranmış proteinleri ve organelleri parçalayan yerleşik geri dönüşüm sistemini işaret etti. Normal koşullarda otofaji sağlıklı bir ev işi sürecidir; ama aşırı ve uzun süreli tetiklendiğinde yaralı böbrekleri uyumsuz onarıma ve skarlaşmaya itebilir. Stres altındaki böbrek hücrelerinde P4HA2-AS1, otofaji akışını hızlandırdı ve geri dönüşüm veziküllerinin birikmesine yol açtı. RNA bloke edildiğinde bu aşırı geri dönüşüm hem hücrelerde hem de obstrükte fare böbreklerinde normale yakın düzeye düştü. Otofajinin merkezi başlatıcı enzimi olan ULK1 eksik fareler de skarlaşmaya karşı korundu; bu hayvanlarda P4HA2-AS1 fazla eklenmesi artık hasarı kötüleştiremedi ve böylece RNA’nın etkileri ile bu yol arasındaki bağlantı güçlendi.
Üç Parçalı Moleküler Zincir
Daha derine inerek ekip, P4HA2-AS1’e fiziksel olarak bağlanan proteinleri belirlemek için biyokimyasal avlama teknikleri kullandı. Bir protein öne çıktı: diğer proteinlere küçük moleküler “işaretler” olan ubiquitini ekleyen bir enzim olan TRIM32. RNA TRIM32’ye bağlanıyor ve onun yıkımından koruyarak hücre içindeki düzeylerini yükseltiyor. Stabilize olan TRIM32 ise ULK1’e spesifik bir ubiquitin zinciri ekliyor. Bu zincir ULK1’i yok etmeye göndermek yerine bir güçlendirici gibi davranarak ULK1’in otofajiyi tetiklemedeki yeteneğini artırıyor. Bilim insanları TRIM32’yi ya farelerde ortadan kaldırdıklarında ya da böbrek hücrelerinde susturduklarında hem skarlaşma hem de aşırı otofaji azaldı. P4HA2-AS1 bloke edilmiş hücrelere TRIM32 yeniden verilmesi, kısmen skarlaşma yanıtını geri getirdi; bu da bu enzimin zincirin önemli bir orta halkası olduğunu gösteriyor. 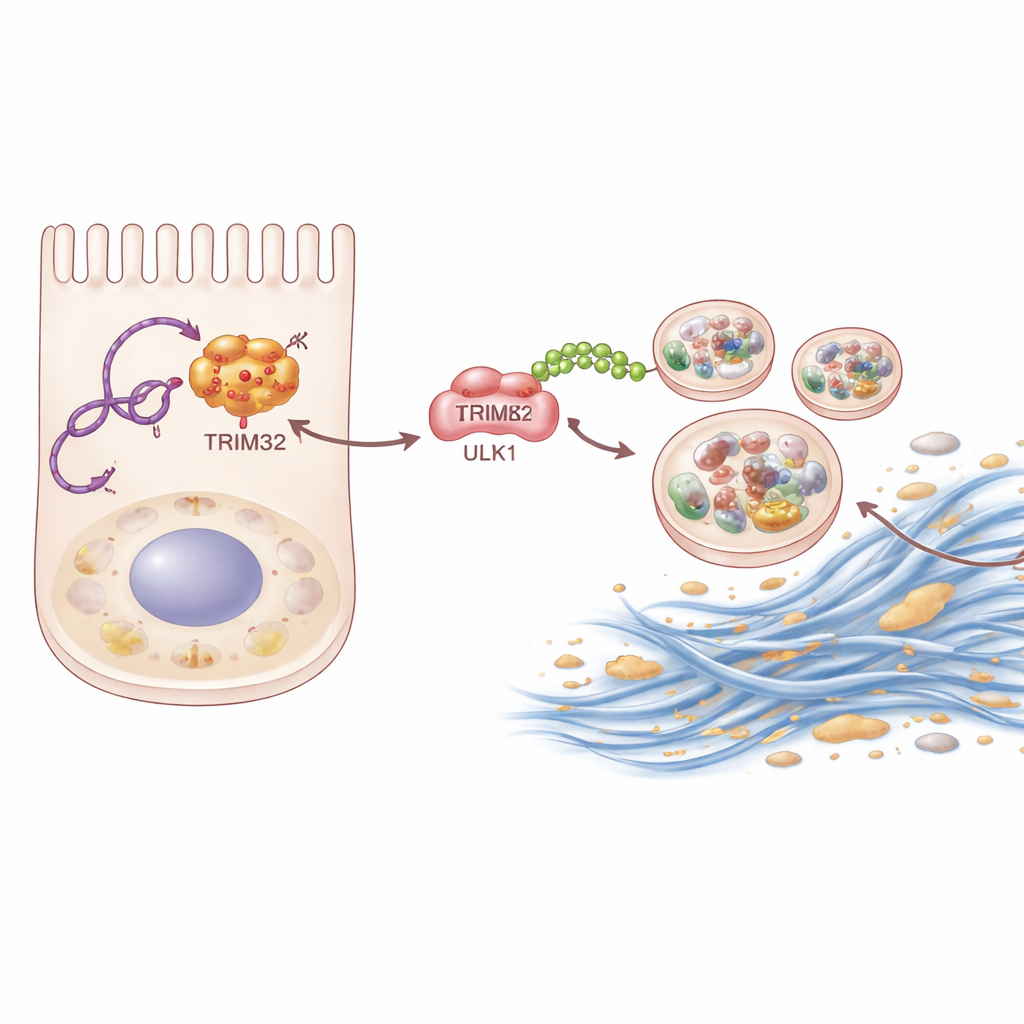
Daha Yumuşak Böbreklere Giden Yeni Yollar
Birlikte ele alındığında bu çalışma, uzun kodlayıcı olmayan RNA, protein etiketlemesi ve hücresel geri dönüşüm süreçlerini böbrek skar dokusu birikimine bağlayan daha önce bilinmeyen bir moleküler yolu açığa çıkarıyor. Yaralı böbreklerde P4HA2-AS1 yükselir, TRIM32’yi stabilize eder, ULK1’i süperşarj eder ve otofajiyi yararlı sınırlarının ötesine iterek sonuçta fibrotik protein birikimini ve işlev kaybını teşvik eder. Uzman olmayanlar için çıkarılacak ana mesaj şu: böbrek skarlaşması kaçınılmaz bir kara kutu değildir; ilaçla hedeflenebilecek tanımlanabilir anahtarlarla sürülür. Bu P4HA2-AS1–TRIM32–ULK1 eksenini hedeflemek—kaçak RNA’yı düşürmek, TRIM32’yi yatıştırmak veya ULK1 aktivitesini ince ayarlamak—bir gün kronik böbrek hastalığının ilerlemesini yavaşlatacak veya önleyecek yeni tedaviler sunabilir.
Atıf: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Anahtar kelimeler: kronik böbrek hastalığı, renal fibroz, otofaji, uzun kodlayıcı olmayan RNA, böbrek tübülleri