Clear Sky Science · tr
Histon demetilaz KDM7A, fibrotik makrofaj polarizasyonunu ve akciğer fibrozisi progresyonunu negatif olarak düzenler
Neden skarlaşmış akciğerler hepimizi ilgilendirir
Akciğerlerde inatçı skar dokusu oluştuğunda soluk almak günlük bir mücadele haline gelir. Pulmoner fibroz olarak bilinen bu durum milyonları etkiler ve şu an için kesin bir tedavisi yok—sadece hasarı yavaşlatan ilaçlar bulunuyor. Bu çalışmada araştırmacılar, makrofaj adı verilen bağışıklık hücrelerinin içinde akciğer skarlaşmasını kontrol altında tutmaya yardımcı olan daha önce gizli bir moleküler “fren” keşfettiler. Bu frenin anlaşılması, yalnızca akciğer fibrozisi için değil, zararlı skarlaşma ve kontrolsüz inflamasyonun bir arada görüldüğü diğer hastalıklar için de yeni tedavilere kapı açabilir.
Şekil değiştiren bağışıklık hücrelerinin öyküsü
Makrofajlar, dokularda devriye gezen, artık maddeleri temizleyen ve hasarın onarımına yardımcı olan ön saflardaki bağışıklık hücreleridir. Ancak aynı zamanda şekil değiştiren hücrelerdir: bazı durumlarda pro-inflamatuar savaşçılara dönüşürler, bazı durumlarda ise yara onarımını destekleyen ve skar oluşumunu tetikleyebilen hücrelere dönüşürler. Fibrotik skarlaşmayı destekleyen özel bir tür olan profibrotik makrofajlar (Fib-Mac), akciğer fibrozisiyle güçlü şekilde ilişkilidir. Bu hücreler fibroblastları aktive eden moleküller üretir; fibroblastlar aşırı kollajen ve diğer matriks bileşenlerini biriktirerek akciğeri yavaşça sertleştirir. Yazarlar, makrofajların içinde hangi genetik “ayarların” onların bu tehlikeli Fib-Mac hücrelerine dönüşüp dönüşmeyeceğini veya daha dengeli, koruyucu durumlarda kalmayı seçeceğini belirlediğini öğrenmek istediler.
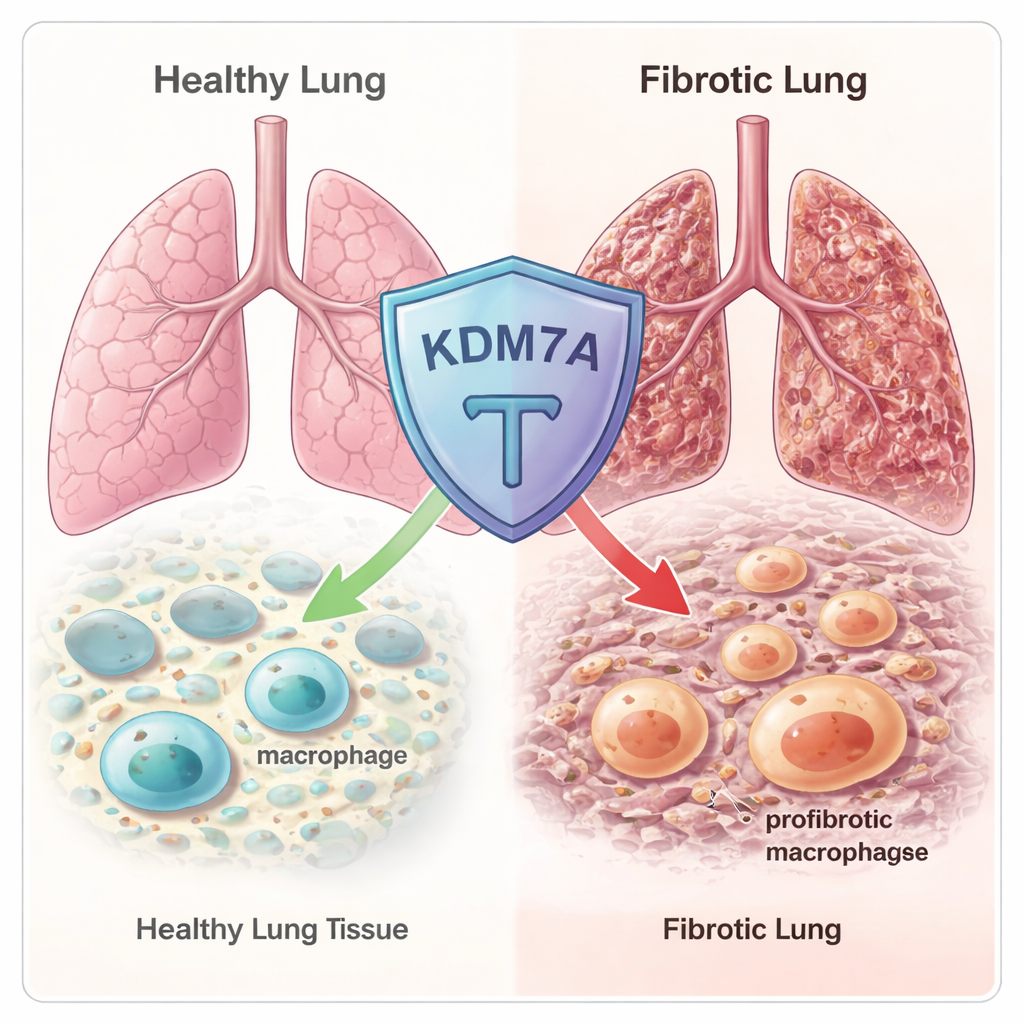
Genomda gizli bir epigenetik fren
Ekip, DNA’nın ne kadar sıkı paketlendiğini ve hangi genlerin açık ya da kapalı olduğunu inceleyen yüzlerce bilinen epigenetik düzenleyiciyi taramakla başladı. İnsan ve fare makrofajlarında RNA dizilemesi kullanarak KDM7A adlı bir enzimin makrofajlar fibrotik, yara-onarıcı duruma sevk edildiğinde güçlü şekilde açıldığını buldular. KDM7A bir “histon demetilaz”dır: DNA’nın sarıldığı histon proteinlerinden belirli kimyasal işaretleri çıkarır. Bu desen, KDM7A’nın makrofajlar skar-promotör bir kimliğe doğru kaymaya başladığında aktive olan yerleşik bir geri bildirim freni olarak işlev görebileceğini düşündürdü.
Bunu test etmek için araştırmacılar Kdm7a geninden yoksun fareler kullandılar ve kemoterapi ilacı bleomisin ile akciğer hasarı tetiklediler; bu, pulmoner fibrozis için standart bir modeldir. Yaralanmanın erken döneminde, normal ve Kdm7a eksik hayvanlarda akciğer dokusu benzer görünüyordu. Ancak üç hafta sonra Kdm7a eksik farelerde çok daha yaygın skarlaşma, küçük hava keseciklerinin çökmesi ve fibrozisi nicelendiren daha yüksek "Ashcroft skorları" görüldü. Bu knockout farelerde kollajen üretimi ve diğer fibroz ile ilişkili yollarla ilgili genler daha aktifti; bu da Kdm7a kaybının akciğerleri kalıcı ve zararlı skar oluşumuna karşı daha savunmasız hale getirdiğini doğruladı.
KDM7A makrofajları skar-promotör bir kaderden nasıl uzak tutar
Tek hücre RNA dizilemesi kullanarak yazarlar yaralanmış farelerden alınan bireysel akciğer hücrelerine yakından baktılar. Kdm7a yokluğunda, akciğer destek dokusundaki belirli bir makrofaj alt kümesinin dramatik şekilde genişlediğini ve Arg1, Spp1 ve Trem2 gibi genleri ifade eden güçlü bir Fib-Mac imzası kazandığını keşfettiler. Kültürlenmiş makrofajlardaki daha ileri deneyler, Kdm7a’nın kaldırılmasının Fib-Mac belirteç genlerini artırdığını ve hücre metabolizmasını kollajen üretimini ve sürdürülebilir aktivasyonu destekleyen yollara doğru yeniden kabloladığını gösterdi. Başka bir deyişle, KDM7A normalde makrofajları fibrozisi teşvik eden bir duruma sürükleyen hem genetik hem de metabolik programları sınırlıyor.
Daha derine indiklerinde araştırmacılar bu fren sisteminde kilit bir parça buldular: hücre içindeki RNA parçalarını algılayan bir sensör proteini olan TLR8. KDM7A’nın, Tlr8 yakınındaki bir güçlendirici bölgeden baskılayıcı bir kimyasal işaret (H3K27me2) kaldırarak Tlr8 geninin açık kalmasına yardımcı olduğunu buldular. Kdm7a devre dışı bırakıldığında bu işaret birikti, Tlr8 düzeyi düştü ve Fib-Mac özellikleri yoğunlaştı. Makrofajlarda doğrudan Tlr8’in azaltılması da onları fibrotik bir kimliğe itti; buna karşın TLR8’i aktive etmek veya fazla üretmek onları geri çekti, hatta Kdm7a yokken bile. Bu, KDM7A–TLR8 yolunun akciğerleri aşırı skarlaşmadan koruyan moleküler bir devrenin merkezinde yer aldığını gösterir.
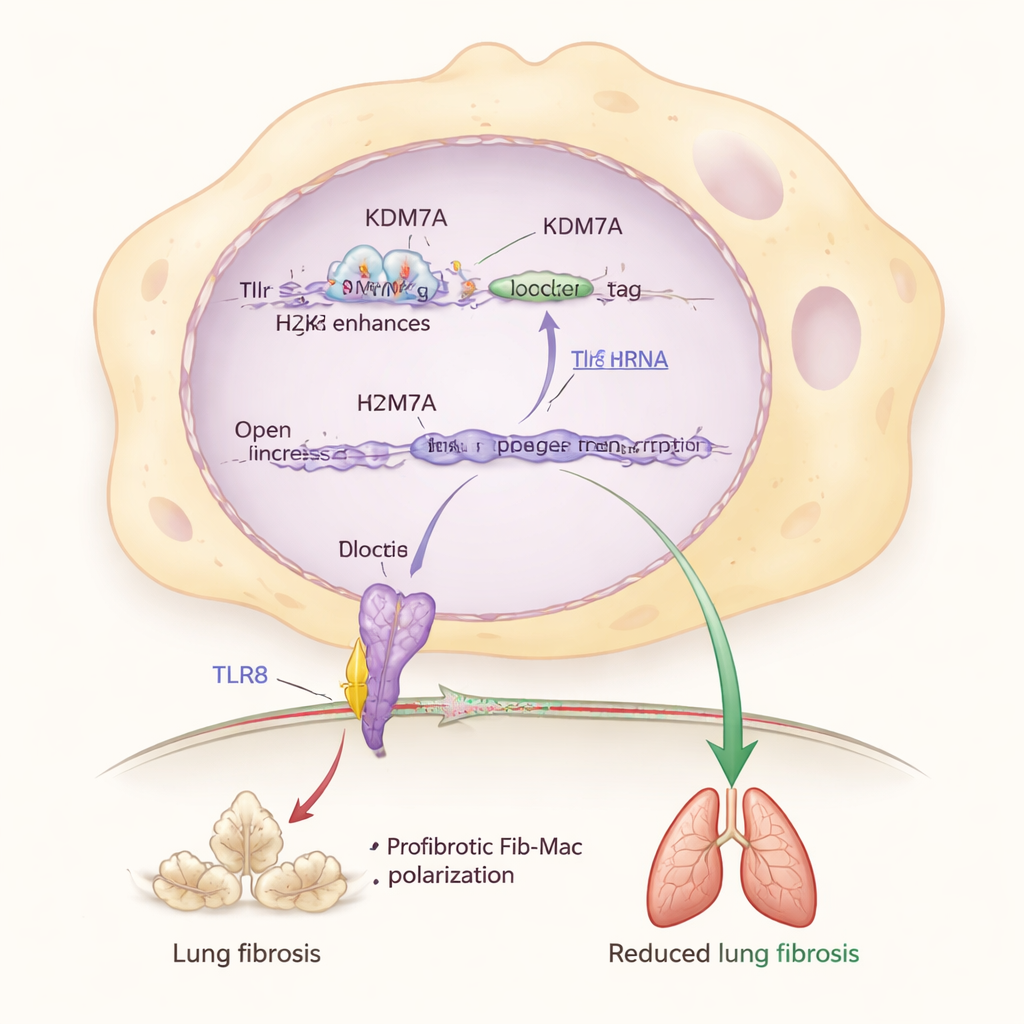
Yaşlanan akciğerlerden insan hastalığına
Bu bulguları insanlarla ilişkilendirmek için ekip fibrotik akciğer hastalığı olan hastalardan alınan akciğer dokusunu inceledi. Hastalıklı akciğerler, hastalıklı olmayan kontrol dokusuna göre çok daha fazla Fib-Mac belirteci taşıyan makrofaj içeriyordu, ancak bu hücrelerde belirgin şekilde azalmış KDM7A ve TLR8 seviyeleri vardı. İdiopatik pulmoner fibrozisi olan hastalardan alınmış mevcut tek hücre veri setlerinin yeniden analizi bu deseni doğruladı: Fib-Mac imzaları yükseldikçe KDM7A ifadesi düştü. Araştırmacılar ayrıca büyük bir fare atlasını taradılar ve erkeklerde makrofajlardaki Kdm7a ve Tlr8 ifadesinin yaşla azaldığını buldular; bu, yaşlı erkeklerde pulmoner fibrozis riskinin daha yüksek olmasını yansıtıyor. Bu, KDM7A–TLR8 freninin yaşa ve cinsiyete bağlı zayıflamasının kimlerin şiddetli akciğer skarlaşmasına daha yatkın olduğunu açıklamaya yardımcı olabileceğini düşündürür.
Gelecekteki tedaviler için ne anlama geliyor
Basitçe ifade etmek gerekirse, bu çalışma bağışıklık sistemimizin faydalı onarım hücrelerinin aşırıya kaçmasını ve kalıcı skarlara dönüşmesini engelleyen içsel bir güvenlik mekanizması taşıdığını gösteriyor. KDM7A, TLR8 aracılığıyla, makrofajların profibrotik moda kilitlenmesini engeller ve böylece yaralanma sonrası esnek, fonksiyonel akciğer dokusunu korumaya yardımcı olur. Bu sistem genetik kayıp, yaşlanma veya diğer faktörlerle aksadığında makrofajlar daha kolay şekilde "skar amplifikatörlerine" dönüşebilir ve fibrozisi kötüleştirir. Bu epigenetik freni ortaya çıkararak çalışma, KDM7A aktivitesini artıran, etkilerini taklit eden veya TLR8’i dikkatle uyaran ilaçların bir gün mevcut antifibrotik tedavilere tamamlayıcı olabileceğini ve ilerleyici, yaşamı sınırlayan akciğer skarlaşmasına karşı daha iyi koruma sağlayabileceğini işaret ediyor.
Atıf: Funagura, N., Koga, T., Etoh, K. et al. Histone demethylase KDM7A negatively regulates fibrotic macrophage polarization and lung fibrosis progression. Commun Biol 9, 309 (2026). https://doi.org/10.1038/s42003-026-09610-1
Anahtar kelimeler: pulmoner fibroz, makrofajlar, epigenetik, KDM7A, TLR8