Clear Sky Science · tr
Siglec-6’nın glikolipit tanıması ve bağlanması hücre zarıyla etkileşimlere bağlıdır
Hücrelerimiz Dostu Düşmandan Nasıl Ayırıyor
Bağışıklık sistemi kendi hücrelerimizi sürekli tarar; ne zaman sakin kalacağını, ne zaman saldıracağını belirler. Bu gözetimin önemli bir parçası, hücre yüzeylerindeki şekerli yapıların tanınmasını içerir. Bu çalışma, Siglec-6 adındaki bir insan bağışıklık reseptörünün yalnızca bu şekerleri değil, aynı zamanda bağlanma kararlarını özellikle hassas kılmak için çevresindeki hücre zarını da kullandığını ortaya koyuyor. Bu sıra dışı strateji, vücudumuzun bağışıklık sinyallerini nasıl ince ayarladığını açıklamaya yardımcı olabilir ve hedefe yönelik tedaviler için yeni yollar açabilir.
Bağışıklık Hücrelerinde Şeker Algılayan Bir Kapı Bekçisi
Siglec’ler, bağışıklık hücrelerinin üzerinde bulunan ve sialik asit içeren şekerleri tanıyan bir reseptör ailesidir; bu sayede bağışıklık sistemi “öz” ile “öz olmayan”ı ayırt etmeye yardımcı olur. Çoğu Siglec, bu şekerlere tutunmak için tek bir, yüksek oranda korunmuş yapıtaşı—arjinin aminoasidini—kullanır. Bu arjinin çıkarıldığında bağlanma genellikle başarısız olur. Ancak Siglec-6 sıra dışıdır: önceki çalışmalar, bu kilit arjinin mutasyona uğrasa bile bazı şeker taşıyan lipidlere bağlanmaya devam edebildiğini göstermiştir. Yeni çalışma, Siglec-6’nın bu görünür kuralı nasıl çiğnediğini ve bunun mast hücreleri, bellek B hücreleri ve insan plasenta hücrelerindeki rolü için ne anlama geldiğini ortaya çıkarmayı amaçladı.
Siglec-6’nın Aradığı Özel Lipitler
Hücre yüzeylerinde ilgili şekerler hem proteinlerde hem de lipitlerde sergilenebilir. Bu çalışma, gangliosidler adı verilen bir grup şeker-taşıyan lipide, özellikle GM1, GM2 ve GM3 adındaki birbirine yakın üç tipe odaklanıyor. Bu üçünün de zar dışına tek bir sialik-asit–kaplı “baş”ı çıkar. Önceki deneyler, Siglec-6’nın GM1’e zarın bir parçasıyken güçlü biçimde bağlandığını, ancak şeker başları çok benzer olmasına rağmen GM2 veya GM3’e neredeyse hiç bağlanmadığını göstermişti. Gerçekçi zarların ayrıntılı bilgisayar simülasyonlarını kullanarak, yazarlar GM1 ve GM3’teki sialik asidin eşit derecede açığa çıktığını ve erişilebilir olduğunu doğruladılar. Başka bir deyişle, basit fiziksel erişim GM1’e özel statüyü vermiyor. Bunun yerine, GM1’in ucundaki ek bir şeker—terminal galaktoz—Siglec-6’yı zara karşı doğru şekilde konumlandırmaya yardımcı olan kritik bir unsur olarak ortaya çıktı.
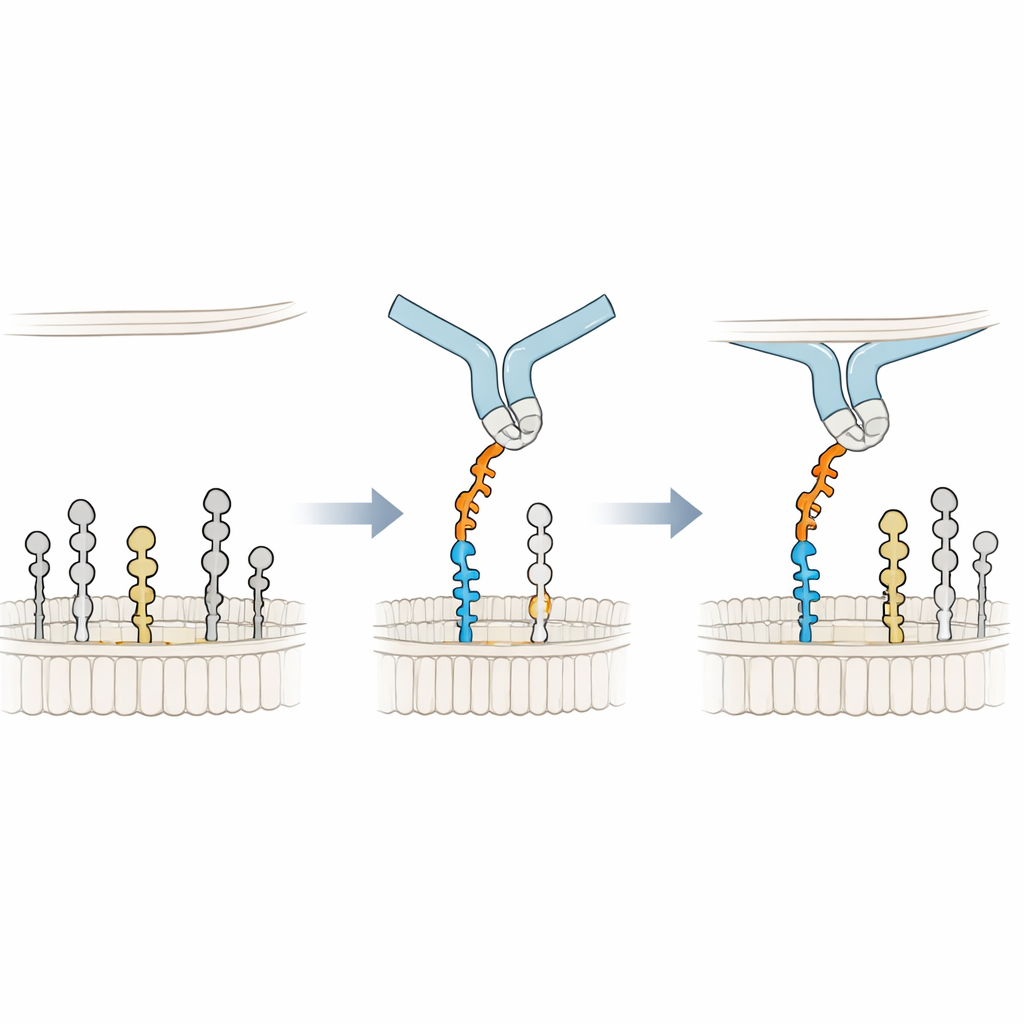
Daha İyi Bir Tutunma İçin Zama Dayanma
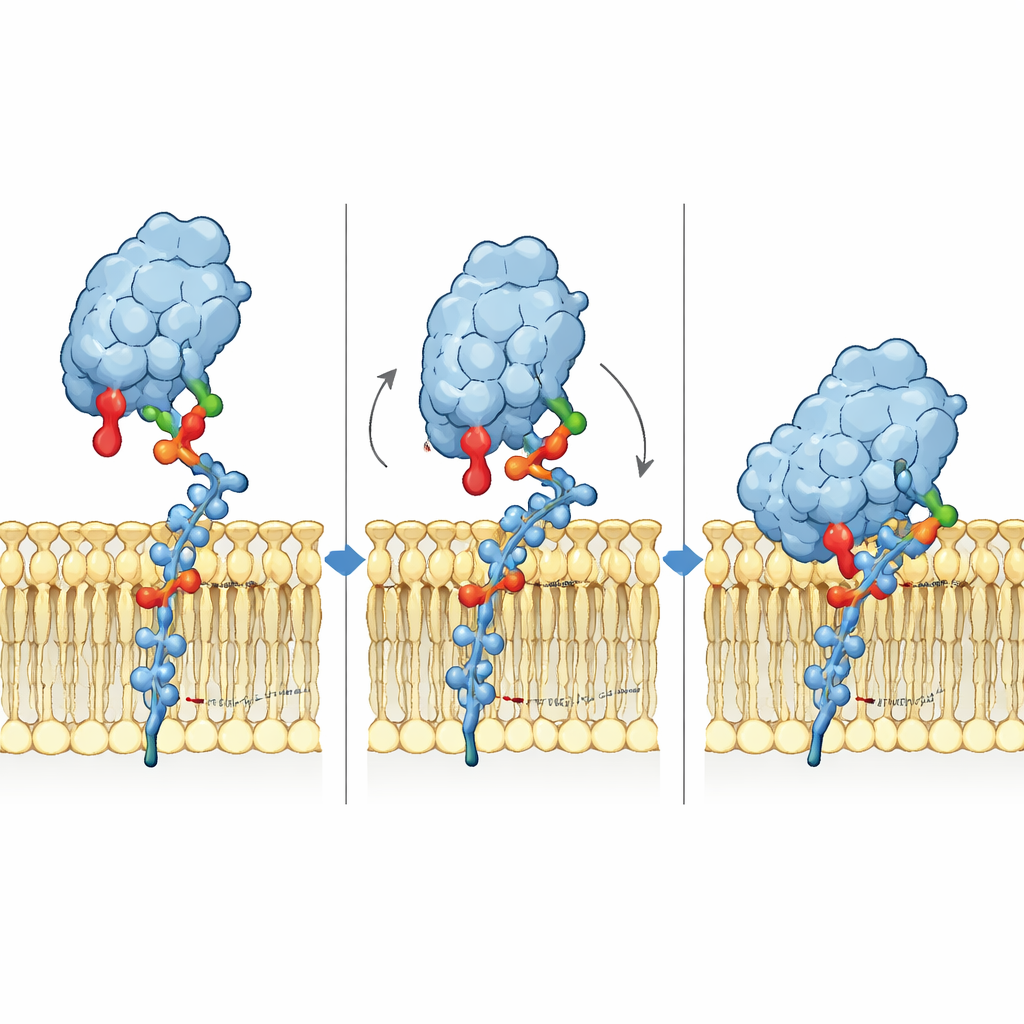
Bağlanma mekanizmasını atomik ayrıntıda anlamak için araştırmacılar, Siglec-6’nın zar içindeki GM1 ile etkileşimini gösteren 3B modeller oluşturup uzun moleküler dinamik simülasyonları çalıştırdılar. Siglec-6’nın hâlâ kanonik arjinin (Arg122) ile sialik aside temas ettiğini, ancak bu temanın zaman içinde açılıp kapandığını buldular. Kompleksi kararlı kılan şey yeni bir unsurdu: yakındaki bir triptofan (Trp127) yağlı zar kısmına doğru itilerek giriyor, bitişikteki bir lizinin (Lys126) ise çevredeki lipidlerin yüklü baş gruplarıyla etkileştiği görüldü. Zardaki bu “kilit”leme, sıradan şeker–arjinin etkileşimini tamamlayarak bağlanma enerjisinin bir kısmını lipid ortamından ödünç alıyor. GM1’in terminal galaktozu, GM2’yi taklit etmek için çıkarıldığında, Siglec-6’daki esnek bir döngü boşluğa doğru sallanıp reseptörü zardan uzaklaştırıyor ve bu zar desteksiz tutuşu bozuyor; bu durum kararlı bağlanmanın kaybını açıklıyor.
Mekanizmayı Test Eden Deneyler
Araştırma ekibi daha sonra bu bilgisayar temelli bulguları canlı hücre ve biyokimyasal testlerde sınadı. Hücreleri normal veya mutasyona uğramış Siglec-6 eksprese edecek şekilde tasarladılar ve bu hücrelerin florasan lipozomlara ve GM1 taşıyan küçük lipid disklerine ne kadar iyi bağlandıklarını ölçtüler. Kanonik arjininin mutasyonu, GM1 zara entegre olduğunda bağlanmayı yalnızca ılımlı olarak azalttı; bu, Siglec-6’nın bu ortamda yalnızca bu residuğe bağlı olmadığını doğruladı. Buna karşılık, Trp127’nin mutasyonu GM1 içeren lipozomlara bağlanmayı neredeyse tamamen ortadan kaldırdı ve hem Trp127 hem de Lys126 birlikte mutasyona uğradığında bağlanma neredeyse tamamen kayboldu. Aynı mutantlar, zar dışında sunulan GM1-benzeri şekerlere normal şekilde bağlandı; bu da Siglec-6’nın temel yapısının sağlam olduğunu gösterdi. Doğal kütle spektrometrisi deneyleri ayrıca Siglec-6’nın sadece GM1’e değil, sıradan fosfolipitlere de bağlanabildiğini ve bu lipid etkileşiminin Trp127 çıkarıldığında kaybolduğunu ortaya koydu. Dikkat çekici şekilde, Siglec-6 GM1 içermeyen “çıplak” lipozomlara bile Trp127’e bağımlı olarak yapıştı; bu, önce zarı denediğini, ardından GM1 ile karşılaştığında kilitlediğini düşündürüyor.
Serbest Şekerler Farklı Bir Öykü Anlatıyor
Aynı üç gangliosid zarın bir parçası yerine serbest yüzen şeker parçacıkları olarak test edildiğinde, Siglec-6 akranlarına daha çok benzedi. Çözelti içinde GM1, GM2 ve GM3’e benzer derecede zayıf afiniteyle bağlandı ve bu durumda kanonik arjinin artık elzemdi: Arg122’nin mutasyonu bağlanmayı keskin biçimde azalttı, Trp127’nin mutasyonunun ise az etkisi oldu. Bu karşıtlık, Siglec-6’nın şekerlerle zar içinde mi yoksa serbest formda mı karşılaştığına bağlı olarak etkili bir şekilde mekanizma değiştirdiğini gösteriyor. Zar ortamında, şeker başı, GM1’in terminal galaktozu ve doğrudan zar teması arasındaki işbirliğine dayanıyor; çözeltide ise klasik arjinin merkezli tanıma motifine geri dönüyor.
Bağışıklık Kontrolü İçin Neden Önemli
Bir arada ele alındığında, çalışma Siglec-6’yı membranın fiziksel bağlamını kullanarak özgüllüğünü keskinleştiren ince ayarlı bir sensör olarak tanımlıyor. Çevresindeki lipitlere kısmen demirleyerek, çok benzer gangliosidler arasında GM1’i seçici biçimde tanıyabiliyor; bu şekilde genel bir “sialik asit okuma”yı belirli bir yüzey deseninin yüksek hassasiyetli detektörüne dönüştürüyor. Bu zar destekli strateji şimdiye kadar incelenen Siglec’ler arasında benzersiz görünmektedir ve Siglec-6’nın bağışıklık yanıtlarını düzenleyen veya belirli dokuları (örneğin insan plasentasını) işaretleyen özgül glikolipit imzalarını taramasına yardımcı olabilir. Bu çift modlu tanımayı anlamak, Siglec-6’nın şeker ve zar algısını bir arada kullanan tedavi ve tanı araçlarının tasarımına katkıda bulunabilir.
Atıf: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Anahtar kelimeler: Siglec-6, gangliosidler, hücre zarı, glikolipit tanıma, bağışıklık regülasyonu