Clear Sky Science · tr
ATM İnhibisyonu, AAV Kaynaklı Apoptotik Yol Aktivasyonunu Bastırarak Knock-in Verimliliğini Artırır
Gen Düzenlemeyi Daha İyi Hale Getirmek
CRISPR gen düzenleme, kalıtsal hastalıklar için tedaviler, dayanıklı bitkiler ve güçlü araştırma araçları vadeder. Ancak en değerli numaralarından biri—genoma seçilmiş bir noktaya yeni DNA’yı kesin olarak yerleştirme, yani “knock-in”—hala verimsiz çalışıyor. Bu çalışma bazı hücrelerin yeni DNA’yı neden diğerlerinden daha kolay kabul ettiğini araştırıyor ve özellikle adeno-associate virüs (AAV) kullanıldığında hücreleri daha sık ve doğru düzenleme yapmaya yönlendirecek bir yol ortaya koyuyor.
DNA Tamirini Gerçek Zamanlı İzlemek
Hangi etkenlerin hassas gen yerleştirmeyi kolaylaştırıp hangilerinin engellediğini anlamak için araştırmacılar fare embriyo kök hücreleri içinde karmaşık bir “gösterge paneli” kurdular. Bu üçlü raporlayıcı sistemi, aynı hücrelerde CRISPR’ın DNA’yı kesip kesmediğini, kesin bir knock-in olup olmadığını ve hücrenin bunun yerine bağlama/ekleme yöntemleriyle bağışçı DNA’yı kaba şekilde yerleştirip yerleştirmediğini izlemek için üç floresan belirteç kullanır. Akış sitometrisiyle farklı renk kombinasyonlarını okuyarak, şablon-temelli temiz düzenlemeleri hata eğilimli eklemelerden ve düzenlenmemiş hücrelerden ayırabildiler. Bu yan yana izleme, farklı DNA tamir yollarının her sonuca nasıl katkıda bulunduğunu eski PCR tabanlı testlerden çok daha yüksek çözünürlükle haritalamalarına olanak verdi.
İki DNA Yardımcısı, İki Çok Farklı Tepki
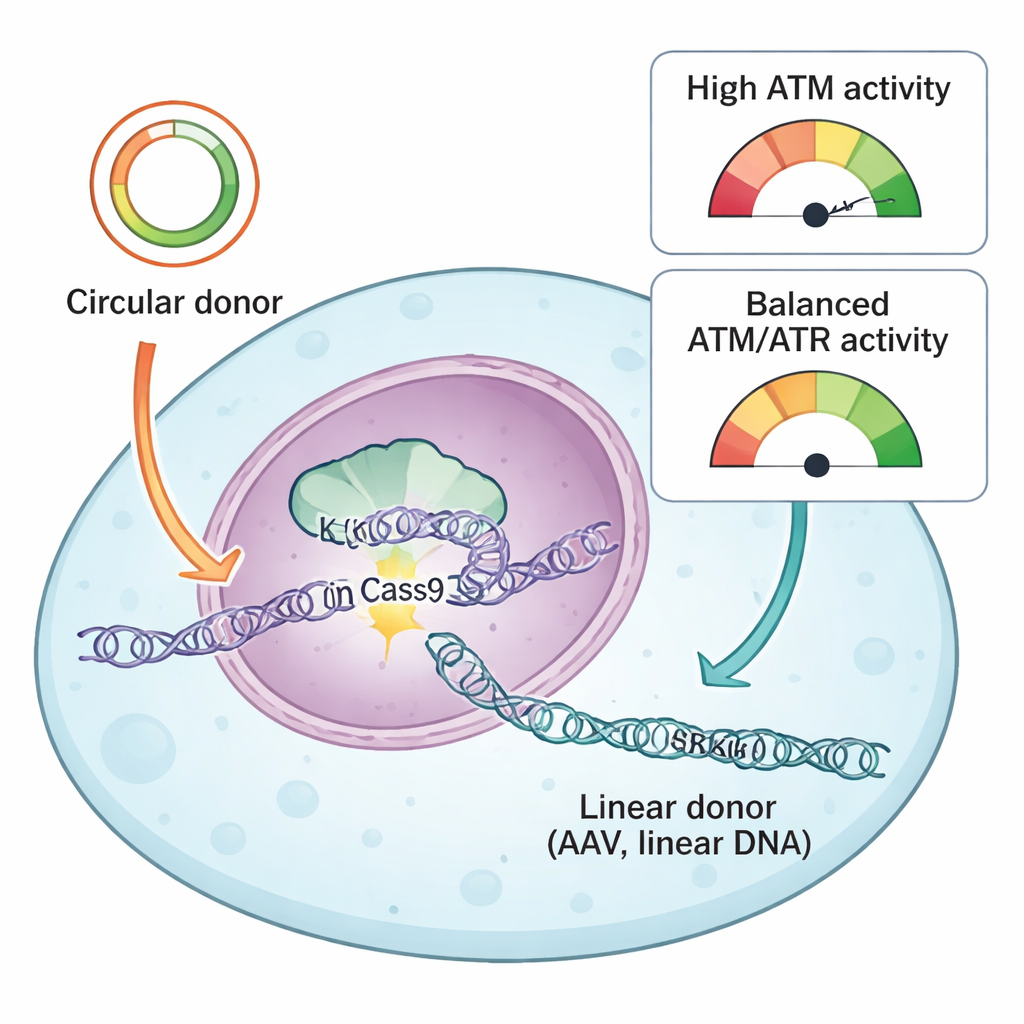
Takım, CRISPR onarımlarını yönlendirmek için yaygın olarak kullanılan iki bağışçı DNA türünü karşılaştırdı: dairesel plazmidler ve doğrusal AAV kaynaklı DNA. Her ikisi de hücreye yeni diziyi nereye yerleştireceğini söyleyen uyum kolları (“homology arms”) taşır, ancak hücreye farklı fiziksel biçimlerde girerler. Dairesel plazmidler çift sarmallı, kapalı döngüler iken AAV bağışçıları genellikle tek doğrusal moleküller halinde gelir. Raporlayıcı sistemleri ve DNA hasar–yanıtı proteinlerini hedefleyen bir ilaç kütüphanesi kullanarak, yazarlar bir anahtar proteinin, ATR’nin, her iki bağışçı türü ile başarılı knock-inler için evrensel olarak gerekli olduğunu buldular. ATR’nin inhibisyonu kesin insertasyonu keskin biçimde azalttı, oysa KEAP1–NRF2 yoluyla ATR aktivitesini hafifçe artırmak özellikle AAV bağışçıları ile knock-in verimliliğini yükseltti.
DNA Koruması İşe Yaramayınca Geri Tepiyor
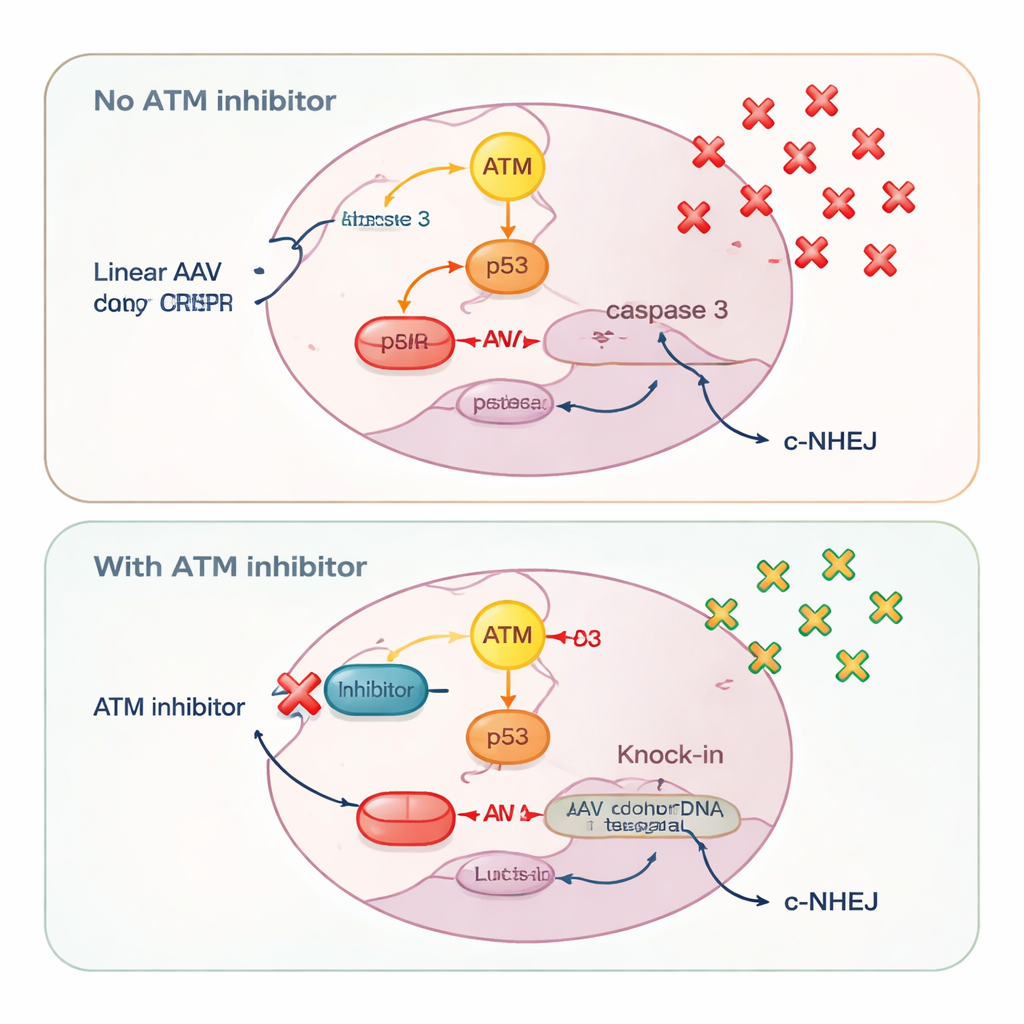
Farklı bir DNA hasar algılayıcısı olan ATM ise dikkat çekici şekilde bağışçıya bağımlı bir davranış sergiledi. Dairesel plazmid bağışçılarla ATM’i engellemek, çift kırıkların onarımına yardım eden klasik rolüyle uyumlu olarak hem kesin knock-inleri hem de uç-birleştirme yoluyla olan eklemeleri azalttı. Ancak doğrusal DNA ile—ister AAV, ister kendi-kendine tamamlayıcı AAV, ister doğru parçalara kesilmiş plazmidler olsun—ATM inhibisyonu ters etki yaptı: knock-in verimliliğini artırdı. Araştırmacılar bu etkinin, hücrelerin doğrusal DNA patlamalarını nasıl yorumladığına dayandığını izlediler. Yüksek dozda AAV, ATM’yi güçlü biçimde aktive etti ve bu da p53 ile kaspaz 3’ü açığa çıkararak programlı hücre ölümünü başlattı. Çok sayıda bağışçı DNA almış olan hücreler—dolayısıyla başarılı bir knock-in yapma olasılığı en yüksek olanlar—aynı zamanda bu alarm sistemi yüzünden öldürülme olasılığı en yüksek olanlardı.
En Donanımlı Hücreleri Kurtarmak
ATM inhibitörleri eklenerek bilim insanları ATM–p53–kaspaz 3 ölüm yolunu susturdular. Bu, yüksek miktarda bağışçı DNA taşıyan hücrelerin hayatta kalmasını sağladı ve daha fazla hücrenin kesin bir knock-in tamamlamasına izin verdi. Viral genom kopyalarının ölçümleri, ATM inhibisyonunun hücre içinde tutulan AAV molekülü sayısını artırdığını doğruladı. Aynı zamanda ATM blokajı, bu yolakta merkezi bir enzim olan DNA-PK aktivasyonunun azalmasıyla gösterildiği üzere hızlı, kaba bir onarım yolu olan klasik homolog olmayan uç-birleştirmeyi hafifçe zayıflattı. Bu rekabet eden onarım seçeneğini zayıflatmak, daha fazla CRISPR kesisinin bağışçı şablonunu dikkate almayan hızlı yamalardan ziyade homoloji-temelli knock-in yönüne itildi.
Gelecekteki Gen Terapileri İçin Anlamı
Uzman olmayanlar için mesaj şudur: DNA hasarından koruyan aynı hücresel güvenlik mekanizmaları, özellikle büyük miktarda viral bağışçı DNA kullanıldığında hassas gen düzenlemeyi istemeden sabote edebilir. Bu çalışma, bu koruyucuları nazikçe ayarlamanın—ATR’yi aktif tutup doğrusal bağışçılar (ör. AAV) mevcutken ATM’yi geçici olarak sınırlamanın—CRISPR knock-inlerini daha güvenilir ve verimli kılabileceğini gösteriyor. Böyle bir strateji, planlanan değişikliği kabul eden daha fazla hücreye yardımcı olarak gen terapilerini, hücre mühendisliğini ve hastalık modellerini iyileştirebilir ve gereksiz hücre kaybını azaltabilir.
Atıf: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Anahtar kelimeler: CRISPR knock-in, AAV gen düzenleme, DNA hasar yanıtı, ATM inhibisyonu, genom mühendisliği