Clear Sky Science · tr
Terapi Tasarımını İyileştirmek İçin Nanobody Geliştirilebilirliğinin Karakterize Edilmesi: Therapeutic Nanobody Profiler
Geleceğin ilaçları için küçük antikor kuzenleri neden önemli
Bugünün birçok en çok satan ilacı antikorlardır—hastalık hedeflerine büyük bir hassasiyetle bağlanan proteinler. Nanobody adı verilen daha yeni ve daha küçük bir bağlayıcı sınıfı, virüslerin, tümörlerin ve diğer moleküllerin zor erişilen ceplerine nüfuz edebilir. Ancak bir hedefe bağlanabilmek tek başına yeterli değildir: aday bir ilacın üretiminin kolay olması, flakonda kararlı kalması ve vücutta güvenli olması gerekir. Bu makale, bilim insanlarının yalnızca diziden erken safhada hangi nanobody’lerin pratik ilaçlara dönüşme olasılığının daha yüksek olduğunu değerlendirmesine yardımcı olmak için tasarlanmış hesaplamalı bir araç olan Therapeutic Nanobody Profiler’ı tanıtıyor.
Ümit vaat eden fikrî aşamadan pratik ilaca
Bir proteini gerçek bir terapiye dönüştürmek, “geliştirilebilirlik” terimi altında toplanan bir dizi pratik engeli içerir. Proteinlerin büyük miktarlarda üretilebilmesi, çözünür kalması, birbirine yapışmaktan kaçınması ve nakil ile depolama sırasında kararlı olması gerekir. Son on yılda araştırmacılar, bol klinik veri ve özel laboratuvar testleriyle desteklenen tam boy monoklonal antikorlar için bu özelliklerin birçoğunu nasıl tahmin edeceklerini öğrendiler. Ancak nanobody’ler yapısal olarak farklıdır: bir çift zincir yerine tek bir domainden oluşurlar, genellikle daha uzun bağlayıcı döngülere sahiptirler ve geleneksel antikorlarda gömülü olan yüzey bölgelerini açığa çıkarırlar. Sonuç olarak, sıradan antikorlara göre ayarlanmış yöntemler nanobody’lere uygulandığında yanıltıcı sonuçlar verebilir.
Nanobody tuhaflıklarına göre inşa edilmiş bir profiler
Bu uyumsuzlukla başa çıkmak için yazarlar, önceki bir standart antikor aracından ilham alarak ama nanobody biyolojisi etrafında yeniden mühendislik yaparak Therapeutic Nanobody Profiler (TNP)ı tasarladılar. Klinik denemeler, doğal bağışıklık repertuarları, patentler, bilimsel makaleler ve bilinen kristal yapılar dahil olmak üzere birçok kaynaktan nanobody dizilerini derlediler. Tek domainli antikorlara uygun derin öğrenme yapı tahmincileri kullanarak bu diziler için 3B modeller ürettiler. Her modelden bağlayıcı döngülerin uzunluğunu, bir anahtar döngünün proteinden ne kadar uzaklaştığını ve yüzeydeki hidrofobik ile yüklü kalıntı kümelerinin nasıl düzenlendiğini ölçtüler—bunlar çözünürlük, agregasyon ve özgül olmayan yapışma üzerinde güçlü etkileri olan özelliklerdir.
İki yapısal tür, her ikisi de kullanılabilir
En çarpıcı bulgulardan biri ana bağlayıcı döngü olan CDR3 ile ilgilidir. Ekip bu döngünün ne kadar “kompakt” olduğunu—uzunluğunu proteinden ne kadar uzandığıyla karşılaştırarak—nicelendirince iki yapısal stile açık bir ayrım gördüler. Bir alt tipte döngü daha uzundur ve proteinin yan tarafı üzerine geri katlanarak belirli işaretleyici kalıntılarla birçok stabilize edici temas oluşturur. Diğerinde döngü, geleneksel bir antikor fragmanındaki gibi daha çok dışarı doğru çıkar. Klinik aşamasındaki nanobody’ler her iki alt tipte de yer alıyor ve araştırmacılar agregasyon, kendi kendine ilişki ve termal stabilite gibi onlarca pratik laboratuvar ölçümüyle karşılaştırdıklarında, hiçbir stilde sistematik bir dezavantaj görmediler. Bu, diğer özellikler kabul edilebilir olduğu sürece ilaç tasarımcılarının genel döngü şeklinin birini diğerine tercih etmeleri gerekmediği anlamına geliyor.
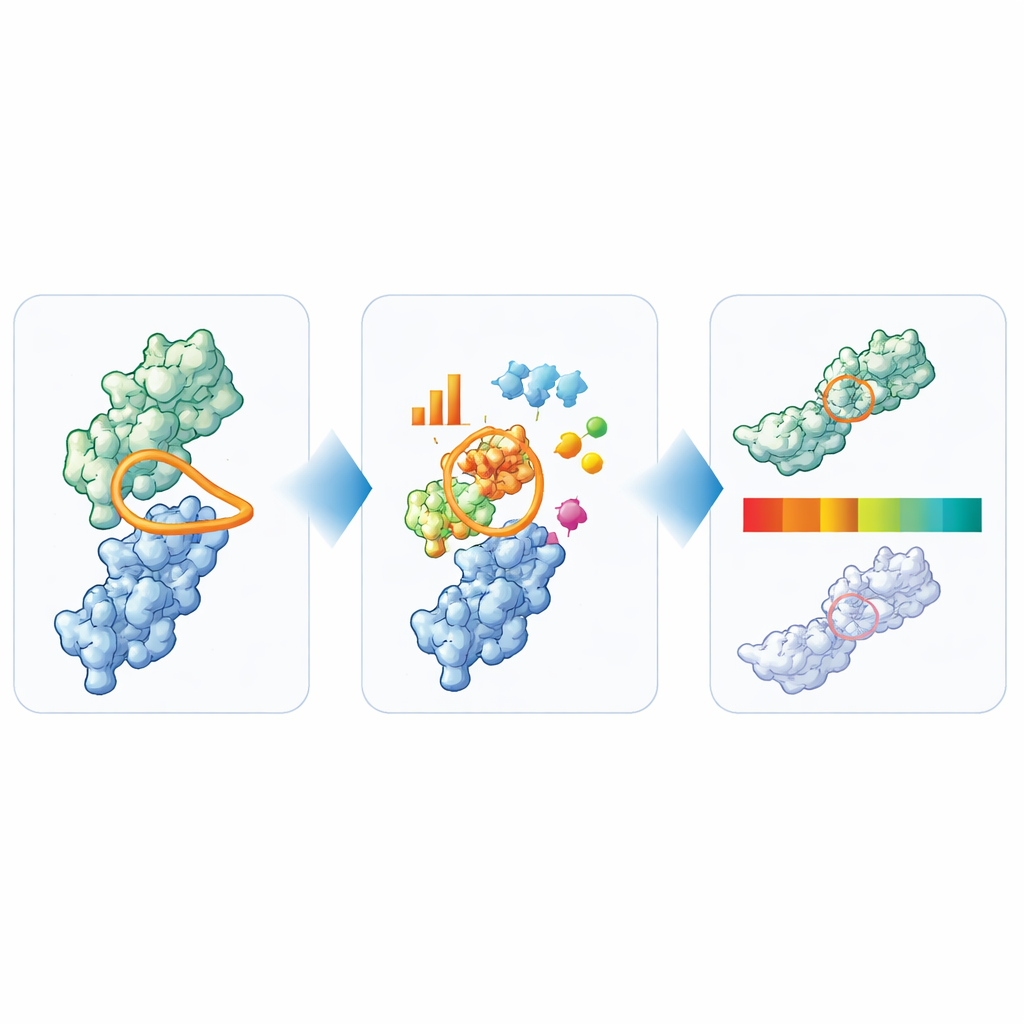
Yapıyı basit trafik ışıklarına dönüştürmek
Geniş analizlerinden yazarlar, nanobody’lerin temel geliştirilebilirlik kaygılarını birlikte yakalayan altı ana özelliği çıkardılar: toplam döngü uzunluğu, CDR3’ün özgül uzunluğu ve kompaktlığı ile bağlanma bölgesi etrafındaki hidrofobik, pozitif yüklü ve negatif yüklü yüzey yamalarının boyutları. Ardından her ölçü için pratik sınırları belirlemek adına klinik testlere ulaşmış 36 nanobody’yi kullandılar. Merkezi, yaygın değerler “yeşil”, sınırdaki değerler “amber” ve açık aykırılar “kırmızı” olarak etiketlendi. Bu sinyallerin ne kadar bilgilendirici olduğunu test etmek için TNP’yi 72 ek tescilli nanobody üzerinde uyguladılar ve bayrakları kapsamlı bir laboratuvar test paneliyle karşılaştırdılar. TNP tarafından açık aykırı olarak işaretlenen nanobody’ler genellikle birden çok deneysel uyarı işareti de gösterirken, hesaplamada temiz görünenler laboratuvarda daha sık iyi davranış sergiledi.
Yarının tedavileri için anlamı
Uzman olmayanlar için temel mesaj, bir nanobody’nin şeklinin ve yüzey deseninin artık pahalı laboratuvar çalışmalarına başlamadan önce basit bir geliştirilebilirlik profiline dönüştürülebilir olmasıdır. Therapeutic Nanobody Profiler deneylerin yerini almaz ve özellikle laboratuvar testleri nanobody’lerin daha büyük antikor parçalarına füzyonları üzerinde yapıldığı için tahminlerle testler arasında hâlâ uyumsuzluklar olabilir. Ancak olağandışı uzun veya sıkı katlanmış döngüleri ya da sorunlu yüzey yamalarını hızla işaretleyerek TNP, güvenilir ilaçlara dönüşme olasılığı daha yüksek nanobody’lere dikkat çekilmesine yardımcı olur. Daha fazla nanobody klinik denemelere girdikçe ve referans küme genişledikçe bu aracın daha da hassaslaşması ve küçük, dayanıklı antikor benzeri ilaçların tasarımını hızlandırması bekleniyor.
Atıf: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Anahtar kelimeler: nanobody'ler, biyolojik ilaç geliştirilebilirliği, hesaplamalı profilleme, antikor mühendisliği, protein stabilitesi