Clear Sky Science · tr
DTX1 aracılı TUBB3 yıkımı, Kupffer hücrelerinde M1/M2 polarizasyonunu düzenleyerek hepatosellüler karsinom ilerlemesini hafifletir
Karaciğer kanserinde bağışıklığın “komşularının” önemi
Çoğu insan kanseri kontrolünü yitiren hücrelerin hastalığı olarak düşünür. Oysa tümörler bağışıklık hücreleri, kan damarları ve destekleyici dokudan oluşan yoğun bir mahallede yaşar; bu çevre kanserle savaşabilir veya sessizce onu besleyebilir. Bu çalışma karaciğer kanserine —özellikle hepatosellüler karsinoma— odaklanıyor ve özelleşmiş karaciğer bağışıklık hücreleri içinde bir proteinin anti-kanser yanıt ile tümör-dostu bir ortam arasındaki dengeyi nasıl kaydırdığını ortaya koyuyor. Bu gizli kontrol anahtarını anlamak, mevcut immünoterapileri iyileştirmenin yeni yollarını açabilir.
Çevresi tarafından yönlendirilen bir karaciğer kanseri
Karaciğer, organı sağlıklı tutmaya yardımcı olan yerleşik bir popülasyon olan Kupffer hücreleri de dahil olmak üzere zengin bir bağışıklık hücresi çeşitliliğine sahiptir. Karaciğer kanserinde bu hücrelerin bir kısmı tümör ilişkili makrofajlara dönüşür; bunlar ya kanseri hedef alan (M1-benzeri durum) ya da onu koruyan (M2-benzeri durum) işlevler gösterebilir. Tümörleri M2-tipi makrofajlarla dolu olan hastaların genellikle daha kötü seyrettiği ve PD-1 inhibitörleri gibi bağışıklık engellerini kaldıran ilaçlara daha kötü yanıt verdiği gözlemleniyor. Yazarlar, halk veri tabanları ve hasta örneklerini tarayarak hem karaciğer kanseri hem de bu makrofajlarla ilişkili molekülleri aramaya başladı ve tümör dokusunda beklenmedik şekilde bol bulunan yapısal bir protein olan TUBB3’e odaklandı.
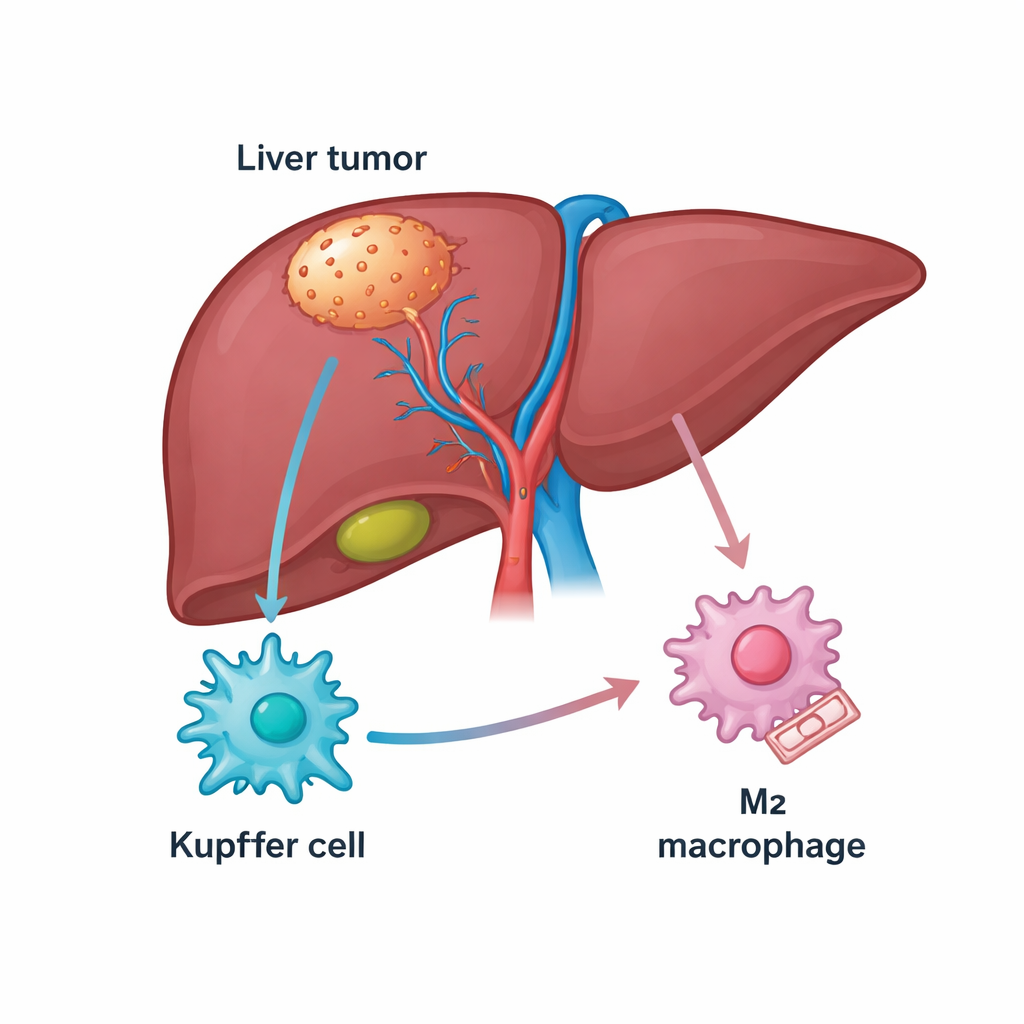
Makrofajları tümöre yardım edecek şekilde iten şaşırtıcı bir protein
TUBB3 hücre içindeki mikroskobik “rayların” bir yapı taşı olarak en iyi bilinir, ancak çeşitli kanserlerde agresif davranış ve ilaç direnci ile de ilişkilendirilmiştir. Burada araştırmacılar, TUBB3 düzeylerinin çevre sağlıklı dokuya kıyasla karaciğer tümörlerinde çok daha yüksek olduğunu ve daha fazla TUBB3’e sahip hastaların genellikle daha kısa sağkalıma sahip olduğunu buldu. Boyama teknikleriyle TUBB3’ün tümör içindeki Kupffer hücrelerinde özellikle zengin olduğunu ve varlığının tümöre yardım eden M2 belirteçleriyle güçlü şekilde korele olduğunu gösterdiler. Başka bir deyişle, TUBB3 ile dolu Kupffer hücreleri bağışıklık saldırısını hafifleten ve kanser büyümesini destekleyen davranışlara daha yatkındı.
Makrofajları yeniden programlayarak karaciğer tümörlerini dizginlemek
Neden-sonuç ilişkisini test etmek için ekip laboratuvar deneylerinde Kupffer hücrelerindeki TUBB3 düzeylerini düşürdü. TUBB3 baskılandığında, bu hücreler daha az M2-tipi sinyal, daha fazla M1-tipi sinyal üretti ve normalde bağışıklık aktivitesini baskılayan molekülleri daha az salgıladı. Bu yeniden programlanmış makrofajlara maruz kalan karaciğer kanseri hücreleri daha yavaş büyüdü, daha az bölündü ve göç ile invazyon kapasiteleri azaldı. Farelerde, karaciğer kanseri hücrelerini TUBB3 eksik Kupffer hücreleri ile karıştırmak daha küçük tümörlere, daha fazla kanser hücresi ölümüne ve yıkıcı proteinlerle donanmış daha fazla katil CD8 T hücresinin tümöre girmesine yol açtı. Makrofajlar hayvanlardan tamamen uzaklaştırıldığında TUBB3 bloke etmenin yararı büyük ölçüde kayboldu; bu da etkinin yalnızca kanser hücrelerinden ziyade bu bağışıklık hücreleri aracılığıyla gerçekleştiğini vurguluyor.
Önemli bir sinyal yolunda içsel bir frenin keşfi
Çalışma ayrıca TUBB3’ün bu etkiyi nasıl uyguladığını inceledi. Yazarlar, makrofajların M1 ya da M2 kimliğini de şekillendiren PTEN ve AKT proteinleri tarafından kontrol edilen iyi bilinen bir büyüme ve hayatta kalma yoluna odaklandı. TUBB3’ü düşürmenin PTEN’i artırdığını, bunun da AKT üzerindeki aktive edici “fosfat etiketlerini” azalttığını ve makrofajları tümörle savaşan duruma doğru ittiğini buldular. AKT’yi yapay olarak yeniden aktive ettiklerinde, makrofajlar M2 desenine geri döndü ve kanser hücreleri TUBB3 yokluğunda bile saldırgan davranışlarını yeniden kazandı. Bu, TUBB3’ün makrofaj davranışı için PTEN ve AKT’nin üzerinde bir tür içsel düğme olduğunu gösteriyor.
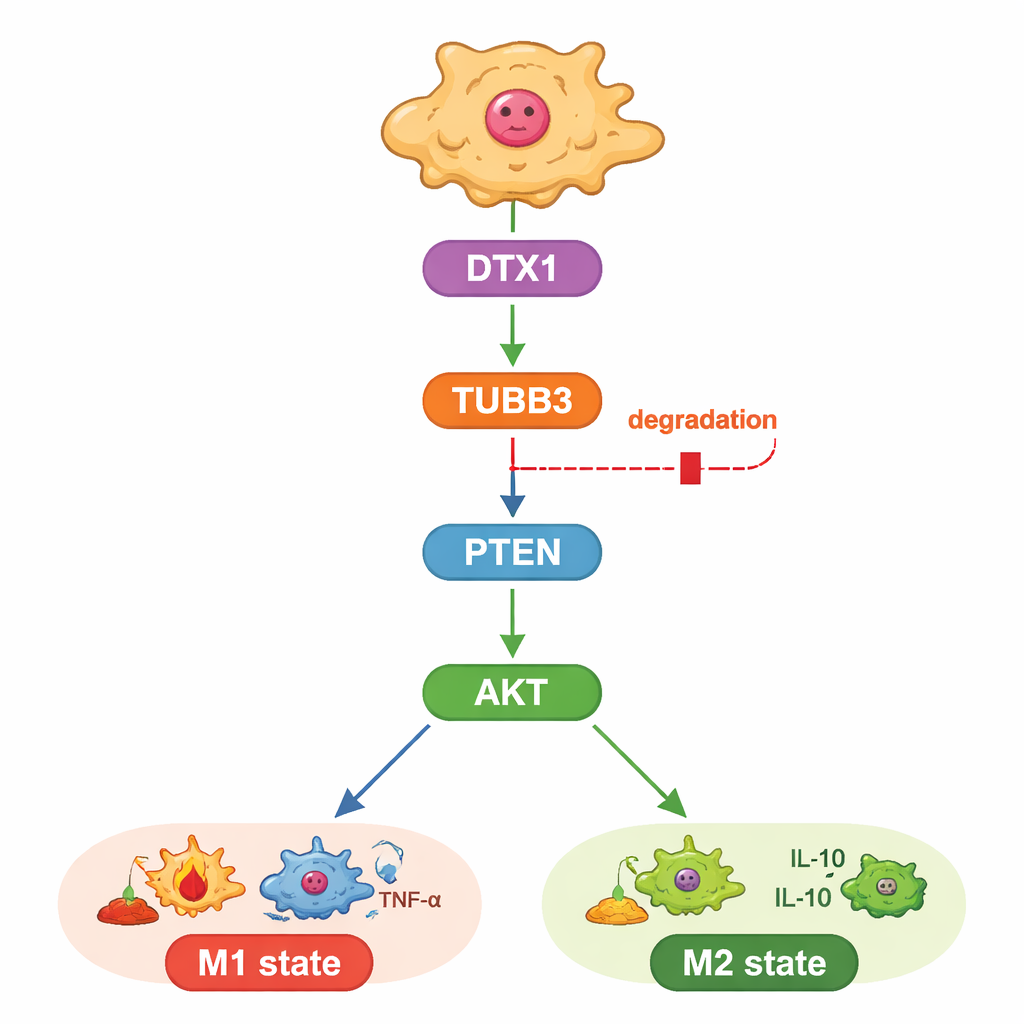
Yeniden açılabilecek içine gömülü bir çöp etiketi
Son olarak araştırmacılar, TUBB3’ün karaciğer tümörlerinde neden bu kadar bol olduğunu sordular. Biyoenformatik tahminleri ile ifade verilerini birleştirerek proteinleri yok edilmek üzere etiketleyen bir aileden enzim olan DTX1’i muhtemel bir düzenleyici olarak tanımladılar. DTX1 düzeyleri karaciğer tümörlerinde sağlıklı dokuya göre daha düşüktü ve daha iyi hasta sonuçları ile M1-tipi makrofaj varlığıyla ilişkiliydi. Hücrelerde DTX1’i artırmak TUBB3 yıkımını hızlandırdı, AKT aktivitesini azalttı ve makrofajları tümörle savaşan duruma itti; bu da kanser hücresi büyümesini sınırladı. Ekstra TUBB3 yeniden verildiğinde DTX1’in faydaları hem kültürde hem de fare tümörlerinde ortadan kalktı. Bu bulgular DTX1’den TUBB3 ve PTEN/AKT’ye kadar uzanan ve tümörün immün tonunu belirleyen açık bir hattı çiziyor.
Gelecekteki karaciğer kanseri tedavisine etkileri
Uzman olmayanlar için temel mesaj şudur: Bu çalışma, karaciğer yerleşik bağışıklık hücreleri içinde onların kanserle yardım mı yoksa zarar mı verdiğini belirleyen daha önce gizli bir kontrol sistemini tanımlıyor. Çöp-etiketleme enzimi DTX1 düşük olduğunda TUBB3 birikir, bir büyüme yolu aktive olur ve Kupffer hücreleri immünoterapinin etkisini azaltan tümör-destekleyici bir moda kayar. Bu yolu geri getirmek —TUBB3’ü düşürmek, DTX1’i artırmak veya PTEN/AKT sinyalini dikkatli şekilde ayarlamak— yerel bağışıklık savunmasını yeniden uyandırabilir ve PD-1 engelleyiciler gibi tedavileri daha etkili kılabilir. Bu stratejiler hâlâ deneysel aşamada olsa da, yalnızca tümör hücrelerini değil, karaciğer kanserinin seyrini güçlü biçimde etkileyen çevresindeki bağışıklık “komşularını” da hedeflemenin vaatlerini vurguluyor.
Atıf: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Anahtar kelimeler: hepatosellüler karsinom, tümör ilişkili makrofajlar, Kupffer hücreleri, immünoterapi, AKT sinyalleşmesi