Clear Sky Science · tr
Geri dönebilen YAP ve mitojen kontrolüyle siklin D1/p27 oranının geçici çoğalması
Dokuların Ne Zaman Büyüyeceğini Nasıl Bildiği
Derinizi kestiğinizde veya bir organ zarar gördüğünde, çevredeki hücreler kısa süreliğine dinlenme halinden onarım moduna geçer; yarayı yamamak için yeterli sayıda çoğalır ve sonra tekrar dururlar. Bu makale görünüşte basit bir soruyu ele alıyor: hücreler ne zaman bölünmeye başlayacaklarını ve aynı derecede önemli olarak ne zaman duracaklarını nasıl bilirler, böylece iyileşme kanser benzeri aşırı büyümeye dönüşmez? Araştırmacılar, güçlü bir büyüme sinyalini yalnızca geçici olarak açıp ardından güvenilir şekilde kapatan hücre içi yerleşik bir denge mekanizmasını ortaya koyuyorlar.
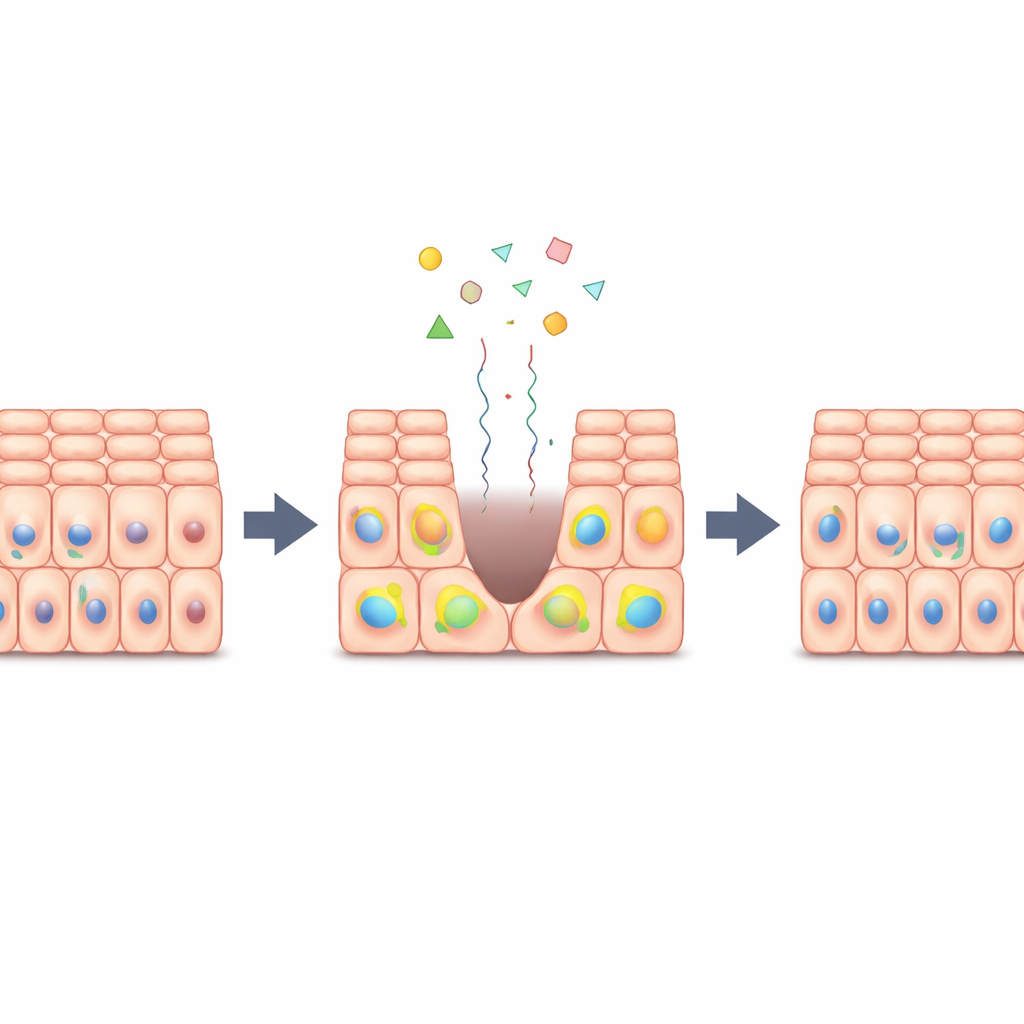
Hücre Bölünmesi İçin Bir Trafik Lambası
Birçok dokuda Hippo–YAP olarak adlandırılan moleküler bir sistem hücre büyümesi için bir trafik kontrolörü gibi davranır. Dokular sıkışık ve sağlam olduğunda Hippo, YAP adlı bir proteini çekirdeğin dışında tutar ve hücreler sessiz kalır. Doku yaralandığında veya gerildiğinde Hippo gevşer, YAP çekirdeğe girer ve hücreler bölünmeye teşvik edilir. Yazarlar, düz levhalar halinde yetiştirilen binlerce epitel hücresini çeşitli büyüme faktörleri (mitojenler), ilaçlar ve hücre yoğunlukları kombinasyonlarına maruz bıraktılar. Büyüme faktörü sinyallerinin, fiziksel sıkışıklığın ve YAP aktivitesinin ayrı çalışmadığını; bunun yerine hücrelerin her birinin hücre döngüsüne yeniden girip girmeyeceğini belirleyen tek bir iç karar noktasında birleştiğini buldular.
Hücre İçindeki Anahtar Oran
Ana bulgu, hücrelerin G1 olarak bilinen erken büyüme evresinde çekirdek içindeki iki proteinin oranına göre bölünmeye karar verdiğidir. Bir protein, siklin D1, hücreyi bölünmeye doğru iter; diğeri, p27, bir fren görevi görür. Her iki proteinin mutlak miktarından ziyade önemli olan siklin D1/p27 oranıdır. Bu oran kritik bir eşik değerin üzerine çıktığında, Rb adlı bir kapı bekçisi proteini fosforlanır ve DNA replikasyonu için gerekli makineyi serbest bırakarak hücrenin ilerlemesine izin verir. Bu eşiğin altında hücre dinlenme halinde kalır. Ekip, YAP’ı yapay olarak aktive etmenin veya Hippo yolundaki yukarı akış frenlerini engellemenin siklin D1/p27 oranını tutarlı şekilde yükselttiğini ve normalde hücreleri sessiz tutan koşullar altında bile hücreleri bu eşiğin ötesine ittiğini gösterdi.
Dışarıdan Gelen Sinyallerin Nasıl Güçlendiği ve Sonra Söndüğü
YAP tek başına hareket etmez: hücrenin dışarıdan gelen büyüme sinyallerine yanıt verme duyarlılığını artırır. Araştırmacılar, RNA dizileme ve protein ölçümleri kullanarak YAP’ın hücre yüzeyindeki reseptör proteinlerin sayısını ve aktivitesini artırdığını, EGFR ailesi üyeleri ve diğer reseptör tirozin kinazlarını da kapsadığını gösterdiler. Bu reseptörler MEK–ERK gibi klasik büyüme yollarına ve daha az oranda mTOR’a bilgi iletir; bunlar siklin D1’i yükseltir ve p27’yi düşürerek iç oranı bölünmeye doğru eğimli hale getirir. Önemli olarak, bu artış hızlı bir açma-kapama düğmesi değildir. YAP aktivitesi engellendikten sonra bile yükselmiş reseptör sinyallemesi ve artmış siklin D1/p27 oranı saatler boyunca ancak yavaşça azalır; bu da frenler tamamen yeniden uygulanmadan önce hücrelere sınırlı bir bölünme turunu tamamlamaları için zaman tanır.
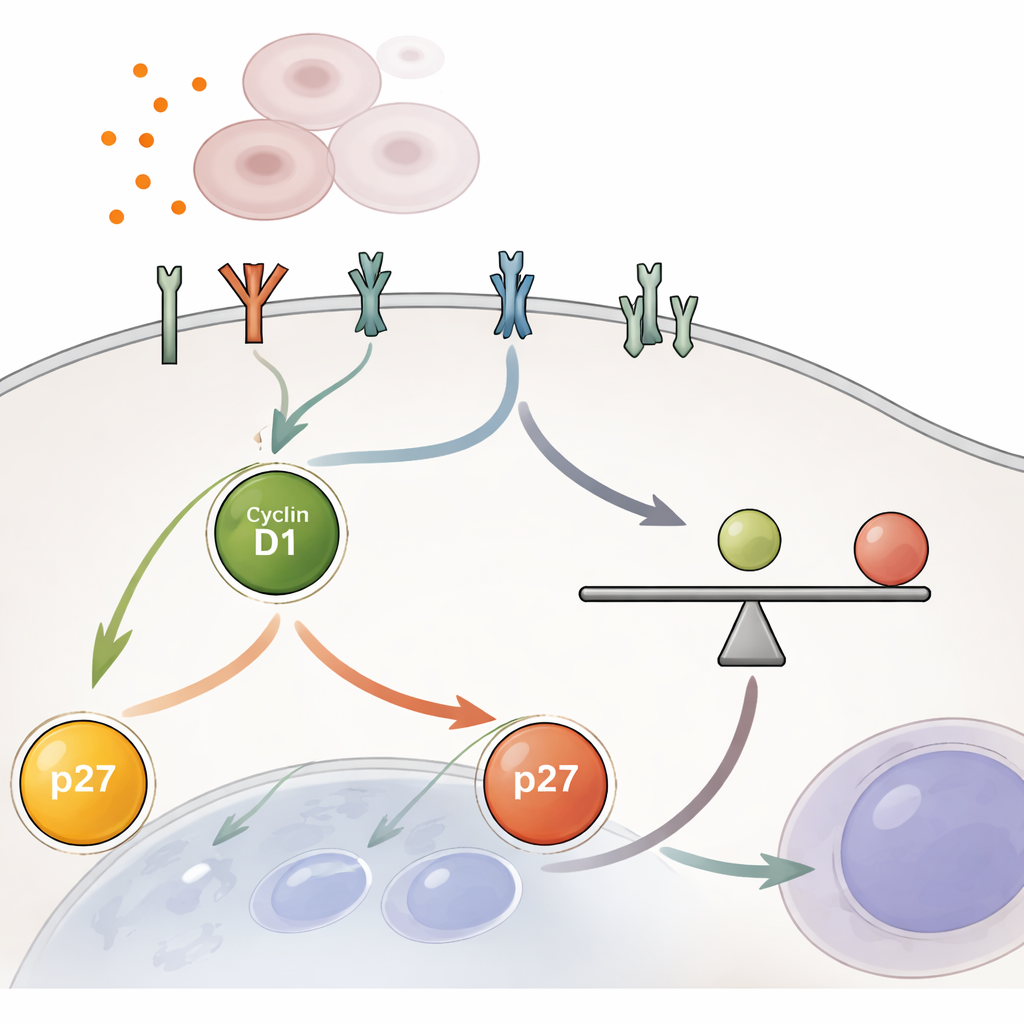
Sınırsız Büyümeye Karşı Yerleşik Güvenlik Mekanizmaları
Çalışma ayrıca YAP üzerindeki doğal frenler zayıfladığında neler olduğunu inceliyor; bu durum bazı tümörlerde görülür. Normalde Hippo’yu aktive etmeye yardımcı olan bağlanma proteini Merlin’in ortadan kaldırılması, YAP’ı kısmen serbest bıraktı ve hücreleri büyüme faktörlerine karşı daha duyarlı hale getirdi. Ancak bu hücreler bile çok yüksek yerel hücre yoğunluğuyla kapatılabildi; bu durum temas inhibisyonunu geri getirdi ve siklin D1/p27 oranını düşürdü. Bu, sistemin birden çok kontrol katmanına sahip olduğunu gösteriyor: yüzey reseptörleri, Hippo–YAP ve siklin D1/p27 oranı, hücrelerin bölünmeye devam edip etmeyeceği kararına birlikte katkıda bulunur.
İyileşme ve Kanser Açısından Önemi
Genel okuyucu için önemli mesaj şudur: doku onarımı geçici, kendini sınırlayan bir büyüme programıyla yönlendirilir. YAP aktivasyonu ve artmış reseptör sinyallemesi siklin D1/p27 oranını bir eşik değerinin üzerine çıkarır, böylece hücreler bölünüp hasarı onarabilir. Hücreler bölünüp doku tekrar sıkıştıkça temas inhibisyonu yavaşça YAP ve reseptör sinyallemesini kapatır, oran düşer ve bölünme durur. Bu zamanlama mekanizması bozulduğunda —örneğin sürekli YAP aktivasyonu veya yukarı akış frenlerin kaybıyla— hücreler sıkışıklığa duyarsız hale gelip bölünmeye devam edebilir; bu da kanamere yol açan bir adım olabilir. Bu oran temelli karar mekanizmasının anlaşılması, kontrolsüz büyümeyi tetiklemeden güvenli şekilde onarımı artıracak rejeneratif terapilerin tasarlanmasına yardımcı olabilir.
Atıf: Ferrick, K.R., Upadhya, S.W., Fan, Y. et al. Transient proliferation by reversible YAP and mitogen control of the cyclin D1/p27 ratio. Commun Biol 9, 340 (2026). https://doi.org/10.1038/s42003-026-09590-2
Anahtar kelimeler: YAP sinyalizasyonu, hücre döngüsü kontrolü, doku rejenerasyonu, temas inhibisyonu, siklin D1 p27 dengesi