Clear Sky Science · tr
WRN helikazına dair yapısal bilgiler konformasyonel durumları ve MSI‑H kanser ilaç keşfi için fırsatları ortaya koyuyor
Kanser tedavisi açısından bunun önemi
Bazı kanserlerin yerleşik bir zayıflığı vardır: DNA’larındaki hataları onarmakta zorlanırlar. WRN helikaz adlı bir protein, bu kırılgan tümörleri hayatta tutan moleküler bir onarım aracı gibi davranır. Bu çalışma, WRN’nin DNA boyunca nasıl hareket ettiğini ve deneysel ilaçların bu hareketi nasıl tıkayabildiğini atomik ayrıntıda ortaya koyarak, bu kırılgan kanser hücrelerini seçici olarak öldürüp sağlıklı dokuyu koruyabilecek yeni tedavilere yönelik bir yol haritası sunuyor.
Mikroskop altındaki DNA tamircisi
WRN helikaz, DNA’nın açılmasına yardımcı olarak hasarın tespit edilmesi ve onarılmasını sağlayan hücrenin bakım ekibinin bir parçasıdır. Çalışan WRN olmayan kişiler Werner sendromu geliştirir; bu, erken yaşlanma ile karakterize nadir bir bozukluktur ve proteinin genom bakımındaki önemini gösterir. Kolorektal ve bazı diğer kanserlerde sık görülen "mikrosatellit kararsızlığı–yüksek" (MSI‑H) tümörlerin WRN’ye özellikle bağımlı olduğu ortaya çıkmıştır. Bu hücrelerde WRN kapatıldığında, zaten hassas olan DNA hızla dağılır ve kanser hücreleri ölür. Bu durum WRN’yi cazip bir ilaç hedefi haline getirir, ancak proteinin DNA’yı kavradığı, kimyasal yakıt kullandığı ve genetik madde üzerinde ilerlediği sırada nasıl şekil değiştirdiğine dair net bir görüş şimdiye dek yoktu.
WRN’in esnemesini ve nefes alışını izlemek
Yazarlar, insan WRN helikaz çekirdeğinin birkaç yüksek çözünürlüklü "anlık görüntüsünü" yakalamak için X‑ışını kristalografisini kullandılar. WRN’nin yalnız hallerinin yanı sıra tek sarmallı DNA’ya ve kırılmayan bir ATP‑benzeri yakıt molekülüne bağlı yapıları çözdüler. Bu görünümler, proteinin esnek bir menteşe gibi davranan iki ana loba sahip olduğunu ve bu lobların bir nefes alma eklemi gibi hareket ettiğini ortaya koydu. Dinlenme hâlinde, yakıt yokken WRN, lobların birbirine yakın oturduğu kompakt bir "kapalı" formu benimser. ATP‑benzeri yakıt ve DNA varlığında, loblar DNA’yı pozitif yüklü bir oluğa kucaklayabilecek daha "açık" bir konfigürasyona doğru savrulur. WRN içindeki küçük bir aromatik döngü kısa bir heliks haline gelir ve DNA bazları arasına girerek geri kaymayı engelleyen bir palangaya (ratchet) benzer şekilde ilerlemeye yardımcı olur.
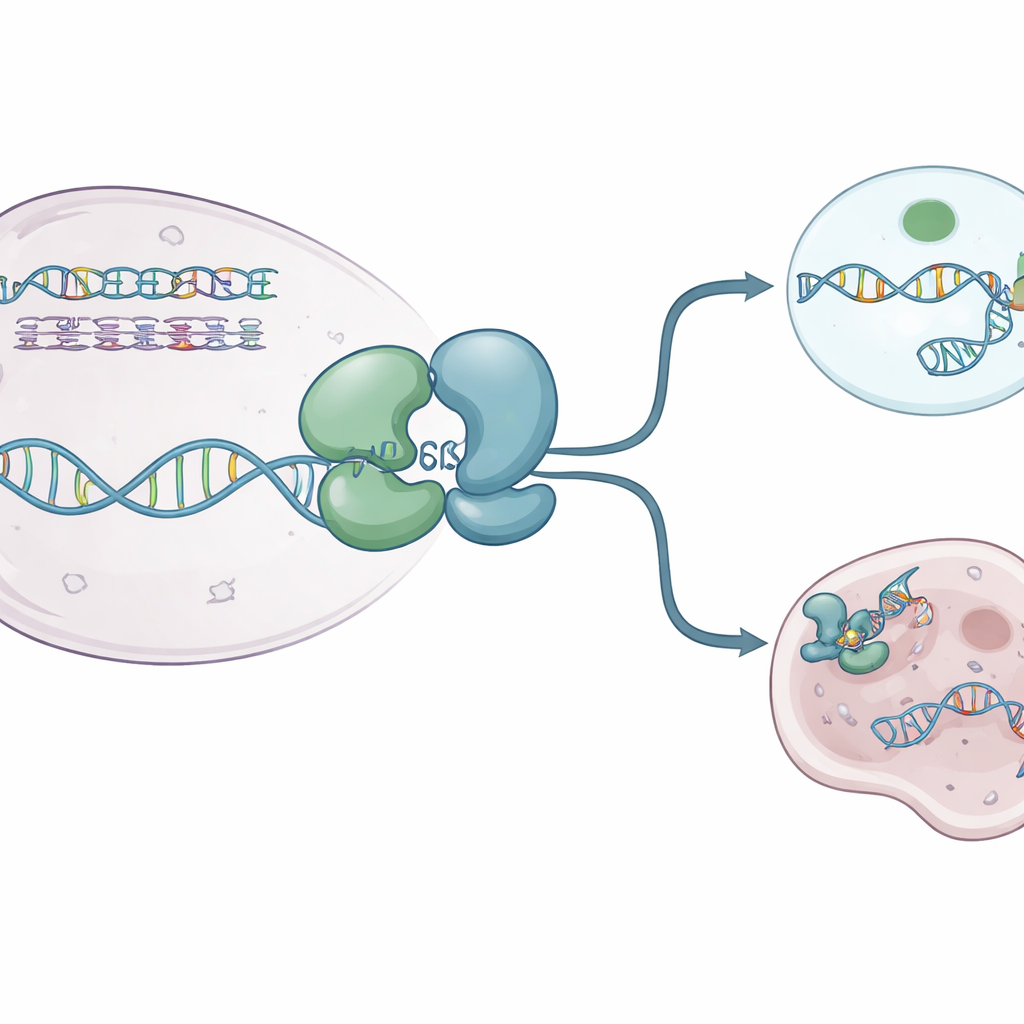
Mevcut ilaçlar WRN’i nasıl kapatıyor
Birkaç WRN‑engelleyen bileşik yakın zamanda klinik testlere girdi. Bunlar proteinin aktif oluğunu doğrudan tıkamıyor. Bunun yerine uzaktan etki ederek menteşe bölgesini kavrar ve WRN’yi DNA’yı uygun şekilde kavrayamayan şekillere kilitlerler. HRO761 ve GSK’dan ilişkili bir klinik aday gibi bazı moleküller bir lobu diğerine göre yaklaşık 180 derece çevirerek DNA’dan uzak duran dramatik bir "bükülmüş" form yaratır. VVD‑133214 ve burada incelenen yakın ilişkili bir bileşik gibi diğerleri ise WRN’yi anahtar DNA kavrama yüzeylerini açığa çıkaramayan sıkı bir "kapalı" düzenlemeye sabitler. Biyofiziksel deneyler, bu ilaçlar bağlandığında WRN’nin tek sarmallı DNA ile artık stabil bir kompleks oluşturamadığını, böylece ATP kullanımını DNA açılmasından ayırdığını doğruladı.
Kanser hücreleri nasıl kaçmayı öğreniyor
Tümörlerin bu ilaçlardan nasıl kaçabileceğini görmek için ekip, MSI‑H kolorektal kanser hücrelerini WRN inhibitörlerinin varlığında haftalarca ila aylarca büyüttü. Dirençli populasyonlar hızla ortaya çıktı. Genetik analiz, her durumda hücrelerin ilaç bağlanan menteşe yakınında WRN geninde tek, belirli bir değişiklik kazandığını gösterdi. Bir mutasyon "bükülmüş durum" inhibitörü HRO761’in etkisini zayıflatırken, farklı bir mutasyon VVD‑133214’e karşı duyarlılığı azalttı; bu bileşik kapalı durumu tercih ediyor. Ayrıca birçok dirençli hücre WRN üretimini arttırarak hedefin daha fazla kopyasını elde etti ve böylece ilacın etkisini kısmen seyreltmiş oldu. Bu bulgular, hedef proteindeki küçük yapısal değişikliklerin veya aşırı ifade edilmenin tedaviyi körelttiği diğer hedefe yönelik kanser ilaçlarında görülen direnç örüntülerini yansıtıyor.
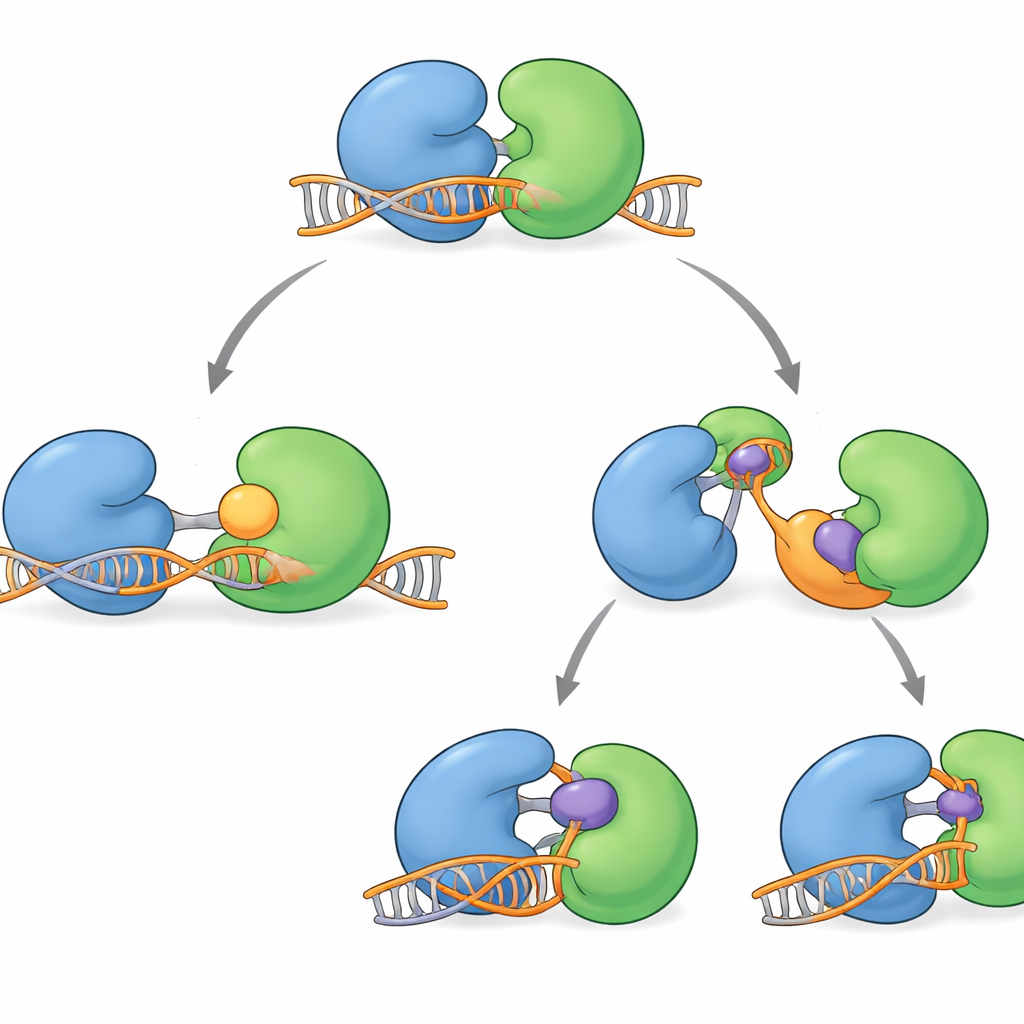
Daha akıllı WRN engelleyicilerine doğru
Yeni yapılar bir arada ele alındığında, WRN’nin DNA’ya tutunup ilerlediği ve sonra sıfırladığı tam bir çalışma döngüsünü haritalandırıyor. Ayrıca bugünkü klinik bileşiklerin çoğunun proteinin "DNA‑dışı" formlarını stabilize ettiğini gösteriyor. Genel okuyucu için ana nokta, artık WRN’nin nereden savunmasız olduğunu ve tümörlerin nasıl uyum sağlayabileceğini anlamış olmamızdır. Bu, WRN’nin DNA’ya sıkı tutunduğu anda bağlanan, onu toksik bir durumda hapsetme potansiyeli olan bir sonraki nesil inhibitörleri öneriyor—diğer DNA onarım enzimlerini tuzağa düşüren başarılı ilaçlara benzer şekilde. Böyle "DNA‑üzerinde" WRN engelleyicileri, tek başına veya mevcut ajanlarla birlikte kullanıldığında, MSI‑H kanserlerin gizli zayıflığından yararlanmanın daha kalıcı yollarını sunabilir.
Atıf: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Anahtar kelimeler: WRN helikazı, mikrosatellit kararsızlığı, DNA onarımı, allosterik inhibitörler, ilaç direnci