Clear Sky Science · tr
CISH: hücre içi kilit bir kontrol noktası, mevcut ve yeni kanser immün kontrol noktalarıyla karşılaştırma ve kombinasyon
Kanserle Savaşan Hücrelerdeki Frenleri Serbest Bırakmak
Kanser immünoterapileri birçok hasta için görünümü değiştirdi, ancak büyük bir hasta grubu hâlâ çok az veya hiçbir fayda görmüyor. Bu çalışma, vücudun kendi T hücrelerini—immün sistemin tetikçilerini—güçlendirmek için yeni bir yolu araştırıyor: CISH adlı içsel bir “fren”i devre dışı bırakmak. Hücre yüzeyindeki anahtarlara etki eden mevcut ilaçların aksine, bu strateji hücre içinde gömülü bir kontrol sistemini hedefliyor; amaç, mühendislikli T hücrelerini tümörleri bulma ve yok etme konusunda çok daha yetenekli hâle getirmek, kanserler saklanmaya çalışsa bile.
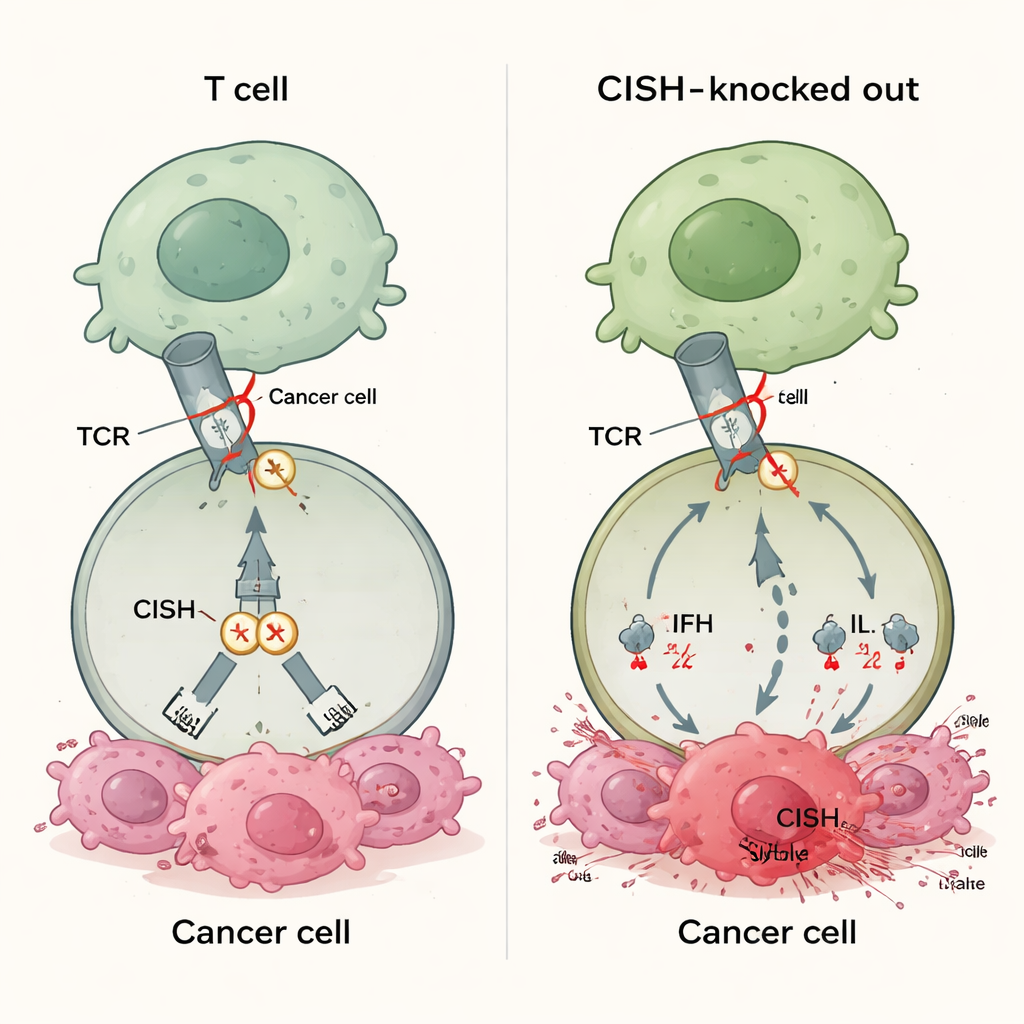
Yeni Tür Bir İmmün Fren
Onaylı immünoterapi ilaçlarının çoğu T hücrelerinin yüzeyindeki PD-1 gibi proteinleri bloke eder. Bu ilaçlar, tümörler eşleşen partner moleküllerini (ör. PD-L1) gösterdiğinde etkilidir ve birçok kanser ya bu partnerleri yeterince hiç ifade etmez ya da zamanla kaybeder. Bu durum, hastaların %30–60’ının günümüz kontrol noktası terapilerine yanıt vermemesini kısmen açıklar. CISH, T hücresi içinde yer alan ve farklı bir fren sınıfına ait bir proteindir. T hücresi reseptörü bir hedefi algıladığında CISH açılır ve ardından anahtar bir sinyal proteininin yıkımını teşvik ederek sinyali zayıflatır. Bu eylem tümör tarafından ifade edilen ligandlara bağlı olmadığından, CISH’in kapatılması teoride PD-L1 durumu veya diğer biyobelirteçlerden bağımsız olarak birçok kanser türünde T hücresi yanıtlarını artırabilir.
Mevcut Kontrol Noktalarıyla Yüz Yüze
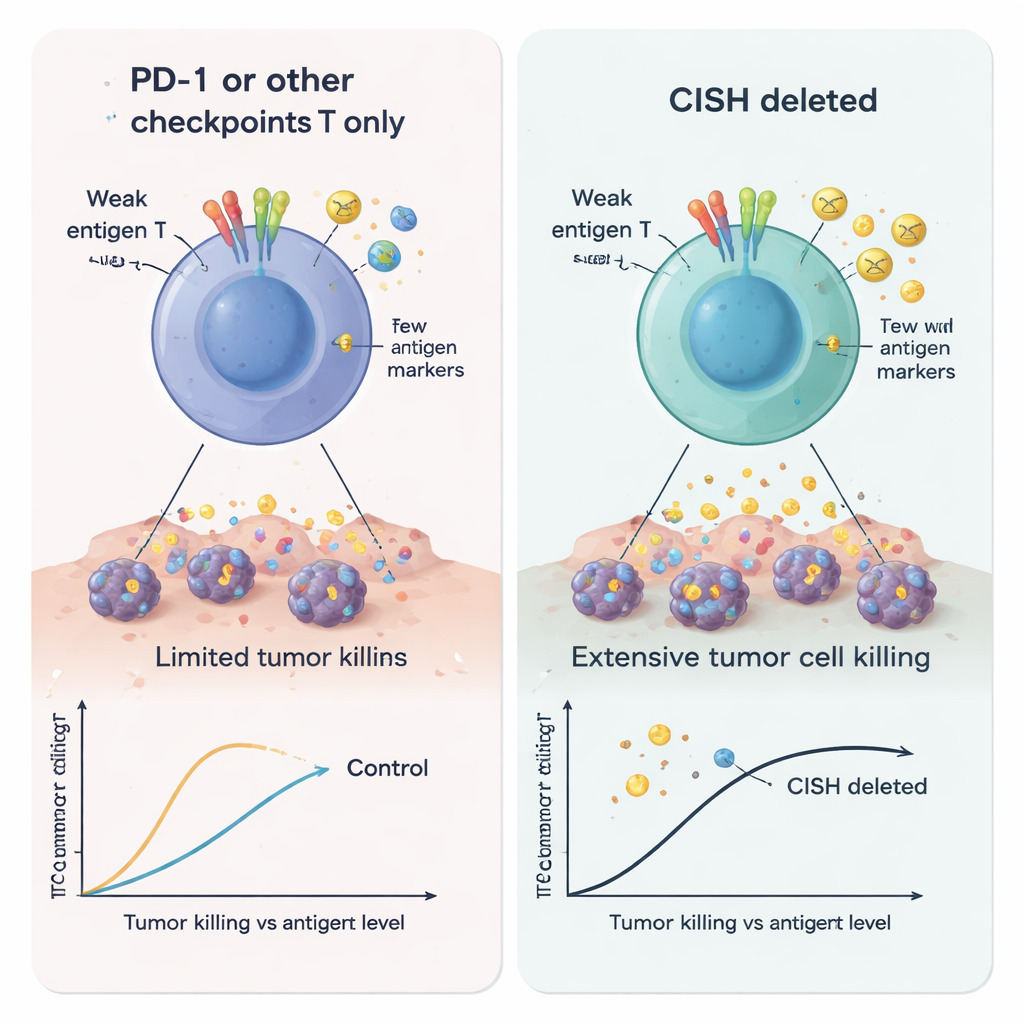
Araştırmacılar CISH’i ortadan kaldırmak için CRISPR gen düzenlemesini kullandılar ve ortaya çıkan T hücrelerini PD-1’den veya diğer bazı hücre içi frenlerden yoksun hücrelerle karşılaştırdılar. T hücrelerini zayıf şekilde uyardıklarında—sadece az miktarda antijen gösteren tümörleri taklit etmesi amaçlanan bir durum—CISH silinmiş hücreler interferon-gamma, TNF-alfa ve IL-2 dahil olmak üzere çok daha fazla ana immün haberci üretti. Bu hücreler ayrıca daha “çok işlevli”ydi; yani bireysel T hücreleri aynı anda birkaç görevi yerine getirebiliyordu ki bu, güçlü antitümör aktivitenin bir işaretidir. Buna karşılık, yalnızca PD-1’in çıkarılması bu düşük sinyal koşullarında yardımcı olmadı. Birçok testte, CISH kaybı aktivasyonu, öldürme kapasitesini ve dayanıklı bellek-benzeri T hücrelerinin oluşumunu RASA2, CBLB, SOCS1, REGNASE1, HPK1 veya PTPN1/2 gibi diğer aday iç kontrol noktalarının yok edilmesinden daha güçlü şekilde artırdı.
Diğer İç Anahtarlarla Birlikte Çalışmak
T hücresi sinyalleşmesi birçok örtüşen yol tarafından kontrol edildiğinden ekip, CISH silinmesinin diğer frenlerin kaldırılmasıyla kombinasyon halinde ek faydalar sağlayıp sağlamayacağını sordu. Çoklu CRISPR düzenleme kullanarak, CISH ile birlikte SOCS1, HPK1 veya RASA2’nin silinmesinin zayıf uyarım altında faydalı sitokin üretimini daha da artırdığını buldular. Yaygın bir KRAS mutasyonuna dayalı tümör modelinde, KRAS-spesifik bir reseptörle mühendisliklenen T hücreleri CISH kaldırıldığında kanser hücrelerini daha iyi öldürdü ve bu etki CISH kaybı SOCS1 veya RASA2 silinmesiyle eşleştirildiğinde daha da güçlendi. Bu bulgular, CISH’in T hücresi biyolojisinde yedeklenmeyen bir düğümü kontrol ettiğini ve seçili ortaklarla iş birliği yaparak tümör-spesifik öldürmeyi keskinleştirebileceğini öne sürer.
Kaçak Tümörlere Karşı CAR-T Hücrelerini Daha Dayanıklı Kılmak
Yazarlar daha sonra klinik açıdan önemli bir duruma yöneldiler: B hücre belirteci CD19’u hedefleyen CAR-T hücreleri. Tedaviden kaçmak için hedeflerini düşüren veya azaltan tümörleri taklit etmek amacıyla farklı CD19 düzeyleri ifade eden lösemi hücreleri oluşturdular. CISH eksik CAR-T hücreleri, CD19 az olduğunda bile kanser hücrelerini yok etmede belirgin biçimde daha iyiydi ve daha fazla aktive edici ve çekici sinyal salgıladı. Aynı zamanda Galectin-1, Galectin-3, çözünebilir 4-1BB, IL-1α ve glikoprotein EMMPRIN/CD147 gibi T hücrelerini zayıflatan veya tümör büyümesini teşvik eden moleküllerin daha düşük miktarlarını serbest bıraktılar. Birlikte, bu değişiklikler özellikle düşman, düşük antijenli tümör ortamlarına uygun daha agresif ve daha az kolay baskılanabilen bir CAR-T hücresine işaret ediyor.
Laboratuvardan Hastalara
Deney tüpleri ve kültür kaplarının ötesinde, CISH’i hedefleme fikri zaten hastalara ulaşmış durumda. İleri evre kolorektal kanseri olan bir kişide CISH’i çıkarmak üzere düzenlenmiş tümör-infiltre edici lenfositleri kullanan ilk insan denemesi, çoklu önceki tedavilere dirençli olmasına rağmen iki yılı aşkın süredir devam eden tam yanıt üretti. CISH’in zayıf tümör sinyallerine karşı bile T hücresi duyarlılığını artıran güçlü, ilaca dönüştürülebilir bir iç kontrol noktası olduğunu göstermesiyle bu çalışma, o dikkate değer klinik sonucu açıklamaya yardımcı oluyor ve gen düzenlenmiş hücreler ya da ilaçlar olsun, bu iç freni güvenli şekilde gevşetecek ve kanser immünoterapisinin kapsamını genişletecek gelecekteki tedavilerin geliştirilmesini destekliyor.
Atıf: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Anahtar kelimeler: kanser immünoterapisi, T hücreleri, CAR-T tedavisi, immün kontrol noktaları, CRISPR gen düzenleme