Clear Sky Science · tr
α-SNAP’taki patojenik bir mutasyon, kritik bir hidrofobik döngüyü gizleyerek membran lipidlerine bağlanmayı bozar
Minik Bir Protein Değişikliği Beyin Gelişimini Nasıl Bozabilir
Beyin hücrelerimiz, vezikül adı verilen küçük kabarcıklarla sürekli yük taşır ve alpha-SNAP adlı yardımcı bir protein bu teslimatların gerçekleşmesinde merkezi bir rol oynar. “hyh” adlı fare hattında bilinen nadir bir alpha-SNAP mutasyonu, beyin oluşumunda ve sıvı dengesinde ciddi sorunlara yol açar. Bu çalışma, büyük sonuçları olan basit görünümlü bir soruyu irdeliyor: alpha-SNAP’teki o tek harflik değişiklik, proteinin hücre membranlarına tutunmasını engelliyor mu ve bunun beyin bozukluklarının temel nedeni olma ihtimali var mı?
Birçok Görevi Olan Hücresel Bir İskele İşçisi
Alpha-SNAP normalde veziküller için bir tür iskele işçisi gibi çalışır; veziküllerin hücre membranlarıyla kaynaşmasına yardımcı olarak yükün salınmasını veya geri dönüştürülmesini sağlar. SNARE adı verilen bir protein seti ve NSF adlı enerji kullanan bir makine ile iş birliği yaparak membranları birbirine çeker ve ardından sistemi bir sonraki tur için resetler. Bu klasik rolün ötesinde, alpha-SNAP otofaji (hücrenin kendi kendini temizlemesi), hücre ölümü, kalsiyum girişi ve enerji algılama gibi süreçlerin düzenlenmesine de yardımcı olur. Tüm bu işlevler, bir şekilde alpha-SNAP’in membranların yağlı yüzeyine dokunma ve kısmen gömülme yeteneğine bağlıdır.
Gizli Bir Döngü ve Sorunlu Bir Mutasyon
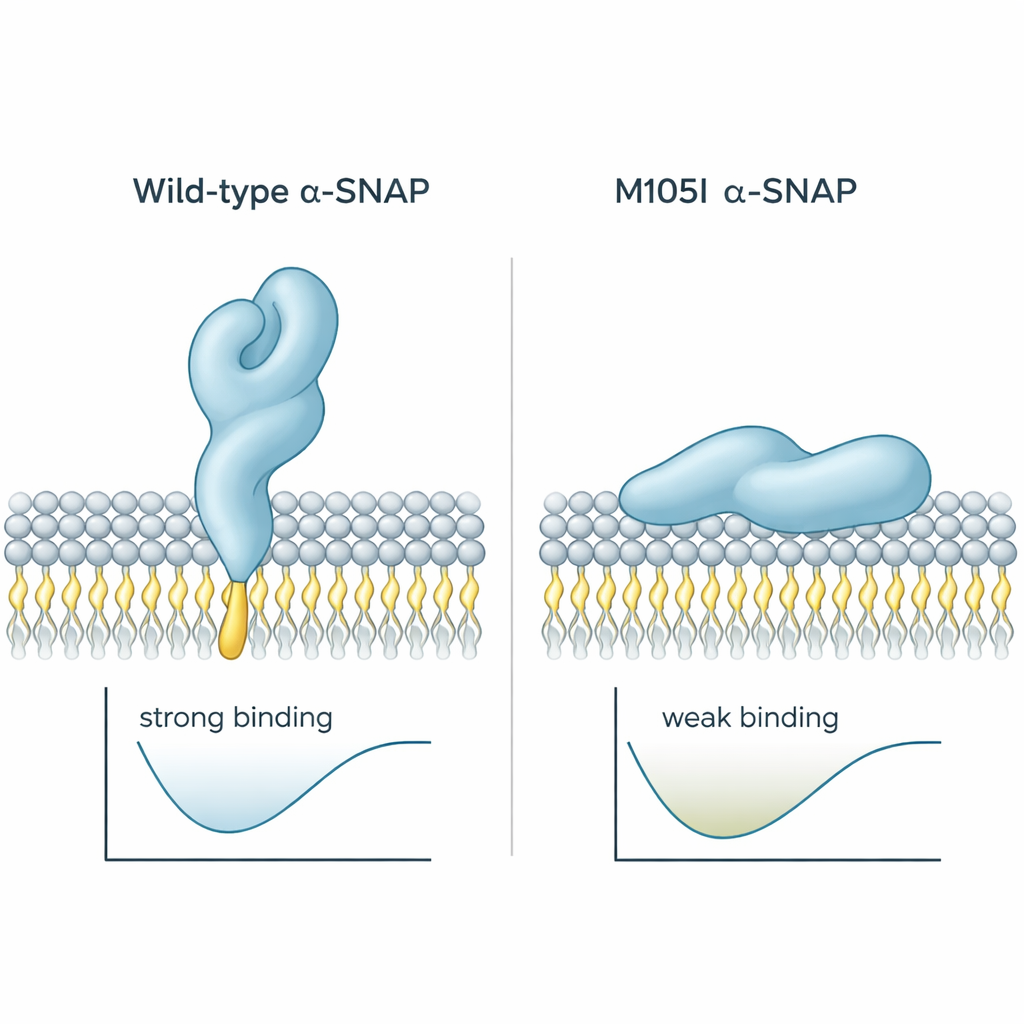
Daha önceki çalışmalar, alpha-SNAP’in proteinin bir ucuna yakın kısa, yağlı bir “döngü” kullanarak membranlara tutunduğunu göstermişti. Sağlıklı proteinde bu döngü dışarı doğru çıkar ve membranın dış tabakasına dalabilir. Hyh faresinde, 105 pozisyonundaki tek bir yapı taşı yer değiştirir ve M105I mutasyonu oluşur. Yazarlar, bu değişikliğin proteinin şeklini nasıl etkilediğini görmek için bilgisayar simülasyonları kullandılar. Mutant proteinin biraz daha kompakt hale geldiğini ve hidrofobik döngüyü su ve membranlardan uzak, içeri doğru saklayacak biçimde büküldüğünü buldular. Sonuç olarak, mutant protein membranlara daha yatay bir açıyla yaklaşır ve daha az yapışkan bir bölgeyle onlara bastırma eğilimindedir; bu da hem temas süresini hem de batma derinliğini azaltır. Bağlanma enerjisinin hesaplanması bunu destekledi: vahşi tip protein düşük enerjili, güçlü bağlı bir duruma yerleşirken mutant daha zayıf, yüzeysel temasları tercih etti.
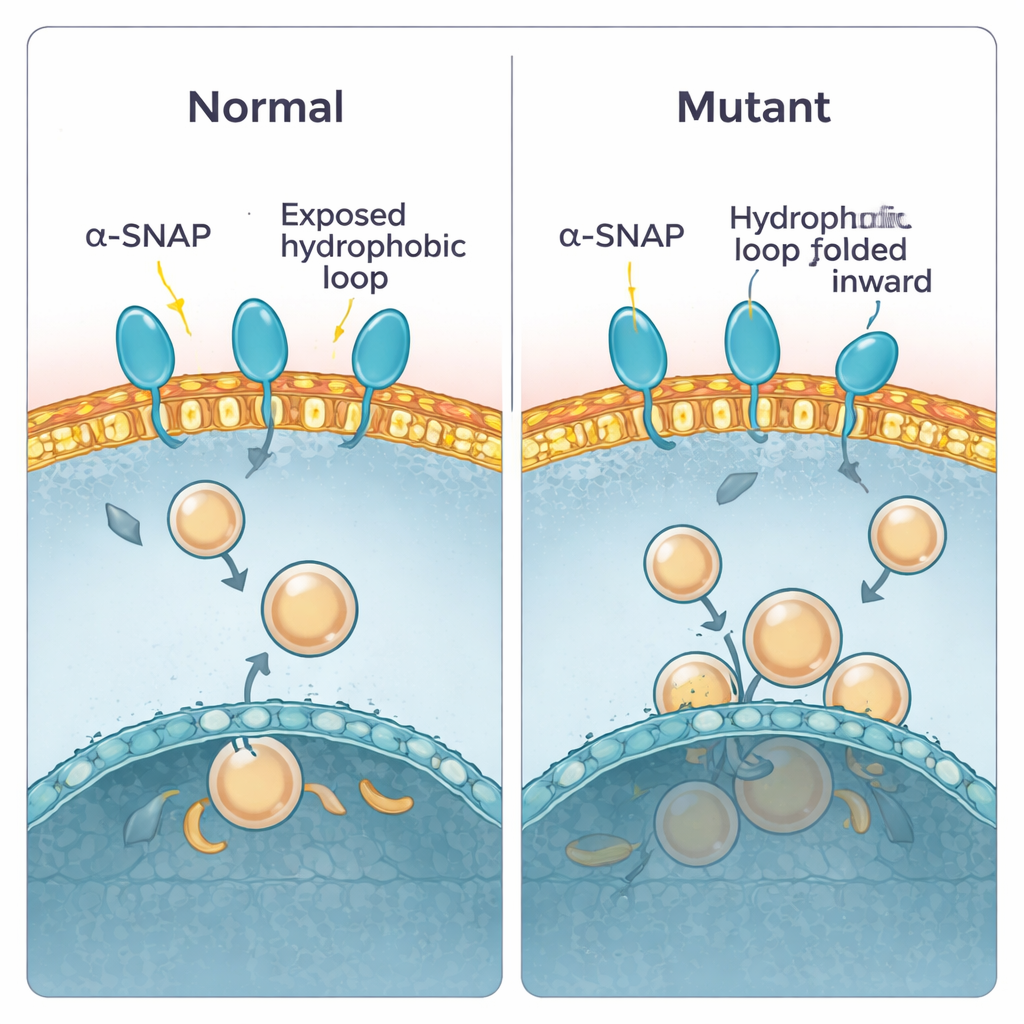
Tahmini Laboratuvarda Test Etmek
Bu tahminleri kontrol etmek için ekip hem normal hem de mutant alpha-SNAP’i saflaştırdı ve farklı deney düzenlerinde nasıl davrandıklarını test etti. Önce su ve yağ fazlarına ayrılan bir deterjan kullandılar; bu, su ile membran arasındaki tercihi taklit ediyordu. Normal alpha-SNAP dengeli bir şekilde bölündü; bu, kısmen yağlı bir yüzeye sahip olduğunu gösteriyordu. Mutant versiyon yağ fazına girmeye daha az istekliydi; bu da yağlı kısımlarının gerçekten daha gömülü olduğunu düşündürdü. Ardından, proteinlerin hücrelerden hazırlanmış düz plazma membran “sayfaları” ile etkileşmesine izin verdiler ve kaç bağlanma noktası oluştuğunu görüntülediiler. Yine, normal alpha-SNAP membranı noktalandırırken mutant çok daha az bağlandı. Son olarak, beyin lipitlerinden yapılmış yapay membran kabarcıkları (liposomlar) şeker gradyanlarında yüzdürdü. Vahşi tip alpha-SNAP, plazma membranı lipitleri zengin olan veziküllerle birlikte yukarı doğru hareket etti; oysa mutant geride kaldı ve veziküller farklı, daha içsel bir membran karışımından yapılmadıkça kötü bağlandı.
Gelişmekte Olan Beyindeki Sonuçlar
Araştırmacılar daha sonra, yeni nöronların doğduğu bir döneme odaklanarak gelişen fare embriyolarının beyinlerine yöneldiler. Hücre içeriklerini çözünebilir ve membrana bağlı havuzlar olarak ayırarak, hyh beyinlerinde toplam alpha-SNAP seviyelerinin zaten azaldığını, ancak daha önemlisi membrana bağlı fraksiyonun normal farelere kıyasla orantısız şekilde düşük olduğunu gösterdiler. Farklı membran tiplerini daha da ayırdıklarında, en büyük kaybın hücrenin dış yüzeyi olan plazma membranında olduğunu, iç membranların çok daha az etkilendiğini buldular. Mikroskopi aynı hikâyeyi anlattı: normal dokuda alpha-SNAP, bilinen bir yüzey belirteciyle eşleşen petek deseninde hücreleri çevreliyordu. Hyh beyinlerinde bu net sınır boyaması daha yaygın, içsel bir ışıltıya dönüştü; bu, mutant proteinin vezikül füzyonunun ve sinyal iletiminin en aktif olduğu hücre kenarında sabit kalamadığını gösteriyordu.
Hastalık Açısından Neden Önemli
Bir arada ele alındığında, çalışma M105I mutasyonunun sadece alpha-SNAP miktarını azaltmadığını; proteinin katlanma şeklini değiştirip ana membran-tutucu döngüsünü gizlediğini gösteriyor. Bu, alpha-SNAP’in plazma membranına tutunmasını ve füzyon makinelerini düzenlemek için doğru yönde durmasını zorlaştırır. Gelişmekte olan bir beyinde, hücre yüzeyindeki sinyallerin ve yapı malzemelerinin hassas tesliminin hayati olduğu yerde, bu ince yapısal kusur muhtemelen hyh farelerinde görülen hidrosefali, korteksin yanlış bağlantılanması ve diğer kusurlara katkıda bulunur. Uzman olmayanlar için mesaj açık: tek bir proteinin şeklindeki küçük bir değişiklik bile hücrelerin nasıl iletişim kurduğunu ve dolayısıyla bir beynin nasıl inşa edildiğini yeniden şekillendirebilir.
Atıf: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Anahtar kelimeler: alpha-SNAP, membran bağlanması, protein mutasyonu, beyin gelişimi, vezikül füzyonu