Clear Sky Science · tr
Kapaisin türevi prohibitin ligandlarının Aurora kinaz A/PHB2 etkileşimini ve kanser hücrelerinde mitofajiyi modüle etmek için geliştirilmesi
Neden bir acı biber kimyasalı kanser için önem taşıyor
Acı biberlerin yakıcı hissi, hücrelerimizdeki proteinlere bağlanan küçük bir molekül olan kapaisinden kaynaklanır. Bu çalışma, tanıdık baharatın şaşırtıcı bir dönüşümünü araştırıyor: araştırmacılar kapaisini yeniden tasarlayarak kansere özgü “enerji santralleri” olan mitokondrilere yönelen ve bu organellerin işleyişini dengede tutan bir süreci hafifleten yeni, ilaç benzeri moleküller geliştirdiler. Kanser hücreleri aşırı büyümeyi sürdürmek için verimli mitokondrilere büyük ölçüde güvenirdi; bu destek sistemini seçici olarak bozabilmek, yeni antikanser tedavileri için bir yol açabilir.
Hücresel enerji santralleri ve iç temizlik ekibi
Mitokondriler sürekli olarak yeni birimler inşa etmek ile hasarlı olanları geri dönüştürmek arasında denge kurar. Geri dönüşüm tarafı, mitofaji olarak adlandırılan kalite kontrol sistemi gibi çalışır: eskimiş mitokondriler işaretlenir ve parçalanırken daha sağlıklı olanlar kalır. Birçok kanser hücresi bu dengeyi ele geçirir ve mitofajiyi zayıf mitokondrileri elerken yüksek ATP üreten “süper-performans”lı mitokondrileri zenginleştirmek için kullanır. Tümörlerde sıkça aşırı üretilen Aurora kinaz A (AURKA) adlı bir proteinin, yakın zamanda mitokondriler içinde bulunduğu ve Prohibitin‑2 (PHB2) ile otofaji adaptörü LC3 ile iş birliği yaptığı saptandı. Birlikte mitofajiyi teşvik eden ve kanser hücrelerinde yüksek enerji çıktısını destekleyen bir kompleks oluştururlar.
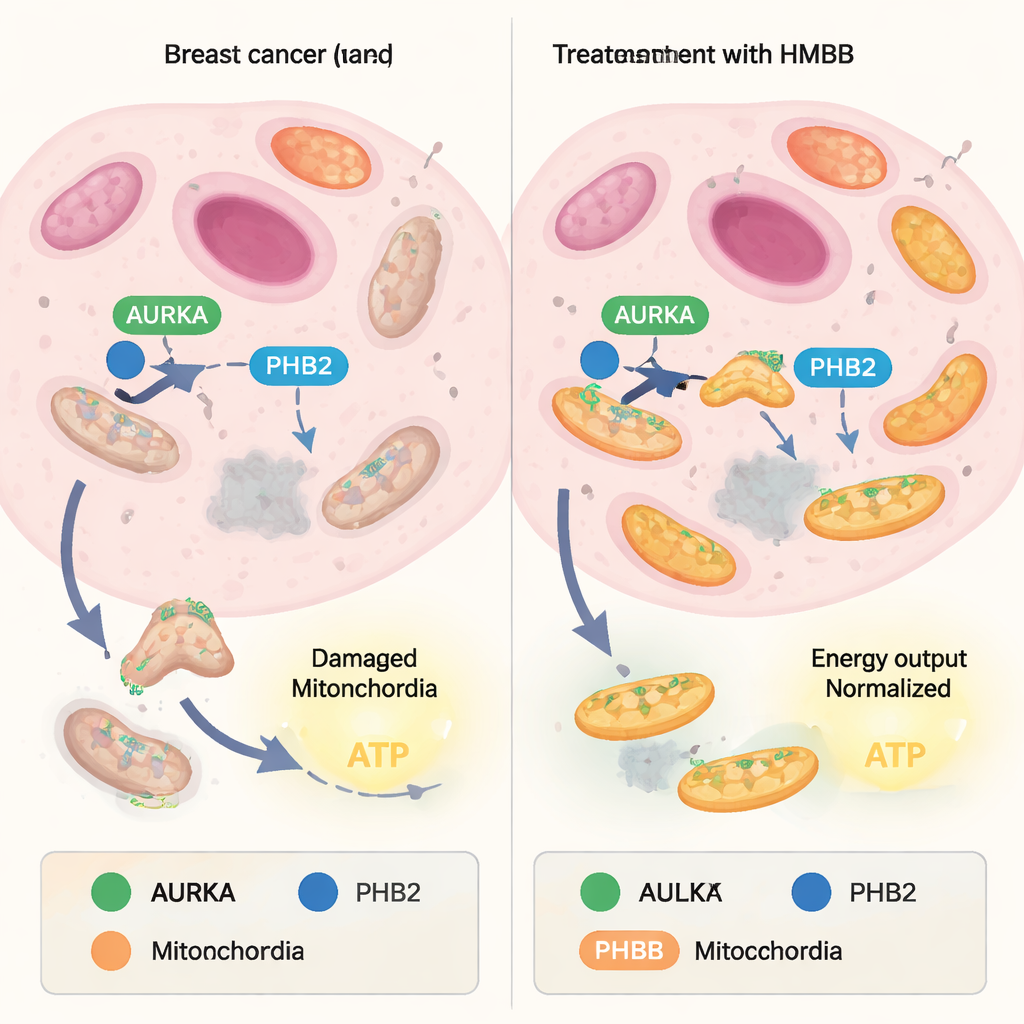
Baharatlı kapaisinden tasarlanmış moleküler araçlara
Daha önceki çalışmalar, doğal bir bileşik olan xanthohumol’ün PHB2’ye bağlanıp AURKA–PHB2–LC3 kompleksini bozabildiğini, mitofajiyi engelleyip mitokondriyal ATP üretimini azalttığını göstermişti. Ancak xanthohumol’ün kimyasal yapısı ilaç geliştirme için ideal değil. Bu çalışmada yazarlar başka bir doğal PHB ligandı olan kapaisine yöneldiler ve bunu daha pratik araçlara dönüştürüp dönüştüremeyeceklerini sordular. Önce kapaisinin canlı meme kanseri hücrelerinde AURKA ile PHB2 arasındaki etkileşimi az da olsa zayıflattığını, iki işaretli proteinin birbirine ne kadar yakın oturduğunu ölçen bir görüntüleme tekniği (FRET/FLIM) kullanarak doğruladılar. Ardından özgün yapının “kuyruk” ve aromatik “kafa” kısımlarını değiştirerek 16 kapaisin esinli molekül sentezlediler ve her bir versiyonun mitokondriler içindeki AURKA–PHB2 ortaklığını nasıl etkilediğini sistematik olarak test ettiler.
Proteinleri bir arada kilitleyen moleküler ‘yapıştırıcı’ keşfi
Modifiye edilmiş moleküller çarpıcı şekilde farklı etkiler gösterdi. Kapaisin’in kendisi veya bileşik 5 gibi bazıları AURKA ile PHB2’nin daha kolay ayrılmasına neden oldu. Diğerleri neredeyse hiçbir şey yapmadı. Ancak bir alt küme — özellikle bileşik 13 olarak adlandırılan ve daha sonra HMBB denen bir molekül — ters etki göstererek AURKA ile PHB2 arasındaki bağı önemli ölçüde sıkılaştırdı. Bilgisayar tabanlı yerleştirme (docking) simülasyonları bu davranışı açıklamaya yardımcı oldu. Kapaisin ve bileşik 5, PHB2 ile fiziksel çarpışmalara yol açan biçimlerde AURKA’nın aktif bölgesine yerleşmeye eğilimliydi ve böylece iki proteinin ayrılmasını teşvik ediyordu. Buna karşılık bileşikler 12 ve 13, AURKA aktif bölgesine yerleşip aynı anda PHB2 üzerinde bilinen bir inhibitör cebiyle temas kurdu; çarpışmaya neden olmak yerine şekilleri, AURKA ile PHB2 arasında köprü oluşturarak kompleksi stabilize etmelerine olanak sağladı — yani bir “moleküler yapıştırıcı” gibi davrandı.
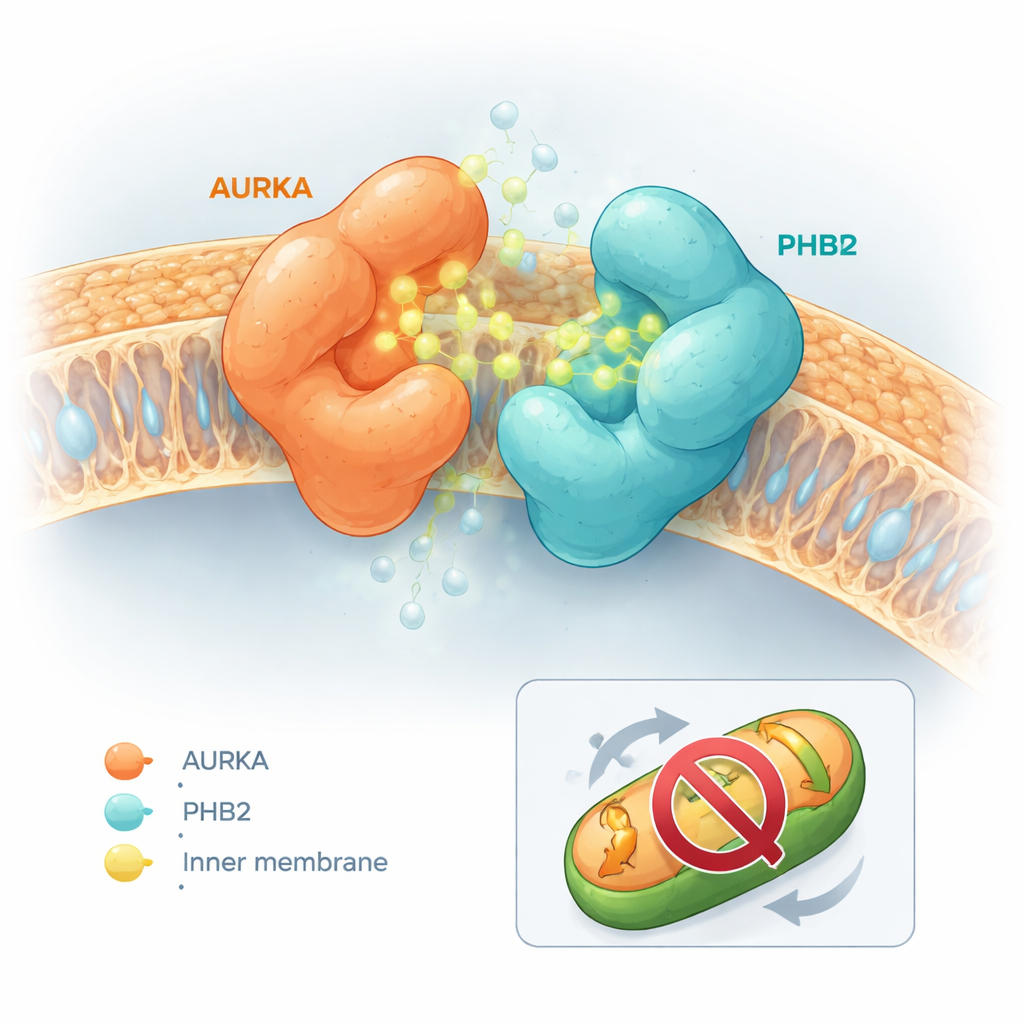
Hücresel kontrol merkezini kapatmadan mitokondri temizliğini engellemek
Temel soru, bu moleküler yapıştırıcı davranışının AURKA’yı hücrenin her yerinde devre dışı bırakarak geniş yan etkilere yol açıp açmadığı ya da daha seçici şekilde hareket edip etmediğiydi. Hücrenin bölünme mekanizmasını organize eden merkezcikler (centrosomlar) üzerindeki AURKA aktivasyonunu bildiren ayrı bir floresan biyosensör kullanıldığında, ekip HMBB’nin bu bölgelerde AURKA aktivitesini azaltmadığını gözlemledi. Yine de mitokondriyel testlerde HMBB, meme kanseri hücrelerinde AURKA aşırı ekpresyonunun genellikle neden olduğu mitokondri kütlesi kaybını tersine çevirdi. Doğal olarak yüksek AURKA seviyelerine sahip hücrelerde HMBB mitokondri içeriğini artırdı; bu, AURKA kaynaklı mitofajinin engellendiğini gösterir. Düşük AURKA düzeyine sahip hücrelerde HMBB’nin etkisi zayıftı; bu da bileşiğin AURKA–PHB2 yoluna bağımlılığını vurguluyor.
Gelecekteki kanser tedavileri için olası anlamı
Bir arada ele alındığında bulgular, özenle tasarlanmış kapaisin türevlerinin mitokondrilerde AURKA ile PHB2 arasındaki etkileşimi ince ayar yapabileceğini gösteriyor. Moleküler yapıştırıcı olarak davranan HMBB ve ilgili bileşikler, AURKA ile PHB2’yi mitofaji programının ilerlemesine izin vermeyen bir konfigürasyonda birbirine kilitliyor; aynı zamanda AURKA’nın hücrenin diğer yerlerindeki temel rollerini kapatmıyor. Popüler okuyucu için ana fikir, yazarların kanser hücrelerinin enerji santrallerini iyi durumda tutma biçimlerini seçici olarak bozabilen prototip moleküller yarattıkları — bu da normal hücre işlevlerine zarar vermeden kanser hücrelerinin enerji kaynaklarını zayıflatabilir. Bu bileşikler hâlâ erken, laboratuvar aşamasında olmasına rağmen, mitochondrideki belirli protein ortaklıklarını hedef almak ve böylece birçok tümörün dayandığı metabolik avantajları aşındırmak için küçük, ilaç benzeri moleküller kullanma konusunda ümit verici bir strateji örneği sunuyor.
Atıf: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Anahtar kelimeler: mitokondri, mitofaji, Aurora kinaz A, kapaisin türevleri, kanser metabolizması