Clear Sky Science · tr
MHC1-TIP, tek tüplü çok modlu immunopeptidom profillemeyi mümkün kılar ve antijen sunumunda tümör içi heterojenliği ortaya çıkarır
Kanserin Kimlik Kartlarına Bir Bakış
Her hücrenin yüzeyinde, bağışıklık sisteminin o hücrenin sağlıklı mı yoksa tehlikeli mi olduğuna karar vermesine yardımcı olan küçük moleküler “kimlik kartları” bulunur. Kanserde bu kimlik kartları—antijen adı verilen kısa protein parçacıkları—tümör hücresinin anormal yönlerini ortaya çıkarabilir ve onu bağışıklık hücreleri tarafından yok edilmek üzere işaretleyebilir. Bu çalışma, MHC1-TIP adını taşıyan yeni bir laboratuvar yöntemi tanıtıyor; bu yöntem, hasta dokusunun çok küçük miktarlarından bu kimlik kartlarını okumayı çok daha kolay ve daha ucuz hâle getirerek daha hassas kanser immünoterapilerine kapı açıyor.
Hücre Yüzeyi Sinyallerinin Neden Önemli Olduğu
Bağışıklık sistemimiz, MHC sınıf I adı verilen özel moleküller üzerinde gösterilen antijenleri kontrol ederek hücreleri sürekli denetler. Tümör hücreleri sıklıkla, T hücreleri tarafından tanınabilecek ve kişiselleştirilmiş aşılar gibi tedavilerle hedef alınabilecek sıra dışı antijenler sergiler. Ancak gerçek hasta örneklerinde hangi antijenlerin bulunduğunu ölçmek teknik olarak zordur. Geleneksel yöntemler çok sayıda hücre, çok sayıda işlem adımı ve pahalı antikorlar gerektirir; bu da onları küçük biyopsiler veya kıt klinik örnekler için uygun olmayan bir hâle getirir. Aynı zamanda tümörler homojen değildir: farklı bölgeler farklı proteinler ifade edebilir; bu da antijen sunumunun tek bir tümör içinde yerden yere değişebileceği olasılığını gündeme getirir.
Kanser Antijenlerine Tek Tüplü Kestirme Yol
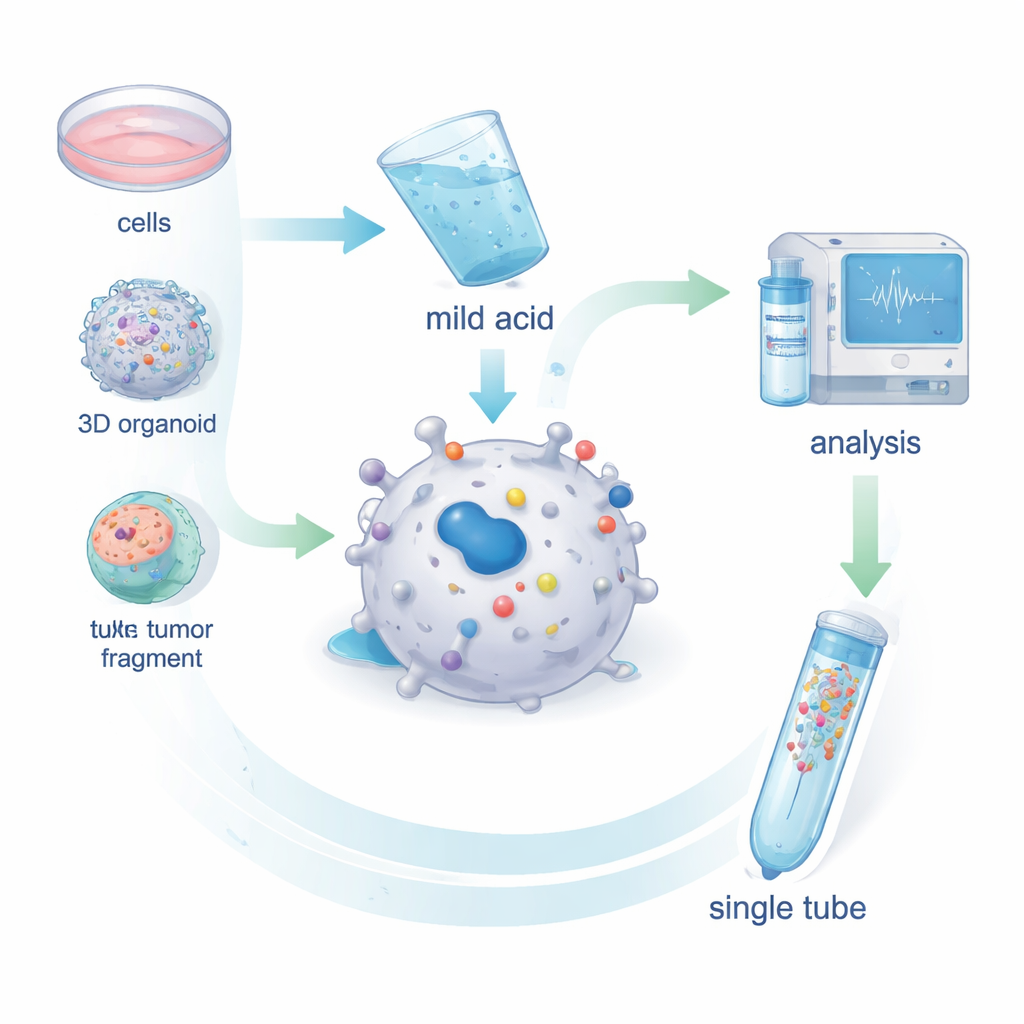
Araştırmacılar, canlı hücrelerden antijenleri toplamayı kolaylaştıran düzenli bir yol olarak MHC1-TIP (MHC-I 1-Tube Immunopeptidomics) geliştirdiler. Hücreleri parçalamak ve antikorlarla MHC moleküllerini yakalamak yerine, sağlam hücreleri—veya küçük tümör parçacıklarını—kısa süreli hafif asidik bir çözelti ile yıkıyorlar. Bu nazik işlem, MHC oluğunda oturan antijenlerin hücreleri öldürmeden kopup düşmesine neden oluyor. Serbest kalan peptitler sonra daha büyük artık maddeleri uzaklaştıran küçük bir filtreden geçiyor ve tek bir tüp içindeki küçük bir kolonda tutuluyor. Oradan doğrudan peptit dizilerini tanımlayan kütle spektrometresine gönderiliyorlar. Melanom hücrelerinde yapılan testler, bu hafif asit yıkamanın yüzeydeki MHC–antijen komplekslerinin neredeyse tamamını uzaklaştırdığını ve elde edilen peptitlerin uzunluk ve dizi desenleri açısından gerçek MHC-bağlı antijenlere çok benzediğini gösterdi.
Daha Az Örnekten Daha Fazla Veri
MHC1-TIP, çok az hücre ile çalışacak ve hâlâ birçok tanımlanabilir antijen sağlayacak şekilde tasarlandı. Yeni iş akışını veri-bağımsız edinim (data-independent acquisition) adı verilen modern bir kütle spektrometresi modu ile eşleştirerek, ekip 100.000 hücre kadar az sayıda hücreden yüzlerce antijen ve birkaç milyon hücreden binlerce antijen tespit etti—alanın altın standart antikor yöntemine benzer derinlikte, ancak daha az materyal ve daha düşük maliyetle. Yöntem ayrıca laboratuvarda büyütülen 3B mini-tümörler olan hasta türevi organoitlerde ve bir kilometre küpünden daha küçük eks vivo tümör parçacıklarında da çalıştı. Önemli olarak, asit yıkama hücreleri büyük ölçüde sağlam bıraktığı için geride kalan materyal aynı örnekten tam ölçekli protein profillemesi için kullanılabiliyor; bu da belirli bir proteinin ne kadarının bulunduğu ile ne kadarının gerçekten antijen olarak sunulduğu arasında doğrudan karşılaştırma yapılmasına izin veriyor.
Tek Bir Tümör İçindeki Gizli Farklılıklar
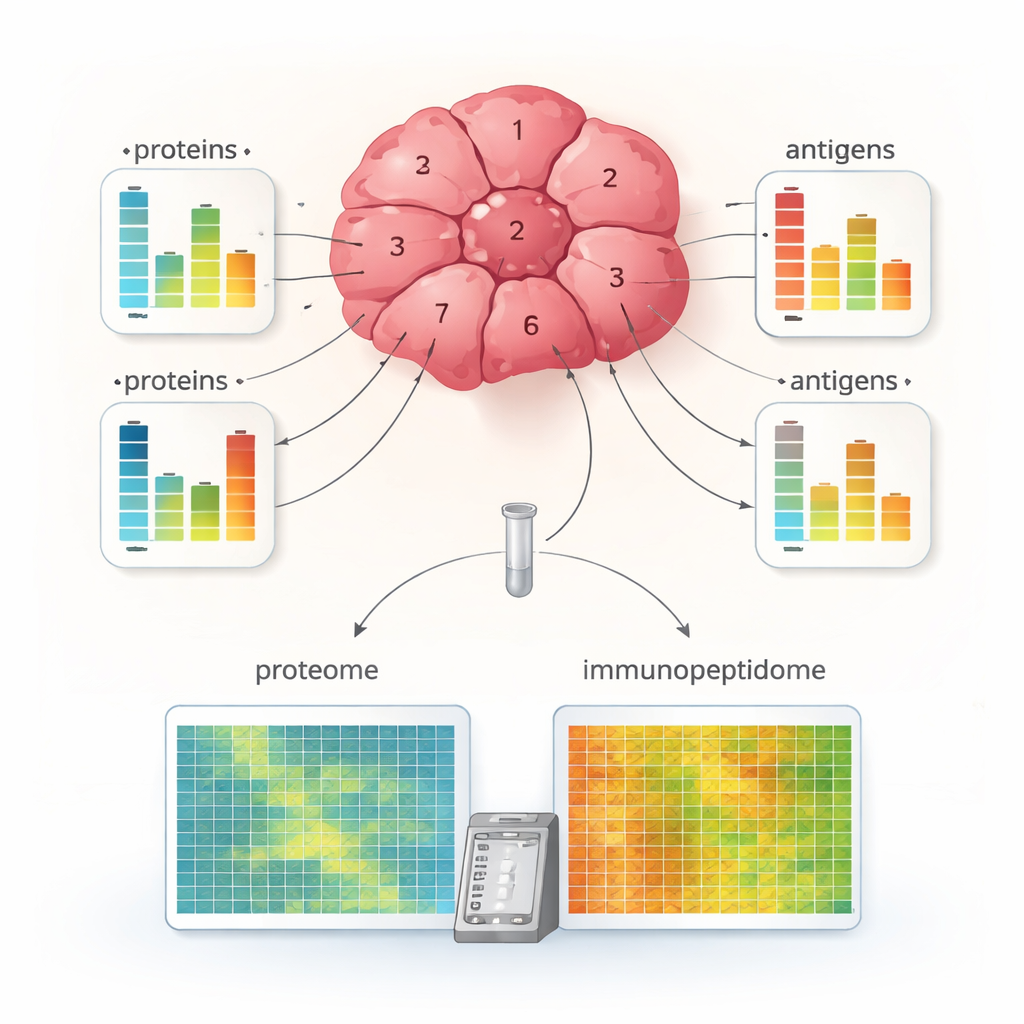
MHC1-TIP’in böbrek hücreli karsinom tümörünün farklı bölgelerinden alınan birden fazla küçük parçaya uygulanması çarpıcı iç çeşitliliği açığa çıkardı. Bazı parçalar zengin antijen sunumu gösterirken, diğerleri çok az antijen sergiledi; bununla birlikte genel protein içerikleri benzer olabiliyordu. Birçok protein için antijen düzeylerindeki değişiklikler, protein bolluğundaki değişikliklerle örtüşmedi; bu durum antijen işleme ve MHC moleküllerine yüklemenin ana protein miktarından bağımsız olarak düzenlendiğini öne sürüyor. Ekip ayrıca antijen verilerini bağışıklık hücreleri ve MHC mekanizması belirteçleriyle birleştirerek, yüksek antijen sunumu ve aktif T hücre işaretleri gösteren “bağışıklık-sıcak” tümör bölgelerini ve daha az antijen ve daha zayıf görünür bağışıklık saldırısı gösteren “bağışıklık-soğuk” bölgeleri tanımladı. Bu düzeyde ayrıntı, böylesine küçük doku parçalarından nadiren elde edilebiliyordu.
Geleceğin Kanser Bakımı İçin Anlamı
Uzman olmayan bir okuyucu için ana mesaj şudur: Bir tümörün hangi proteinleri ürettiğini ölçmek, bağışıklık sisteminin gerçekte neleri görebileceğini bilmek için yeterli değildir. Yeni MHC1-TIP yöntemi, çok küçük, klinik açıdan gerçekçi örneklerden gerçek antijen gösterimini okumak için pratik bir yol sunarken aynı zamanda daha geniş protein manzarasını da ölçüyor. Antijen sunumunun aynı tümörün farklı bölgeleri arasında büyük ölçüde değişebileceğinin ve her zaman protein seviyelerini takip etmediğinin keşfi, yalnızca gen veya protein ekspresyonuna dayanarak aşı veya T hücresi hedefleri seçilmesi konusunda uyarıda bulunuyor. Gelecekte MHC1-TIP benzeri yaklaşımlar, yüzeyde gerçekten gösterilen ve tümör boyunca daha tutarlı şekilde sunulan antijenlere odaklanarak daha etkili, kişiselleştirilmiş immünoterapilerin tasarlanmasına yardımcı olabilir.
Atıf: Bathini, M., Bocaniciu, D., Johnson, F.D. et al. MHC1-TIP enables single-tube multimodal immunopeptidome profiling and uncovers intratumoral heterogeneity in antigen presentation. Commun Biol 9, 296 (2026). https://doi.org/10.1038/s42003-026-09570-6
Anahtar kelimeler: antijen sunumu, immunopeptidomik, kanser immünoterapisi, tümör heterojenitesi, kütle spektrometresi