Clear Sky Science · tr
Radyo-nüklid uyarımlı dinamik tedavi, tamamlayıcı immünojenik nekroptoz ve apoptozis kanser hücresi ölüm yollarını indükler
Kansere Kendi Hileleriyle Karşılık Vermek
Kanser, özellikle vücuda yayılmış agresif meme tümörlerinde en iyi tedavilerimizden kaçmasıyla kötü şöhretlidir. Bu çalışma, radyo-nüklid uyarımlı dinamik tedavi (RaST) adı verilen yenilikçi bir yaklaşımı inceliyor; bu yöntem, tıbbi görüntüleme izotopları ile ışığa duyarlı nanopartikülleri kullanarak kanser hücrelerini öldürür ve aynı zamanda bağışıklık sistemini de uyandırır. Okuyucular için bu çalışma önemlidir çünkü mevcut görüntüleme araçlarının ve akıllı malzemelerin geçici tümör küçülmesinden ziyade daha kalıcı, bağışıklık kaynaklı kanser kontrolü oluşturmak üzere nasıl yeniden amaçlanabileceğini öne sürüyor.
Tümörleri İçten Aydınlatmanın Yeni Bir Yolu
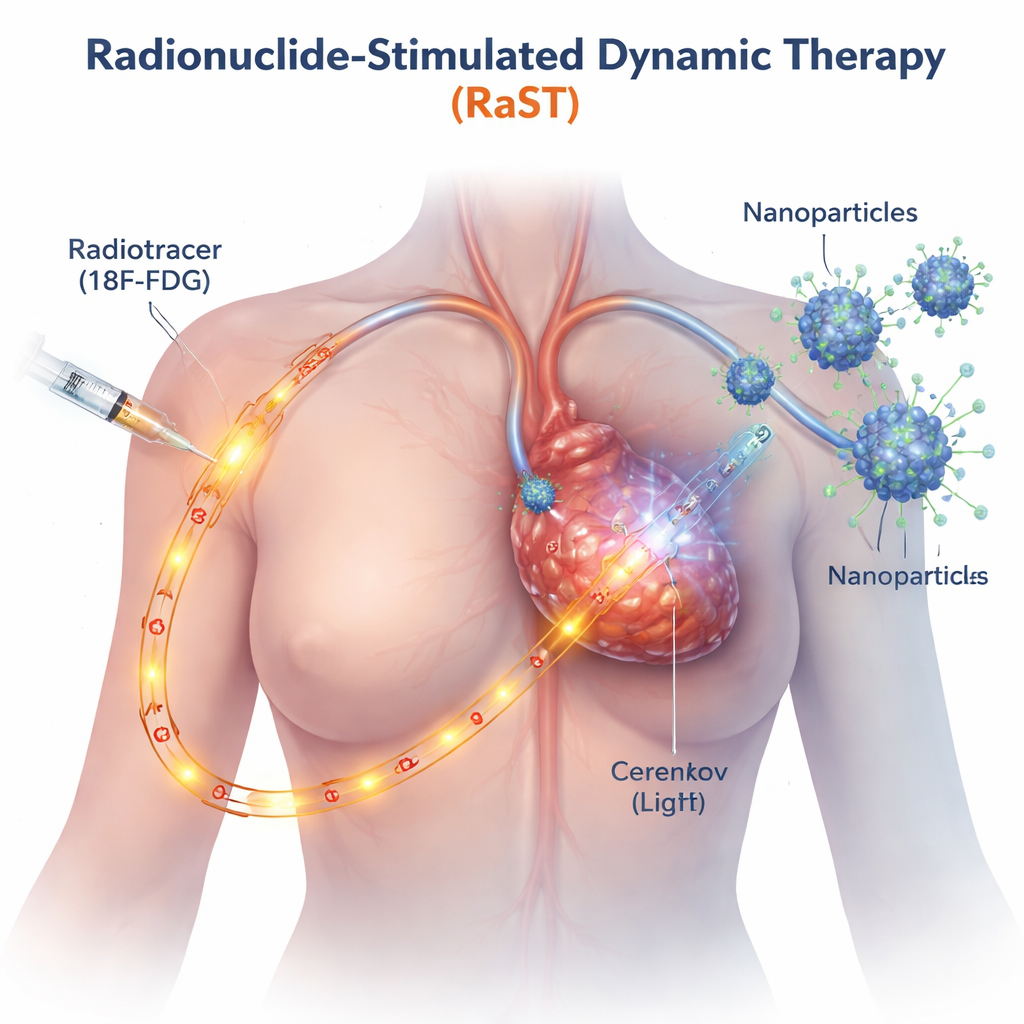
Geleneksel ışık bazlı kanser tedavileri, yalnızca dışarıdan gelen ışının ulaşabildiği yerde, örneğin deri veya yüzeysel tümörlerde etkilidir. RaST, PET taramalarında kullanılan izotopa benzer radyoaktif bir şekeri kullanarak bu sınırlamayı aşar; bu izotop hızla büyüyen kanser hücrelerinde doğal olarak birikir. İzotop tümör boyunca hareket ederken, Cerenkov radyasyonu olarak bilinen zayıf mavi bir parlama yayar. Araştırmacılar, tümöre yönelen bir kanser hedefleme proteini ile kaplanmış küçük titanyum dioksit nanopartikülleri tasarladılar, böylece bunlar da tümöre yönelir. İzotop ve nanopartiküller bir araya geldiğinde içten gelen ışık parçacıkları aktive eder; bu da parçacıkları reaktif oksijen türleri üreten mimariye sokar—kanser hücrelerine içeriden zarar veren yüksek reaktif moleküller.
Hücre Ölümüne İki Farklı Yolun Tetiklenmesi
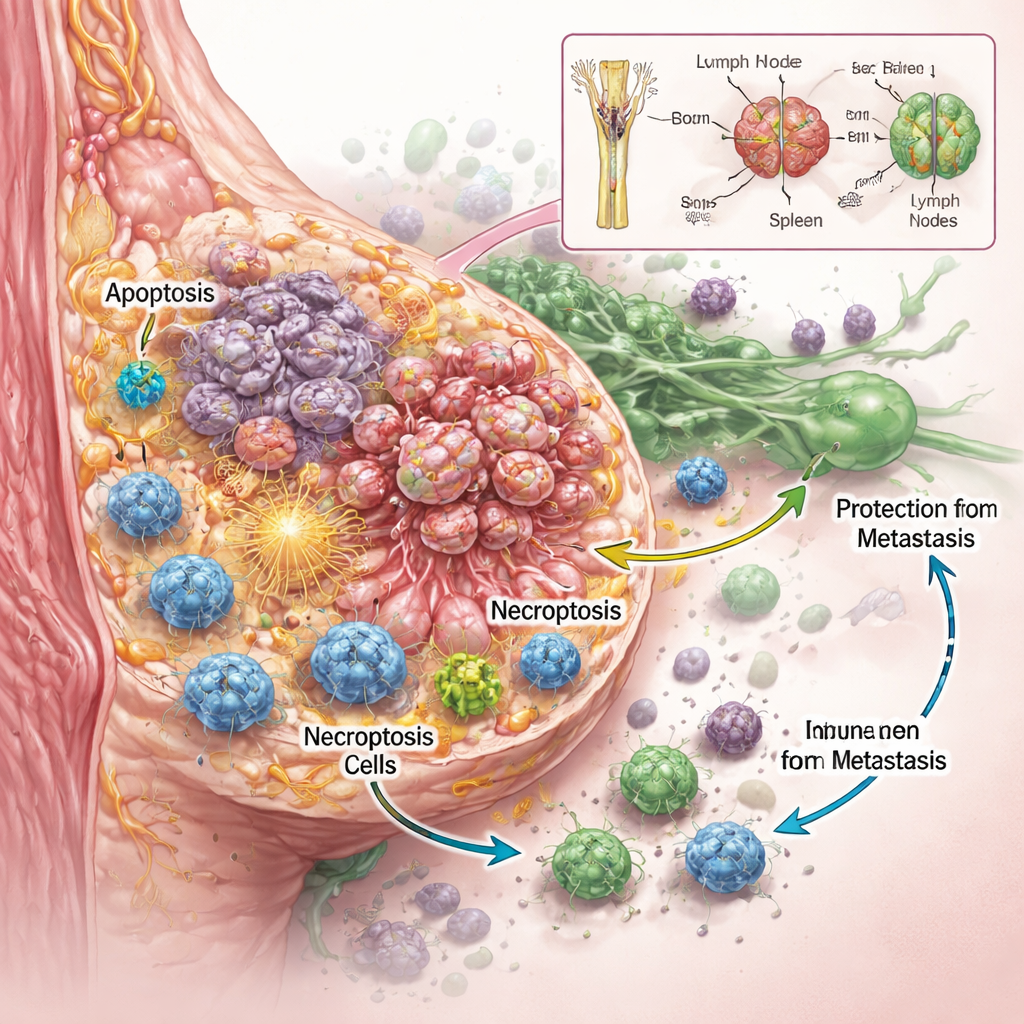
Ekip, RaST’in yalnızca kanser hücrelerini öldürüp öldürmediğini değil, nasıl öldürdüğünü de öğrenmek istedi. Laboratuvarda birkaç agresif meme kanseri hücre hattı kullanarak, dikkatle ayarlanmış radyoaktif izotop ve nanoparçacık dozlarının, tek başına her bir bileşenden daha etkili biçimde tümör hücrelerine zarar verdiğini buldular; bu, standart kemoterapiye dirençli olduğu bilinen tiplerde bile geçerliydi. Ayrıntılı görüntüleme ve protein ölçümleri, RaST’in aynı anda iki düzenlenmiş hücre ölümü programını aktive ettiğini ortaya koydu. Bunlardan biri apoptozdu; genellikle hücrenin düzenli bir şekilde kendini sökmesi olarak tanımlanan “intihar” yoluydu. Diğeri ise nekroptozdu; hücrelerin şiştiği, yırtıldığı ve çevrelerine moleküler distress sinyalleri saçtığı daha patlayıcı bir ölüm biçimiydi. Bu sinyaller—hasara bağlı moleküller ve inflamatuar sitokinler olarak bilinen—bağışıklık hücrelerini çeken ve aktive eden işaret fişekleri işlevi görebilir.
Uzun Süreli Kontrol İçin Bağışıklık Sistemini Seferber Etmek
Bu iltihaplı tümör öldürme tarzının yaşayan organizmalarda önem taşıyıp taşımadığını görmek için araştırmacılar RaST’i meme kanseri fare modellerinde test ettiler. Temel bağışıklık savunmalarından yoksun farelerde, RaST bol miktarda lokal hücre ölümü üretmesine rağmen tümör büyümesini veya akciğere yayılımı durdurmada çok az etkili oldu. Ancak bağışıklık sistemi sağlam farelerde aynı tedavi kısmi ve tam tümör yanıtları oluşturdu ve akciğere metastazı engelledi. RaST’e maruz kalan tümörler, özellikle makrofajlar ve dendritik hücreler gibi ölü materyali yutma ve tümör parçalarını T hücrelerine sunma konusunda ustalaşmış miyeloid hücrelerle doldu. Kan testleri, zaman içinde bağışıklığı uyaran ve düzenleyen dalgalar halinde sinyaller gösterdi; bu da RaST’in önce kanseri hedef alan bir saldırıyı ateşlediğini, daha sonra tümörler küçüldükçe veya stabil hale geldikçe daha dengeli bir duruma kaydığını düşündürüyor.
Gizli Artıkları Avlamak ve Nüksü Önlemek
RaST ile tümörler tamamen iyileşmiş gibi görünen farelerde bile, çok hassas bir görüntüleme boyası daha sonra lenf düğümlerinin içinde saklanmış küçük kanser hücresi odacıklarını ortaya çıkardı. Dikkate değer olarak, bu hayvanlarda aylar boyunca yeni tümörler veya uzak metastazlar gelişmedi. Kimyasal analizler, başlangıçta kemiklerde ve karaciğerde bol bulunan titanyum dioksit nanopartiküllerinin zamanla dalak ve lenf düğümlerine yeniden dağıldığını gösterdi—tam da bağışıklık hücrelerinin devriye gezdiği merkezlere. Bu yavaş göç muhtemelen bağışıklık hücreleri için reaktif oksijenin yerel bir kaynağını koruyarak, onların bu gizli kanser artıklarını yeniden büyümeden veya yayılmadan önce tanımasına ve kontrol etmesine yardımcı oluyor.
Geleceğin Kanser Bakımı İçin Anlamı
Basitçe söylemek gerekirse, bu çalışma RaST’in sadece tümör hücrelerini zehirlemenin başka bir yolu olmadığını gösteriyor. Radyoaktif izotoplar, ışığa duyarlı nanopartiküller ve vücudun kendi savunmalarını birleştirerek, kanser hücrelerini bağışıklık sistemini güçlü biçimde uyaran iki programlı hücre ölümü biçimine zorluyor. Bağışıklık yetkin hayvanlarda bu, agresif meme tümörlerinin kalıcı kontrolüne yol açıyor ve birkaç kanser hücresi lenf düğümlerinde kalsa bile metastazı engelliyor. Bu yaklaşımın insanlarda yaygın şekilde test edilmeden önce yapılması gereken çok iş olsa da çalışma, sadece tümörleri küçültmeyi hedefleyen değil; kanser, hücre ölümü ve bağışıklık arasındaki ilişkiyi yeniden şekillendirerek vücudun hastalığı uzun vadede kontrol altında tutmasına yardımcı olacak gelecekteki tedavilere işaret ediyor.
Atıf: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Anahtar kelimeler: meme kanseri, nanopartiküller, immünoterapi, radyo-nüklid tedavisi, nekroptoz