Clear Sky Science · tr
SDHB mutasyonlarının yönlendirdiği metastatik feokromositom ve paragangliomalarda epigenetik ve metabolik yeniden düzenleme
Neden bu nadir tümörler önemli
Feokromositomlar ve paragangliomalar, genellikle böbreküstü bezlerinin yakınında bulunan hormon üreten sinir hücrelerinden kaynaklanan nadir tümörlerdir. Çoğu yavaş büyür ve cerrahi ile iyileştirilebilir, ancak yaklaşık her beş olgudan biri sonunda diğer organlara yayılır ve hayatı tehdit edebilir. Bu çalışma basit ama hayati bir soruyu soruyor: bu tümörlerden bazılarını tehlikeli hale getiren nedir? Kanserlerin genleri nasıl açıp kapattığına ve kendilerine nasıl yakıt sağladıklarına derinlemesine bakarak, araştırmacılar bir gün yeni tedavilerle hedeflenebilecek gizli bir zayıflık ortaya koyuyor.
Sessiz büyümeden ölümcül yayılmaya
Araştırma ekibi, SDHB adlı genin değişikliklerini taşıyan tümörlere odaklandı. SDHB, hücrenin enerji santralleri olan mitokondrilerin Krebs döngüsünün bir bölümünü yürütmesine yardımcı olur. SDHB hasarlandığında sukkinat adı verilen bir kimyasal birikir ve hücreler gerçekte oksijen yeterli olsa bile düşük oksijen altındaymış gibi davranmaya başlar. Araştırmacılar, tümörleri lokal kalanlarla yayılmış olanları karşılaştırmak için 34 hastadan alınan dokuları incelediler. Genleri açıp kapatan kimyasal etiketleri gösteren yüksek çözünürlüklü bir DNA metilasyon haritası kullanarak, metastatik tümörlerin, özellikle SDHB mutasyonu varsa, benign olanlara göre daha güçlü bir gen susturma desenine sahip olduğunu buldular.
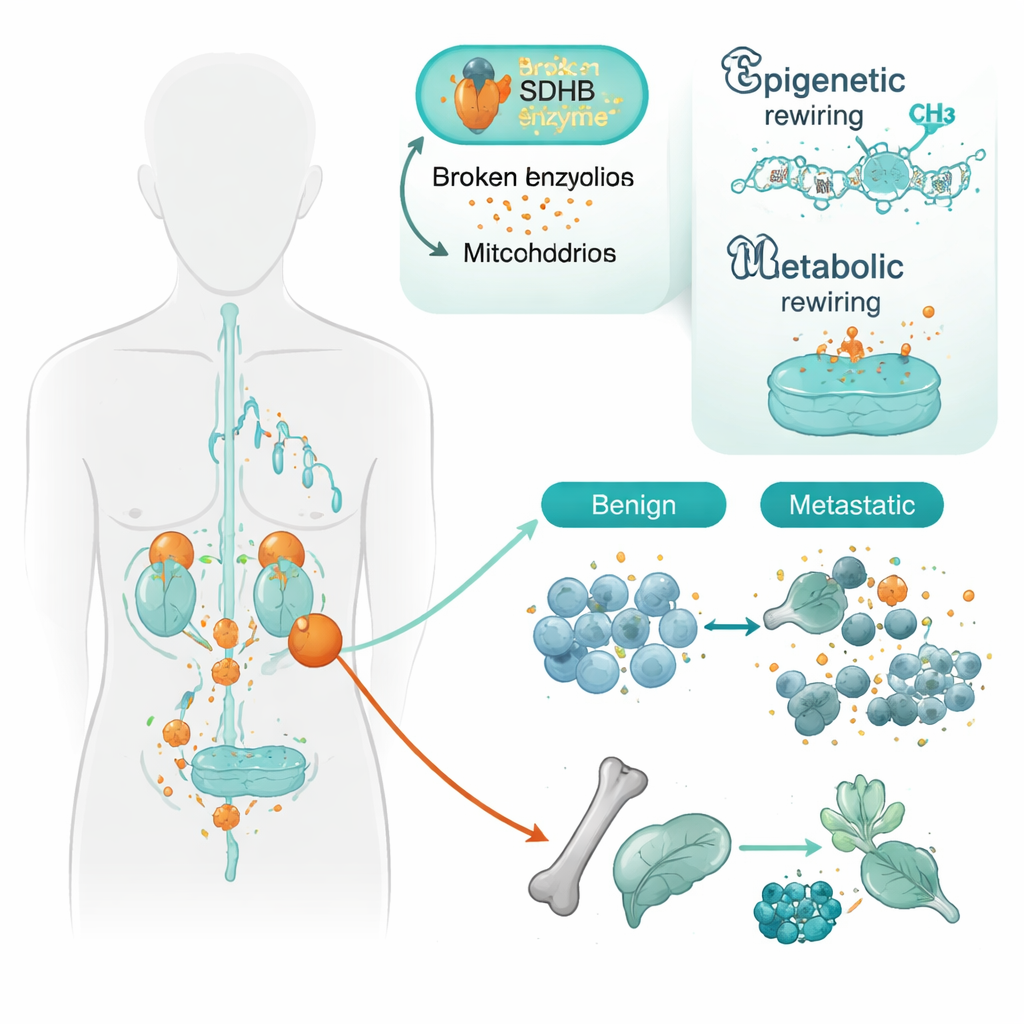
Hücre kimliğinin yeniden programlanması
Agresif tümörlerde susturulan birçok gen, sinir benzeri hücrelerin olgunlaşmasına ve uzmanlaşmış kimliklerini korumasına yardımcı olan genlerdi. Bunlar arasında hücrelerin birbirine nasıl bağlandığını, DNA’yı nasıl düzenlediklerini ve hangi hücre tipine dönüşeceklerine karar veren gen aileleri yer alıyor. Öne çıkan örneklerden biri hücre-adezivite geni PCDHGC3 oldu. SDHB mutantı olup yayılmayan tümörlerde bile bu genin kontrol bölgesi zaten kısmen kapalıydı; metastatik tümörlerde ise susturma daha da belirgindi. DNA’nın büyük bölgelerini organize eden SATB2 adlı başka bir gen ise yalnızca SDHB durumuna bakılmaksızın metastatik tümörlerde susturulmuştu. Bu desenler birlikte SDHB kaybının hücreleri daha az olgun, daha hareketli bir duruma “hazırladığı” ve ek epigenetik değişikliklerin sonra onların kopup yayılmasına yardımcı olduğu izlenimini veriyor.
Tümörlerin şeker yeme biçiminin yeniden kablolaması
Şaşırtıcı biçimde, tüm değişiklikler genleri kapatmakla ilgili değildi. Daha küçük bir gen seti daha az metilasyon geçirip daha aktif hale geldi ve bunlar özellikle şekerlerin hücre içine taşınmasıyla yakından ilişkiliydi. Bunların arasında fruktoz taşıyıcı geni SLC2A5 öne çıktı. GLUT5 olarak bilinen ürünü, meyvelerde ve birçok işlenmiş gıdada yaygın bulunan bir şeker olan fruktozu hücre içine taşır. Düşük oksijene maruz bırakılan tümöre benzer hücre modellerinde SLC2A5 kararlı şekilde açılırken, diğer şeker taşıyıcıları daha az tutarlı yanıt verdi. Yazarlar daha sonra PPGL tümörlerinden türetilmiş hasta kaynaklı hücre kültürleri oluşturup, glukoz kıt olduğunda fruktoz eklemenin bu hücrelerin bölünmeye devam etmesine yardımcı olduğunu, özellikle tümör ortamını taklit eden düşük oksijen koşullarında gösterdiler.
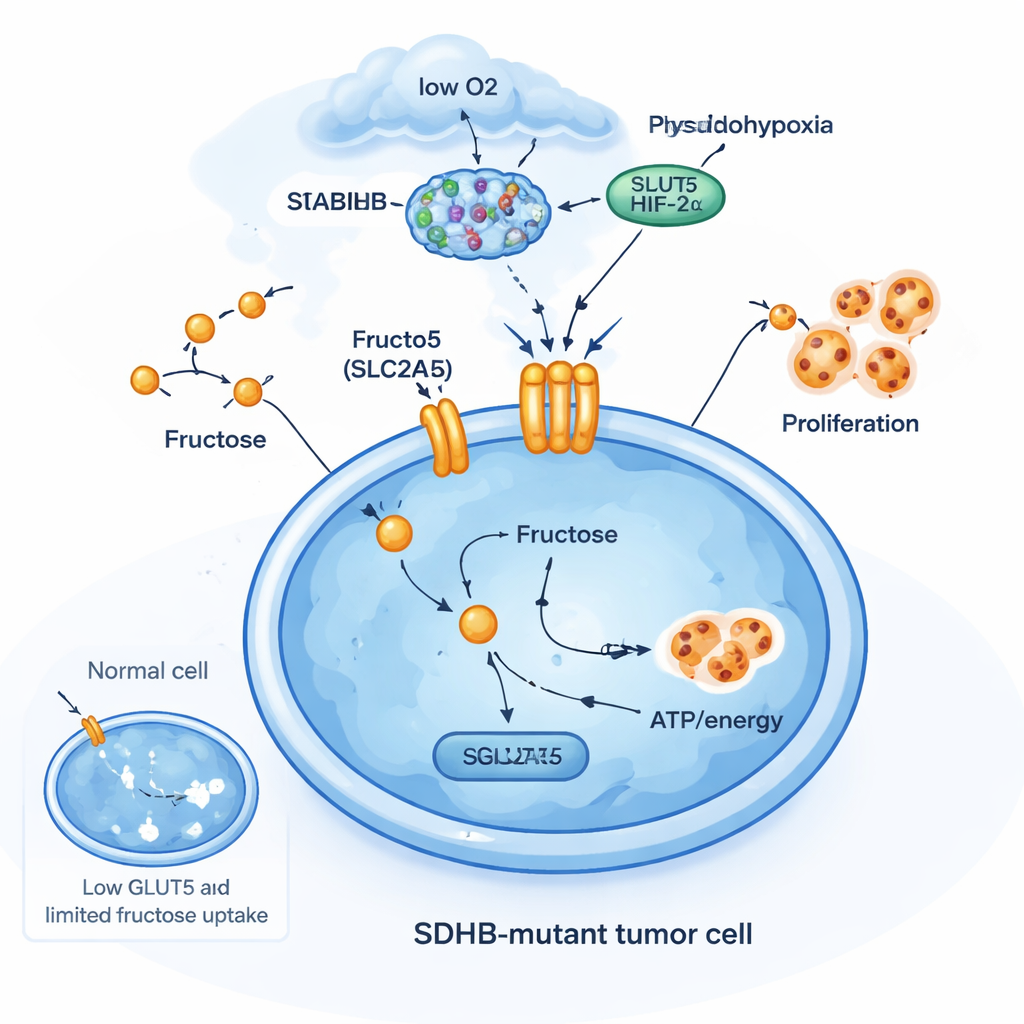
Fruktozla çalışan bir hayatta kalma hilesi
SDHB mutasyonlarının burada neden önemli olduğunu anlamak için ekip birkaç hücre tipinde SDHB’yi düzenleyerek kaldırdı. Böbreküstü bezi kaynaklı kromafin-benzeri hücrelerde ve oksijen algılama faktörü HIF2α’nın sürekli aktive olduğu bir böbrek kanseri hücre hattında SDHB kaybı SLC2A5 düzeylerini artırdı. Ancak bu nöroendokrin özellikleri veya HIF2α aktivitesini taşımayan daha yaygın kanser hücre hatlarında aynı SDHB kesilmesi SLC2A5’i açmadı. Bu, fruktoz taşıyıcısının genel bir stres tepkisinin parçası olmadığını; zaten “sahte‑hipoksik” bir durumda yaşayan belirli hücre tiplerinde çok özgül bir adaptasyon olduğunu gösteriyor. Bu hücrelerde SDHB kaybı, sukkinat birikimi ve HIF2α aktivitesi birlikte oksijen ve glukoz sınırlı olduğunda büyümeyi sağlamak için fruktoz alımına açılan yeni bir metabolik kapı oluşturuyor.
Hastalar için ne anlama geliyor
Özetle, çalışma SDHB mutantı metastatik PPGL’lerde çift yönlü bir kaymayı ortaya koyuyor. İlki, DNA kontrol sistemlerinin hücreleri daha az uzmanlaşmış, invazyona eğilimli ve daha plastik bir duruma itmek üzere yeniden düzenlenmesi. İkincisi, enerji sistemlerinin zorlu, düşük oksijenli ve düşük glukozlu nişlerde alternatif yakıt olarak fruktozu kullanacak şekilde yeniden düzenlenmesi. Fruktoz taşıyıcısı SLC2A5/GLUT5’i bu sürecin kilit oyuncusu olarak tanımlayarak çalışma, fruktoz alımını veya metabolizmasını engellemenin bu tümörleri seçici olarak aç bırakma potansiyeline sahip olabileceğine işaret ediyor. Bu tür terapiler henüz mevcut olmasa da, bu epigenetik ve metabolik haritanın çıkarılması, yüksek riskli SDHB mutantı PPGL’li hastalar için metabolizmaya odaklı daha hassas tedavilere doğru atılmış kritik bir adım niteliğindedir.
Atıf: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Anahtar kelimeler: feokromositom, paraganglioma, SDHB mutasyonu, epigenetik, fruktoz metabolizması