Clear Sky Science · tr
PAK4 hedeflenmesi, NLRP1/caspase-3/GSDME ekseni yoluyla pankreas kanserinde Gemcitabine kaynaklı piroptozisi teşvik eder
Kanser hücrelerini “ateşli” bir biçimde öldürmenin önemi
Pankreas kanseri en ölümcül kanserlerden biridir ve en iyi kemoterapi ilaçlarımız bile tümörler direnç kazandıkça sıklıkla etkisini yitirir. Bu çalışma şaşırtıcı bir dönemeç sunuyor: aynı ilaç olan gemcitabine, kilit bir moleküler “fren” olan PAK4 kapatıldığında kanser hücrelerini daha patlayıcı, iltihaplı bir yolla—piroptozis—öldürebiliyor. Bu freni anlamak ve hedeflemek, mevcut tedavileri birçok hasta için daha etkili kılabilir.
Tedaviye direnen inatçı bir kanser
Pankreatik duktal adenokarsinom genellikle geç evrede teşhis edilir ve tedaviye zayıf yanıt verir; bu yüzden gemcitabine sınırlamalarına rağmen temel bir ilaç olarak kalır. Gemcitabine tipik olarak hücreleri apoptoz yoluyla öldürür; bu düzenli, sessiz bir programlı hücre ölümüdür. Ancak bu çalışmada incelenen pankreas tümörlerinin yarısından fazlası, sessiz ölümü piroptozise çevirebilen GSDME adlı proteinin yüksek düzeylerini üretmişti—piroptozis hücre membranını zarar veren ve iltihaplı sinyaller salan hızlı, “patlayan” bir hücre ölümü biçimidir. Bu da temel bir soruyu gündeme getirdi: tümörler piroptozise girebiliyorsa, neden bu kadar çoku hâlâ gemcitabine’e dirençli?
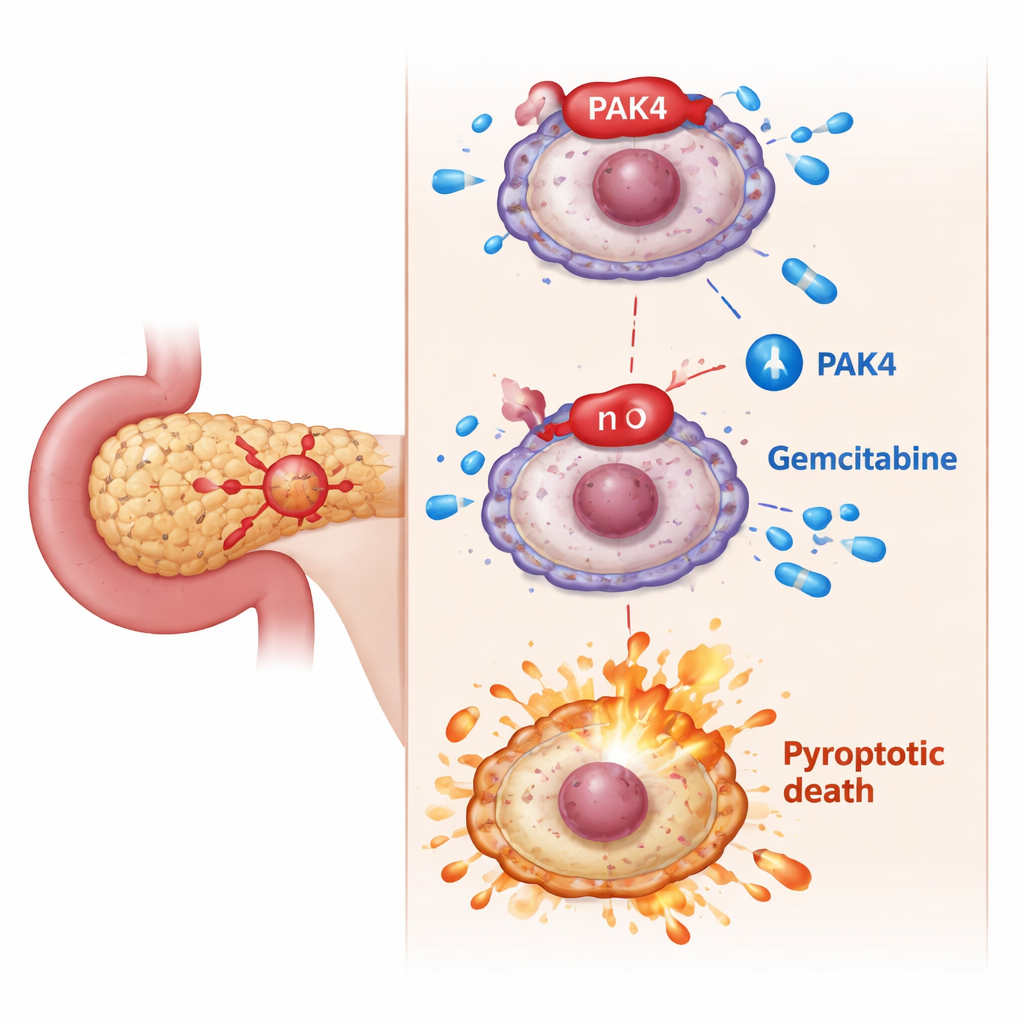
Gizli fren: PAK4 ateşli hücre ölümünü engelliyor
Araştırmacılar PAK4’e odaklandı; pankreas kanserinde aşırı aktif olduğu ve gemcitabine’ye zayıf yanıtla ilişkilendirildiği bilinen bir büyümeyi teşvik eden protein. Hücre deneylerinde, yüksek PAK4 düzeyine sahip kanser hücreleri gemcitabine ile öldürmesi daha zor olan hücrelerdi. Ekip PAK4’ü azalttığında, gemcitabine birdenbire çok daha öldürücü hale geldi: hücreler tipik piroptotik özellikler gösterdi—şişme, balonumsu kabarcıklar, yırtılmış zarlar ve hücre içi içeriklerin artan salınımı. Moleküler düzeyde bu değişim, GSDME’nin caspase-3 adlı başka bir protein tarafından aktif bir parçaya kesilmesine bağlıydı. Caspase-3’ü engellemek GSDME’nin piroptozisi tetiklemesini durdurdu ve PAK4’ün normalde bu ölüm yolunu baskıladığını doğruladı.
PAK4, hücrenin ölüm alarmını nasıl söndürüyor
Daha derine indiklerinde, PAK4’ün GSDME’ye doğrudan saldırmadığını buldular. Bunun yerine yukarı akıştaki bir “alarm sensörü” olan NLRP1’i sabote ediyordu. Hastalarda daha yüksek NLRP1 düzeyleri daha iyi sağkalımla ilişkilendirildi; bu da NLRP1’in tümörleri kontrol altında tutmaya yardımcı olduğunu düşündürüyor. Kanser hücrelerinde NLRP1 ortadan kaldırıldığında, gemcitabine kaynaklı hücre ölümü ve GSDME aktivasyonu keskin şekilde düştü; bu, NLRP1’in piroptozis mekanizmasına katkıda bulunduğunu gösteriyor. Tümör örneklerinde PAK4 ve NLRP1 düzeyleri ters orantılıydı: PAK4 yüksek olduğunda NLRP1 düşüktü. Çalışma, aktif PAK4’ün E3 ligazı Mdm2 üzerinden hareket ederek NLRP1’i hücrenin atık imha sistemi tarafından yok edilmek üzere işaretlediğini gösterdi. PAK4, NLRP1’i bu şekilde işaretleyerek caspase-9 ve caspase-3 aracılığıyla normale göre GSDME kaynaklı piroptozise yol açacak zincir reaksiyonun aktivasyonunu önlüyor.
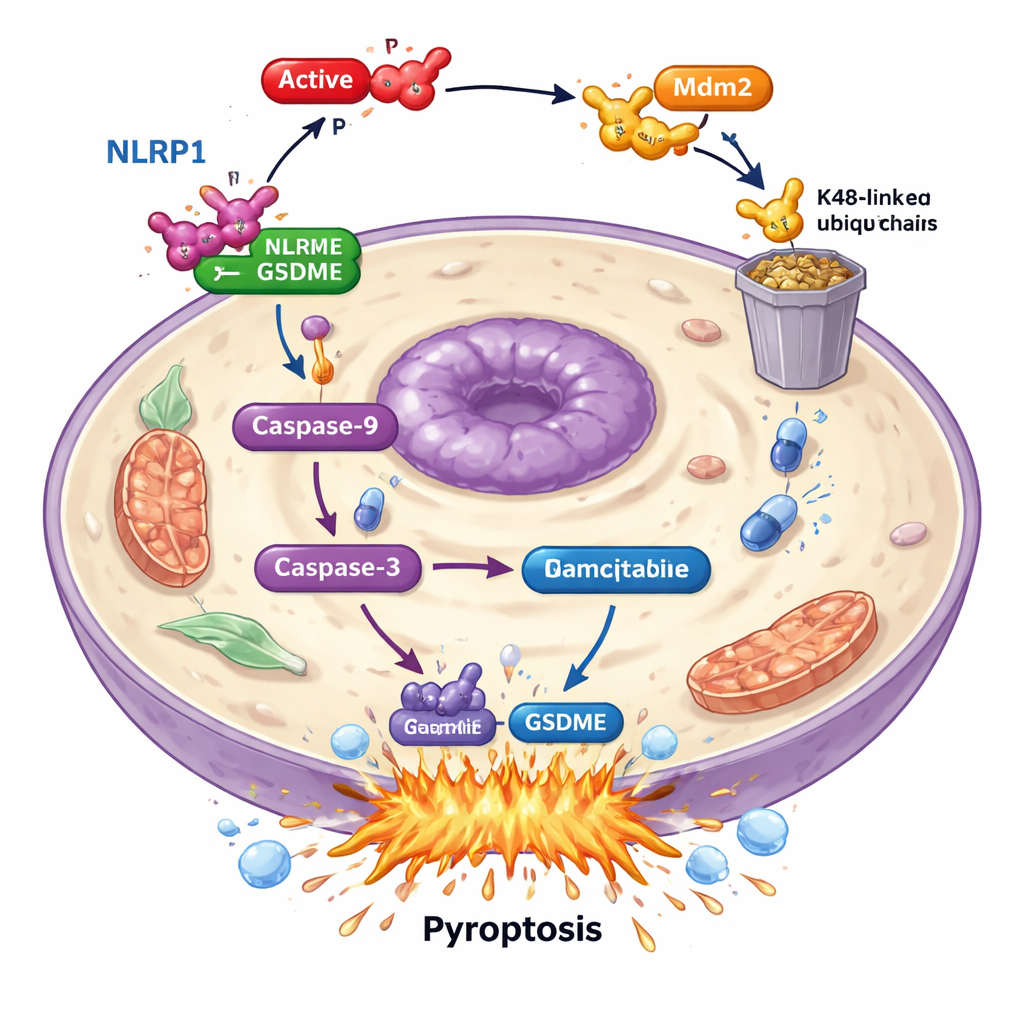
PAK4’ü kapatıp kemoterapiyi güçlendirmek
PAK4 piroptozis üzerinde bir fren görevi gördüğü için ekip, aktivitesini engellemenin gemcitabine’in öldürücü gücünü yeniden uyandırıp uyandıramayacağını test etti. PF-3758309 adında küçük moleküllü bir PAK4 inhibitörü kullandılar. Tek başına bu inhibitör pankreas kanseri hücrelerini piroptozise doğru itiyor, caspase-3 aktivasyonunu, GSDME parçalanmasını ve hücre zarı yıkımını artırıyordu. Gemcitabine ile birleştirildiğinde etki daha da güçlüydü: daha fazla hücre piroptozis yoluyla öldü ve ölüm yolunun moleküler belirteçleri yükseldi. İnsandan alınma pankreas tümörlerini taşıyan fare modellerinde, PAK4’ü azaltmak veya PAK4 inhibitörü ile tedavi etmek gemcitabine’in tümörleri daha etkili küçültmesini sağladı ve kanser içindeki piroptotik belirteçleri artırdı.
Hastalar ve gelecekteki tedaviler için anlamı
Basitçe söylemek gerekirse, bu çalışma kemoterapi altında pankreas kanseri hücrelerinin özellikle yıkıcı bir biçimde ölmesini engelleyen moleküler bir kilit—PAK4—ortaya koyuyor. PAK4 devre dışı bırakıldığında, hekimler gemcitabine ile tedavi edilen tümörleri piroptozise iterek ilacın daha etkili olmasını ve potansiyel olarak bağışıklık sistemi aracılığıyla kanserle mücadeleyi artırabilir. Hastadan türetilen modellerde ve klinik çalışmalarda daha fazla çalışma gerekse de, çalışma net bir yol haritası öneriyor: dirençli tümörleri yanıta çevirmek için mevcut ilaçları daha akıllıca kombinasyonlarda kullanarak PAK4–Mdm2–NLRP1–GSDME yolunu hedeflemek.
Atıf: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Anahtar kelimeler: pankreas kanseri, gemcitabine direnci, piroptozis, PAK4, hedefe yönelik tedavi