Clear Sky Science · tr
Alzheimer hastalarının temporal korteksinde farklı ifade edilen miRNA’lar ve bunların tau patolojisiyle ilişkisi
Alzheimer’da küçük beyin anahtarlarının neden önemli olduğu
Alzheimer hastalığı, hafızayı ve bağımsızlığı yavaşça elinden alır, ancak onu durduracak veya tersine çevirecek tedaviler hâlâ yok. Bu çalışma, hücrelerin hangi proteinleri üreteceğine yardımcı olan kısa RNA molekülleri olan mikroRNA’lar gibi beynin en küçük kontrol anahtarlarından bazılarını inceliyor. Alzheimer’lı kişilerin beyin dokusunu inceleyerek, bu mikroRNA’lardaki değişikliklerin hastalığın temel bir özelliği olan anormal tau proteininin hücre içinde birikimi ve yayılmasıyla bağlantılı olup olmadığını sordular.
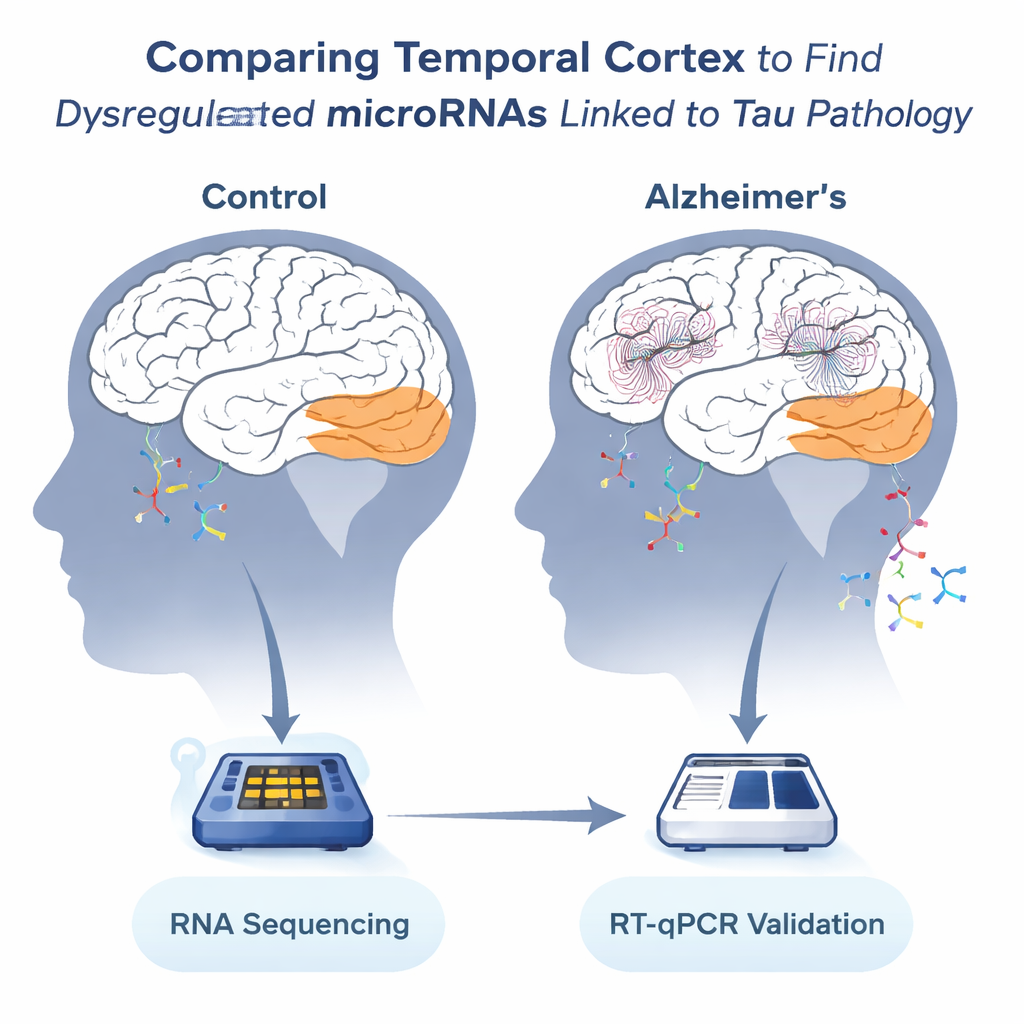
Hassas bir beyin bölgesindeki mesajlara bakmak
Ekip, dil ve hafıza için önemli ve Alzheimer’da yoğun biçimde etkilenen bir bölge olan temporal kortekse odaklandı. Ölüm sonrası, iki Avrupa beyin bankasından 36 bireyden—13’ü Alzheimer’siz ve 23’ü hastalıklı—numuneler toplandı. Bilim insanları bu dokudan RNA çıkardı ve yüzlerce farklı mikroRNA’yı saymak için yüksek verimli dizileme kullandı. Beyin dokusu ölüm sonrası bozulduğundan, RNA kalitesini dikkatle kontrol ettiler ve en ayrıntılı analiz için kabul edilebilir bütünlüğe sahip 19 örneği seçtiler; ardından ana bulgularını doğrulamak için tüm 36 örneği kullandılar.
Alzheimer’ın bir mikroRNA imzasını keşfetmek
Algılanan 449 mikroRNA arasında, Alzheimer temporal korteksinde tutarlı şekilde değişen 13 tanesi öne çıktı. Sekizi azalmış, beşi ise kontrol beyinlere kıyasla artmıştı. En güçlü sinyallerden birkaçını daha önce Alzheimer’da önemli olduğu düşünülen mikroRNA’lar oluşturuyordu: miR-129-5p, miR-132-3p ve miR-146b-5p’nin tümü daha düşükken, miR-151a-5p daha yüksekti. Bu moleküller beyinde bol bulunur ve sinir sağlığıyla ilişkili gen ağlarını düzenlemeye yardımcı oldukları bilinir. Yazarlar, ikinci, daha hedefe yönelik bir teknik (RT-qPCR) kullanarak aynı mikroRNA’ların aynı yönde değiştiğini doğruladılar; daha düşük kaliteli örnekler de dahil olduğunda bile bu, desenin gerçek olduğuna dair güveni güçlendirdi.
Küçük anahtarları kötüleşen tau yumaklarıyla ilişkilendirmek
Beyindeki Alzheimer şiddeti sıklıkla tau yumaklarının farklı bölgelerde ne kadar yayıldığını yansıtan Braak evresiyle derecelendirilir. Araştırmacılar, miR-129-5p, miR-132-3p ve miR-146b-5p düzeylerinin Braak evresi arttıkça düzenli olarak azaldığını, miR-151a-5p’nin ise artma eğiliminde olduğunu buldular. Aynı örneklerde yüksek derecede fosforile olmuş, yumak oluşturmaya yatkın bir tau formunu da doğrudan ölçtüler. Bu anormal tau daha fazla olan beyinler aynı desen gösteriyordu: daha az miR-129-5p, miR-132-3p ve miR-146b-5p ve daha fazla miR-151a-5p. Başka bir deyişle, mikroRNA değişiklikleri hem mikroskobik derecelendirme hem de tau patolojisinin biyokimyasal işaretleriyle paralel seyrediyordu; bu da onların rastgele yan bulgular değil, hastalık süreciyle yakından ilişkili olduğunu düşündürüyor.
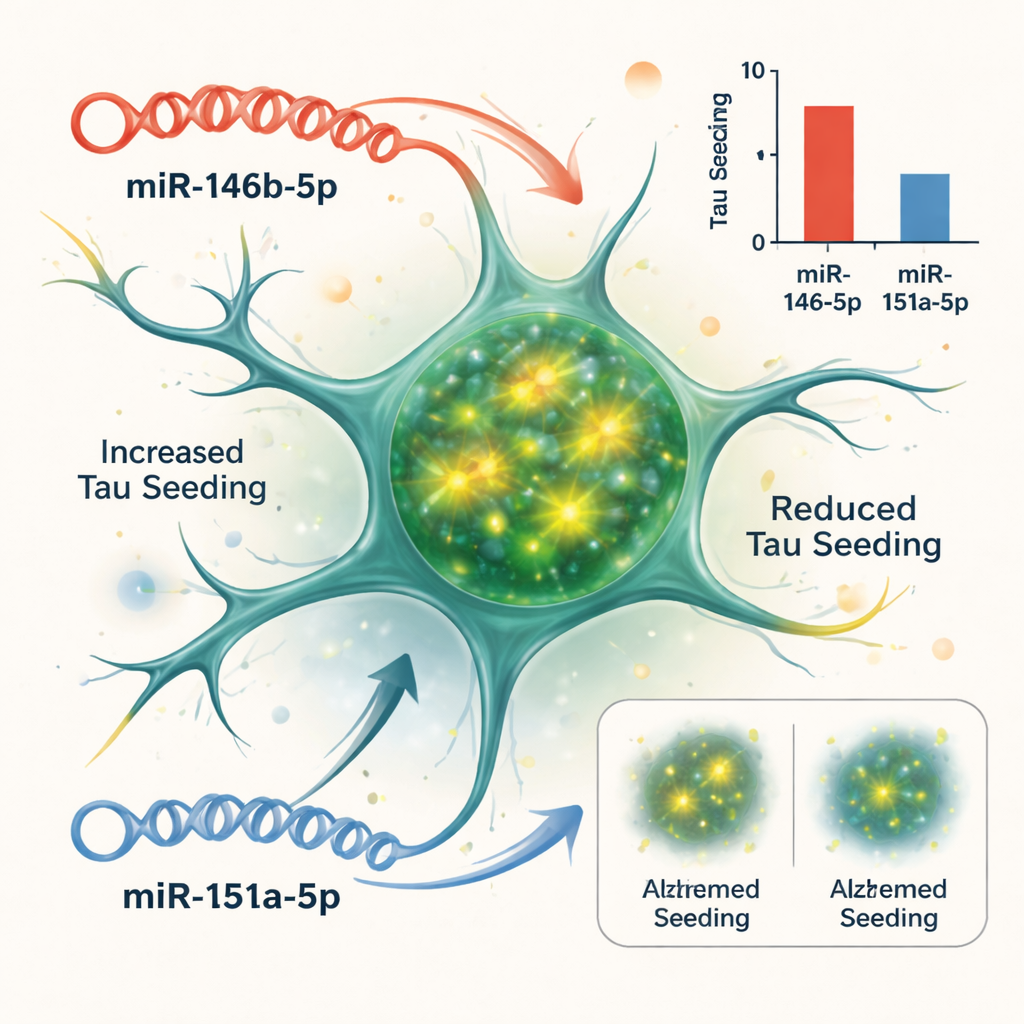
Hücre modelinde nedensellik testi
Korelasyonun mikroRNA’ların hastalığı tetiklediğini kanıtlamadığını bilerek ekip, tau agregalarının ne kadar kolay “tohumlanabildiğini” raporlayan hücre tabanlı bir sisteme yöneldi. Tau lifleri oluştuğunda parlayacak şekilde tasarlanmış biyosensör hücreler kullandılar. Alzheimer beyinlerinden alınan tau açısından zengin madde eklendiğinde hücreler güçlü bir floresans sinyali üretti. Bu hücrelerde belirli mikroRNA’ları artırıp engelleyerek, hangilerinin tau tohumlamasını değiştirdiğini görebildiler. İki tanesi öne çıktı: miR-146b-5p’yi artırmak tau tohumlamasını kötüleştirirken, engellemek tohumlamayı azalttı; tersine, miR-151a-5p’yi artırmak tau tohumlamasını zayıflatırken, onu engellemek tohumlamayı güçlendirdi. Test edilen diğer mikroRNA’lar bu ölçümde çok az etki gösterdi.
Gelecekte tanı ve tedavi için olası çıkarımlar
Bu mikroRNA’ların ne yapıyor olabileceğini anlamak için yazarlar, öngörülen gen hedeflerini bilinen biyolojik yollarla eşleştirmek amacıyla hesaplamalı araçlar kullandılar. Özellikle miR-129-5p, miR-132-3p ve miR-146b-5p gibi aşağı regüle olan mikroRNA’lar, nöron hayatta kalması, sinapslardaki kimyasal iletişim ve Alzheimer ile ilgili yolları içeren ağlarla ilişkilendirildi. Bu, onların normal “fren” etkisinin kaybının birden fazla koruyucu sistemi aynı anda bozabileceğini; miR-151a-5p’deki artışın ise tau agregasyonuna karşı beynin geç dönem, kısmi bir karşı koyma çabası olabileceğini öne sürer. Bu çalışma ölüm sonrası doku ve basitleştirilmiş hücre modellerine dayanmakla birlikte, belirli mikroRNA’ların tau patolojisini hem yansıttığı hem de modüle ettiği fikrini güçlendiriyor. Uzun vadede, bu moleküllerin omurilik sıvısı veya kanda ölçülmesi hastalık ilerlemesini izlemeye yardımcı olabilir ve beyinlerindeki düzeylerini hassas şekilde ayarlamak toksik tau’nun yayılmasını yavaşlatmak veya önlemek için yeni bir yol sunabilir.
Atıf: Nagaraj, S., Quintanilla-Sánchez, C., Ando, K. et al. Differentially expressed miRNAs in the temporal cortex of Alzheimer’s disease patients and their association to tau pathology. Commun Biol 9, 253 (2026). https://doi.org/10.1038/s42003-026-09530-0
Anahtar kelimeler: Alzheimer hastalığı, mikroRNA, tau patolojisi, temporal korteks, nörodejenerasyon