Clear Sky Science · tr
Gen düzenlemesinin hedefli bloklanması, intron içinde gömülü primer mikroRNA’ları düzensizleştirebilir
Genlerimizin İçindeki Gizli Mesajlar
Birçok yeni gen terapisi, hücrelerimizin RNA iletilerini yönlendirerek çalışıyor, ancak bu RNA’lar genetik metnin kenarına yazılmış ekstra “notlar” barındırabiliyor ve bilim insanları bunları yeni yeni çözmeye başlıyor. Bu makale, genlerin hatalı eklenmesini düzeltmek için tasarlanmış ilaçların, intronların—gen bölümleri arasındaki kodlamayan uzantıların—içine gömülü küçük düzenleyici RNA’ları istemeden yükseltebileceğini ve bunun beyin bağlantıları ve gelişim üzerinde beklenmedik etkileri olabileceğini gösteriyor.
RNA’yı Yeniden Yazabilen Gen Terapileri
Antisens oligonükleotidler (ASO’lar), RNA’ya yapışıp onun nasıl okunup işlendiğini değiştiren kısa sentetik genetik parçacıklardır. Birkaç ASO zaten nadir genetik hastalıklar için test ediliyor veya kullanılıyor; özellikle RNA eklenmesi hatalarından kaynaklanan bozukluklarda. Çoğu güvenlik testi, bir ASO’nun doğru proteini geri getirip getirmediğine ve bariz yan etkilere yol açıp açmadığına odaklanır. Oysa birçok genin intronlarında mikroRNA dahil olmak üzere kodlama yapmayan RNA’lar bulunur. Bu küçük moleküller gen aktivitesini güçlü şekilde ayarlayabilir ve omurgalılarda bilinen mikroRNA’ların yarıya kadarı intronlardan türemektedir. Yeni çalışma şu soruyu soruyor: ASO’larla eklenmeyi zorladığımızda, bu gömülü mikroRNA’lara ne oluyor?
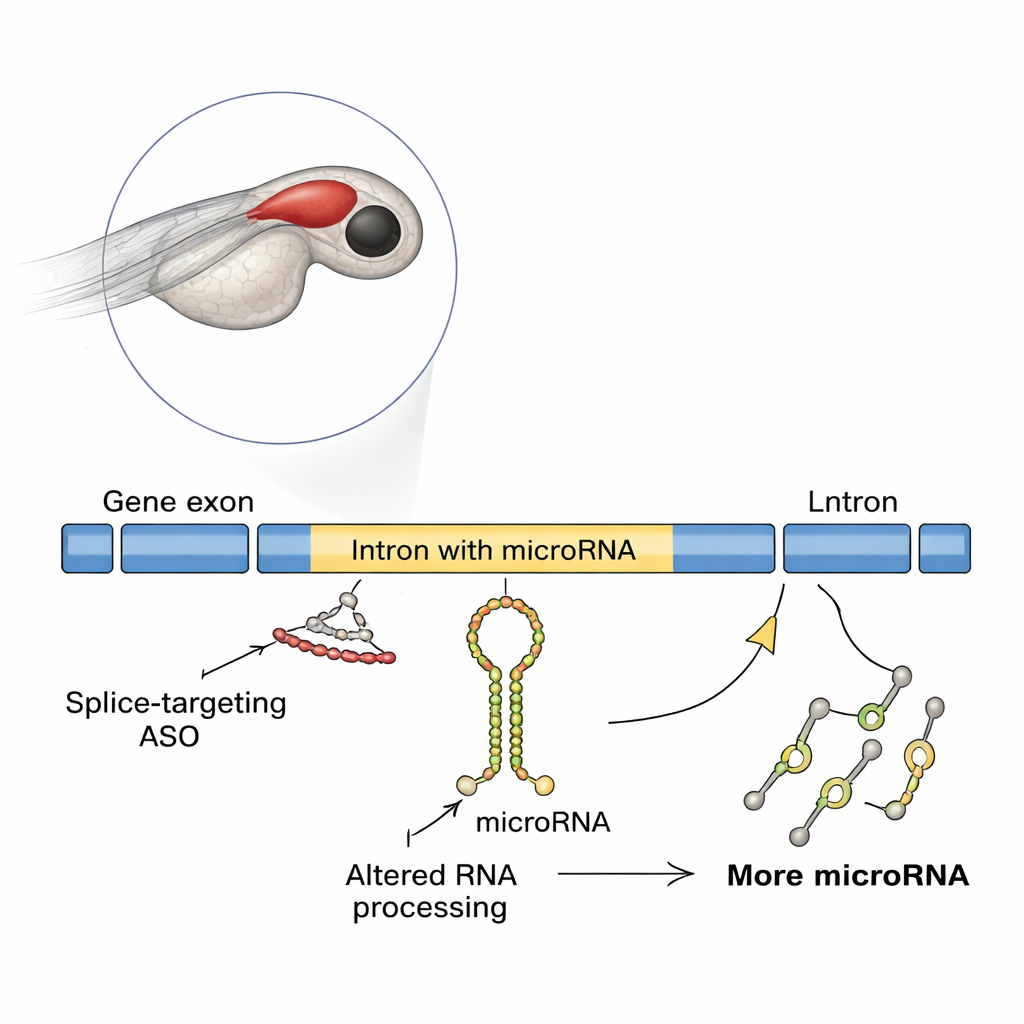
Gelişen Balık Beyinlerinde Beklenmedik Bir Etki
Araştırmacılar, saydam embriyoları sayesinde beyin gelişimini izlemeyi kolaylaştıran popüler bir omurgalı model olan zebrafish’i kullandı. Sinir liflerini yönlendirmeye yardımcı olan ve intronlarından birinin içinde mir-218a-1 adlı bir mikroRNA taşıyan slit3 adlı bir gene odaklandılar. Ekip slit3 çevirisinin başlangıcını engellediğinde, hormon salgılayan hipofiz aksonlarının gelişimi normal görünüyordu. Ancak farklı bir ASO ile slit3’ün belirli bir eklenme (splice) sitesini engellediklerinde, posterior hipofize projeksiyon yapması gereken aksonlar büyük oranda azaldı; buna karşın oksitosin üreten nöron sayısı değişmedi. Moleküler testler, bu splice‑engelleyen ASO’nun genin RNA’sında intron tutulmasına yol açtığını ve beklenmedik şekilde slit3 transkript düzeylerini, uzun intronunu ve intron içine gömülü primer mir-218a-1 transkriptini artırdığını gösterdi.
Protein Kaybı Değil, MikroRNA Bozukluğu Kusuru Sürüklüyor
Aksonel soruna neyin sebep olduğunu ayırt etmek için yazarlar birkaç senaryoyu karşılaştırdı. Yalnızca olgun mir-218a-1’i engellemek slit3 düzeylerini değiştirmedi ve mikroRNA yakınındaki farklı bir eklenme sitesini hedef alan ayrı bir ASO akson kusurlarına veya mir-218a-1 artışına yol açmadı. Kritik olarak, splice‑engelleyen slit3 ASO’su, mir-218a-1’i nötralize eden bir ASO ile birlikte verildiğinde aksonal bağlantılar büyük ölçüde iyileşti. Benzer şekilde, genetik olarak mir-218a-1’den yoksun zebrafish’lerde aynı splice‑engelleyen slit3 ASO’su artık akson kusurlarına yol açmadı; öte yandan sentetik bir mir-218a taklidi normal balıklarda fenotipi taklit edebildi. Bu deneyler, gelişimsel bozulmanın temel sürücüsünün kesilmiş bir Slit3 proteini değil, yükselmiş intronik mikroRNA olduğunu gösteriyor.
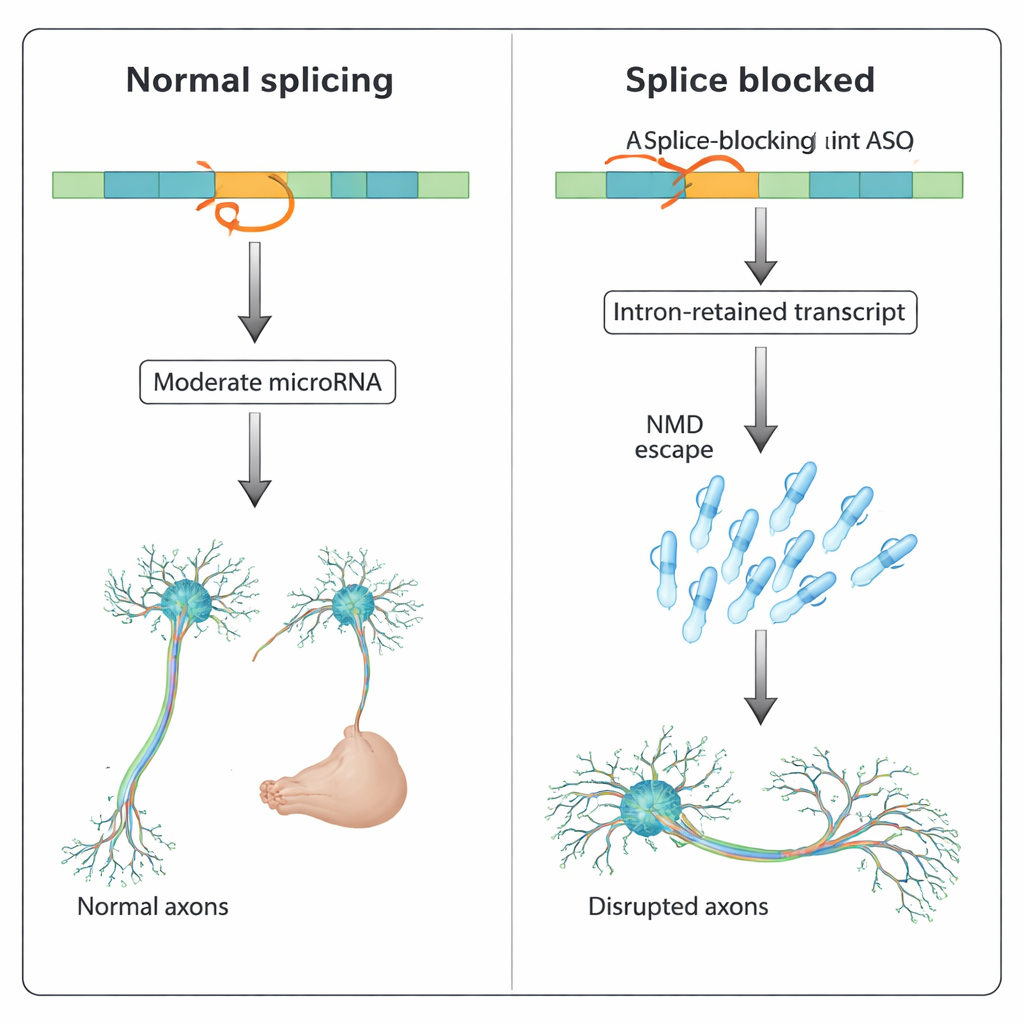
Birden Çok Gende Daha Geniş Bir Desen
Ekip bundan sonra bu etkinin yalnızca slit3’e özgü olup olmadığını sordu. Zebrafish genomunu taradılar ve intronik mikroRNA barındıran onlarca protein‑kodlayan gen buldular; bunların çoğu gelişim ve sinyalizasyonda rol alıyor. Bu genlerden ikisi, pank2 ve dnm2a, daha önce eklenmesi ASO’larla engellendiğinde beyin sıvısı birikimi, kalp şişmesi ve vücut deformiteleri gibi ciddi gelişimsel sorunlar göstermişti—aynı genlerin genetik knockout’ları bu sorunları yeniden üretmemişti. Bu çalışmada, pank2 içindeki mir-103 veya dnm2a içindeki mir-199-5p gibi intronik mikroRNA’ları özgül olarak bloke eden ASO’ların eşzamanlı enjekte edilmesi bu ASO kaynaklı fenotipleri kısmen düzeltti. Bazı durumlarda mikroRNA bloke edilmesi konağın gen ekspresyonunu da geri getirdi; diğerlerinde ise getirmedi; bu da, genel düzeylerde yalnızca ılımlı değişiklikler olsa bile yükselmiş mikroRNA aktivitesinin tek başına zararlı olabileceğini düşündürüyor.
Gelecek Tedaviler İçin Anlamı
Bulgular, splice‑hedefleyen ASO’ların sadece ekzon atlamasına veya intron tutulmasına neden olmayabileceğini; aynı zamanda hücrenin kalite kontrol sisteminden kaçan intron‑tutulan transkriptleri stabilize edebileceğini ve intronik primer mikroRNA’ları artırabileceğini; bunun da hedef gen ağlarını yanlış düzenleyebileceğini ortaya koyuyor. Gelişen nöronlarda böyle kontrolden çıkmış mikroRNA aktivitesi akson büyümesini ve bağlantılanmayı bozabilir. İlaç geliştiriciler için bu, hayvan testlerinde görülen olağandışı veya “hedef‑dışı” fenotiplerin her zaman genel toksisite yollarından (örneğin p53 aktivasyonu) kaynaklanmayabileceği; bunun yerine gizli intronik RNA’lar üzerindeki istem dışı etkilerden ileri gelebileceği anlamına gelir. Çeviri‑engelleyen ve splice‑engelleyen ASO’ların dikkatle karşılaştırılması ve intronik mikroRNA ekspresyonunun izlenmesi, bu riskleri erken aşamada saptamaya ve ASO tasarımlarını hastalara ulaşmadan önce iyileştirmeye yardımcı olabilir.
Atıf: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Anahtar kelimeler: antisens oligonükleotidler, mikroRNA, RNA eklenmesi, zebrafish gelişimi, gen tedavisi güvenliği