Clear Sky Science · tr
MAT2A, SRF aracılığıyla PARN transkripsiyonunu artırarak glikolizi hızlandırır ve osteosarkomda kötü huylu ilerlemeyi tetikler
Bu kemik kanseri çalışması neden önemli
Osteosarkom çocuklar ve gençler arasında en sık görülen kemik kanseridir ve tedaviler onlarca yıldır büyük ölçüde değişmedi. Kanser yayıldığında veya kemoterapiye direnç geliştiğinde birçok genç hasta hâlâ kötü sonuçlarla karşılaşıyor. Bu çalışma, osteosarkom hücrelerinin büyümesine, enerji kullanımını yeniden düzenlemesine ve agresif tümörler oluşturmasına yardımcı olan MAT2A adlı gizli bir “ana anahtar” proteini ortaya koyuyor—ve MAT2A’yı hedef alan bir ilacın laboratuvar modellerinde bu tümörleri yavaşlatabildiğini veya küçültebildiğini gösteriyor.
Tümör hücrelerinin içindeki gizli bir motor
Araştırmacılar işe tek hücre düzeyinde kemik kanseri örneklerini normal kemik dokusuyla karşılaştırarak başladı. Osteosarkom dokusunda daha fazla tümör yapıcı hücre ve daha az bağışıklık hücresi bulundu; özellikle MAT2A adlı bir gen kanser hücrelerinde alışılmadık şekilde aktifti. Kamusal kanser veritabanları ve laboratuvarda yetiştirilen hücre hatlarıyla yapılan analizler MAT2A düzeylerinin sağlıklı kemik hücrelerine göre osteosarkomda çok daha yüksek olduğunu ve MAT2A’sı daha fazla olan hastaların genellikle daha ileri evre hastalığa ve lenf düğümü yayılımına sahip olma eğiliminde olduğunu doğruladı. Bu, MAT2A’yı pasif bir gözlemci yerine hastalığın potansiyel bir sürücü faktörü olarak odak noktasına yerleştirdi.
MAT2A’yı azaltmak kanser büyümesini yavaşlatır
MAT2A’nın tümör davranışı için gerçekten ne kadar önemli olduğunu test etmek için ekip, osteosarkom hücre hatlarında MAT2A düzeylerini genetik araçlarla düşürdü. MAT2A susturulduğunda kanser hücreleri daha yavaş bölündü ve programlı hücre ölümü yaşama olasılıkları arttı. Bu değiştirilmiş hücrelerin implante edildiği farelerde tümörler çok daha yavaş büyüdü ve sonuçta önemli ölçüde daha küçük oldu; hayvanların vücut ağırlığı sabit kaldı. Bu deneyler, osteosarkom hücrelerinin hem hayatta kalma hem de tümör oluşturma yetileri için MAT2A’ya güçlü şekilde bağımlı olduğunu gösterdi.
Hücresel yakıt kullanımını artıran bir sinyal rölesi
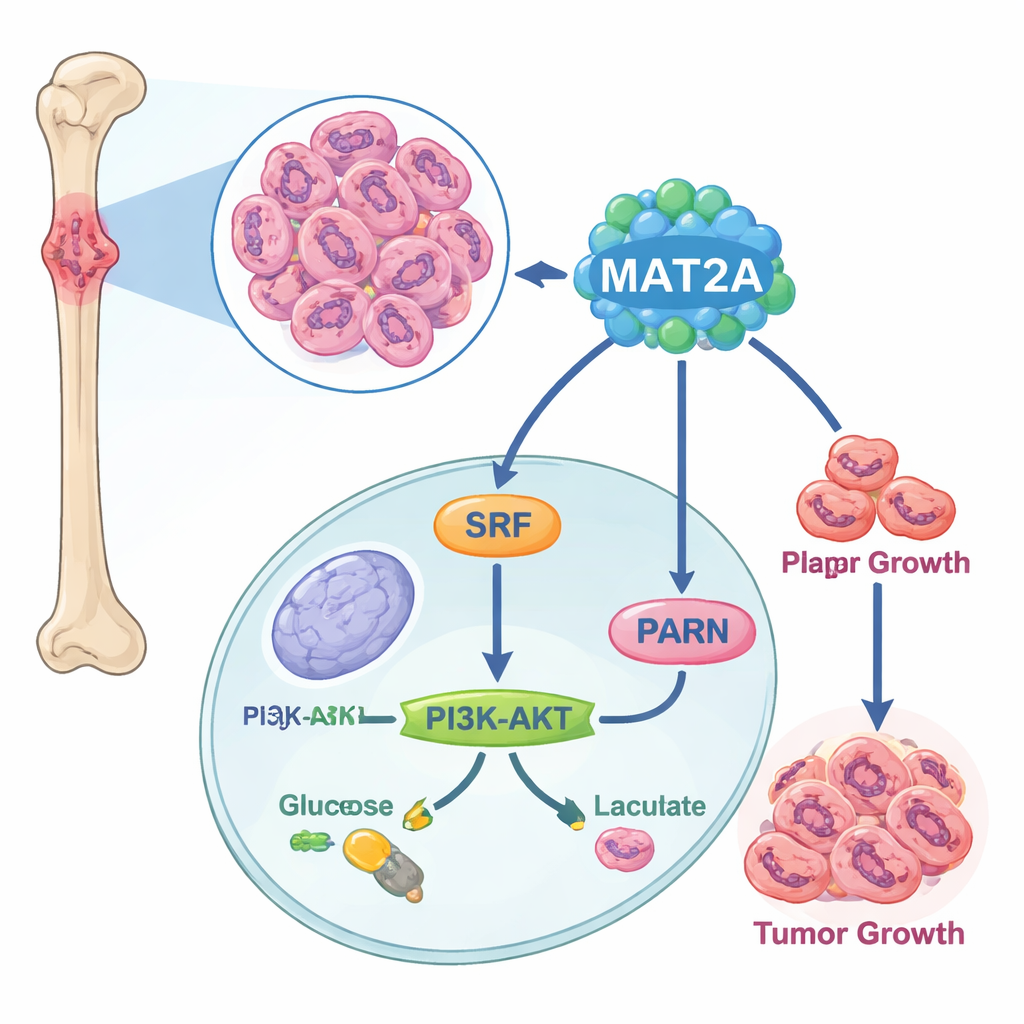
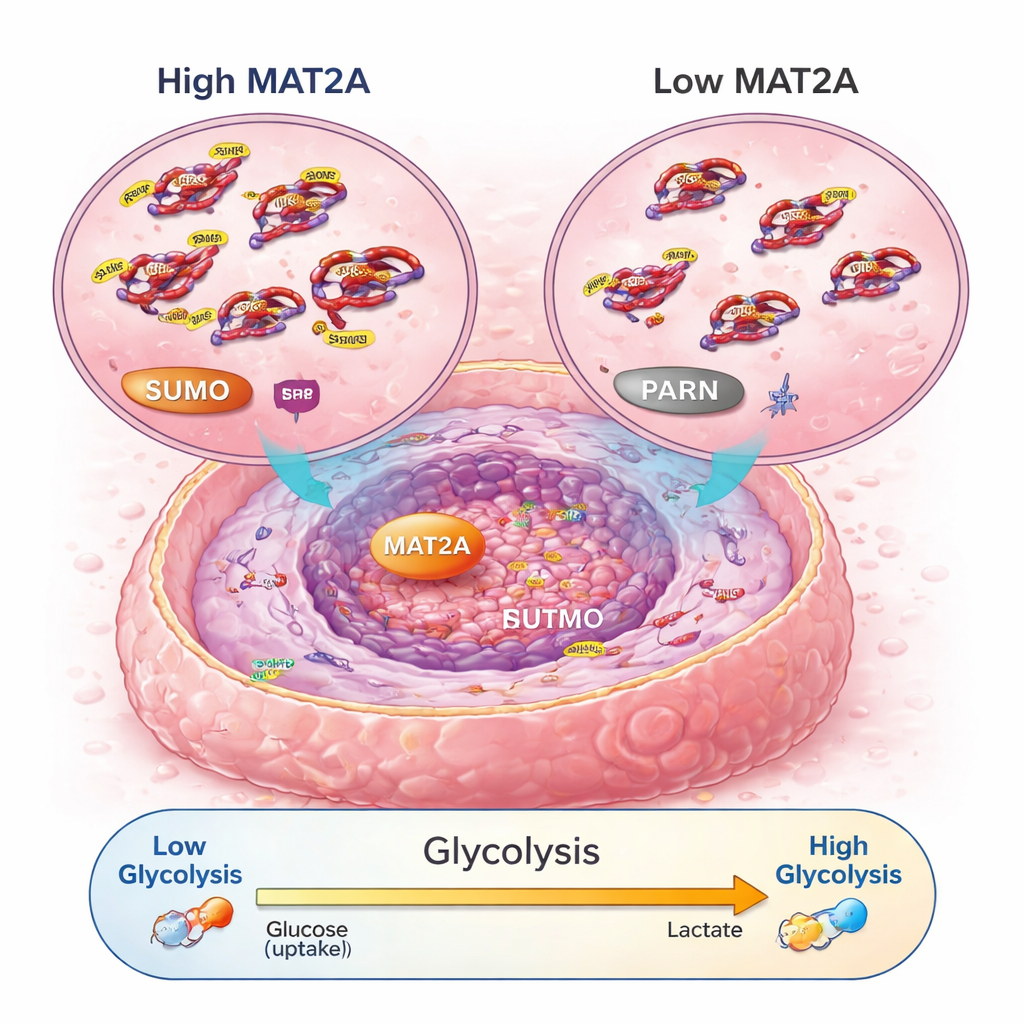
Daha derine indikçe, bilim insanları MAT2A’nın yalnızca olağan metabolik işlevini yerine getirmekten daha fazlasını yaptığını keşfetti. Çekirdeğin içinde MAT2A, SRF adlı bir transkripsiyon faktörüne bağlanıyor; SRF’yi SUMO adı verilen kimyasal bir etiketi teşvik ederek stabil ve aktif tutmaya yardımcı oluyordu. Karşılığında SRF, PARN adlı bir geni etkinleştiriyor; bu da PI3K–AKT yolunu harekete geçiriyor ve hücrelerin tercih ettiği hızlı ama verimsiz bir enerji üretim yolu olan aerobik glikoliz makinesini yükseltiyordu. MAT2A azaltıldığında kanser hücreleri daha az ATP üretti, daha az glukoz aldı, daha az laktik asit üretti ve daha ılımlı, oksijene dayalı solunuma kaydı. PARN veya AKT’yı bozmak MAT2A’nın büyümeyi ve glikolizi teşvik edici etkilerini geri alabiliyordu; bu da MAT2A→SRF→PARN→PI3K–AKT hattının osteosarkomda temel bir enerji ve büyüme devresi olarak işlediğini doğruladı.
Geleneksel olmayan bir rol ve ilaçla hedeflenebilir bir yapı
Dikkat çekici biçimde, normal enzimatik aktivitesinden yoksun bir MAT2A çeşidi bile SRF stabilitesini ve PARN aktivasyonunu destekliyordu; bu da bu kanser teşvik edici rolün olağan kimyasal reaksiyonuna bağlı olmadığını gösteriyordu. Bunun yerine MAT2A, diğer proteinleri organize eden bir iskelet gibi davranıyordu. Bunun pratik sonuçları var: tümörleri zayıflatmak için ilaçların mutlaka katalitik merkezini bloke etmesi gerekmeyebilir. Araştırmacılar MAT2A’yı hedef alacak şekilde tasarlanmış küçük moleküllü bir inhibitör olan FIDAS-5’i hem hücre kültürlerinde hem de fare modellerinde test ettiler. Tedavi nükleer SRF’yi azalttı, PARN ve PI3K–AKT sinyalleşmesini düşürdü, glikolizi baskıladı, hücre büyümesini yavaşlattı ve kanser hücresi ölümünü tetikledi. Farelerde FIDAS-5 tümörleri küçülttü veya yavaşlattı; belirgin kilo kaybı gözlenmedi, bu da bu bağlamda tolere edilebilir yan etkilere işaret ediyor.
Hastalar ve gelecekteki tedaviler için ne anlama geliyor
Uzman olmayanlar için temel mesaj şudur: osteosarkom hücreleri, büyüme programlarını ve şeker yakma motorlarını tam güçle çalıştırmak için MAT2A’ya dayanıyor. Kritik kontrol proteinlerini stabilize ederek ve bir sinyal zincirini güçlendirerek MAT2A tümörlerin daha hızlı büyümesine ve daha agresif hale gelmesine yardımcı olur. Bu proteini gen temelli yöntemlerle veya FIDAS-5 gibi bir ilaçla bloklamak, bu desteği keser; kanser hücreleri yavaşlamak, enerjiyi daha az çılgınca tüketmek ve nihayetinde ölmek zorunda kalır. Bu tür tedaviler kliniğe ulaşmadan önce daha yapılacak çok iş olsa da bu çalışma MAT2A’yı kemik kanseriyle mücadelede umut verici yeni bir hedef olarak konumlandırıyor ve genç hastalar için daha hassas ve daha az toksik tedavilere giden potansiyel bir yol açıyor.
Atıf: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Anahtar kelimeler: osteosarkom, MAT2A, kanser metabolizması, PI3K AKT yolu, hedefe yönelik tedavi