Clear Sky Science · tr
Antikor seyreltme serilerinden elde edilen immün boyamalarda hesaplamalı epitop heterojenliği analizi
Antikor boyama kalitesi neden önemli
Kanser hücrelerini izlemekten enfeksiyonları teşhis etmeye kadar, modern biyoloji hücre içindeki belirli molekülleri "aydınlatan" antikorlara büyük ölçüde dayanır. Yine de birçok laboratuvar sessizce sinir bozucu bir sorunla uğraşır: çok zayıf, çok gürültülü veya yanıltıcı boyamalar. Bu makale, rutin bir antikor-seyreltme serisinden daha fazla bilgi çıkarmaya yarayan pratik, bilgisayar tabanlı bir yöntem tanıtıyor; araştırmacıların boyamalarını daha temiz görüntüler, daha güvenilir ölçümler ve aynı renk kanalında birden fazla hedef boyamanın yeni yolları için ayarlamasına yardımcı oluyor. 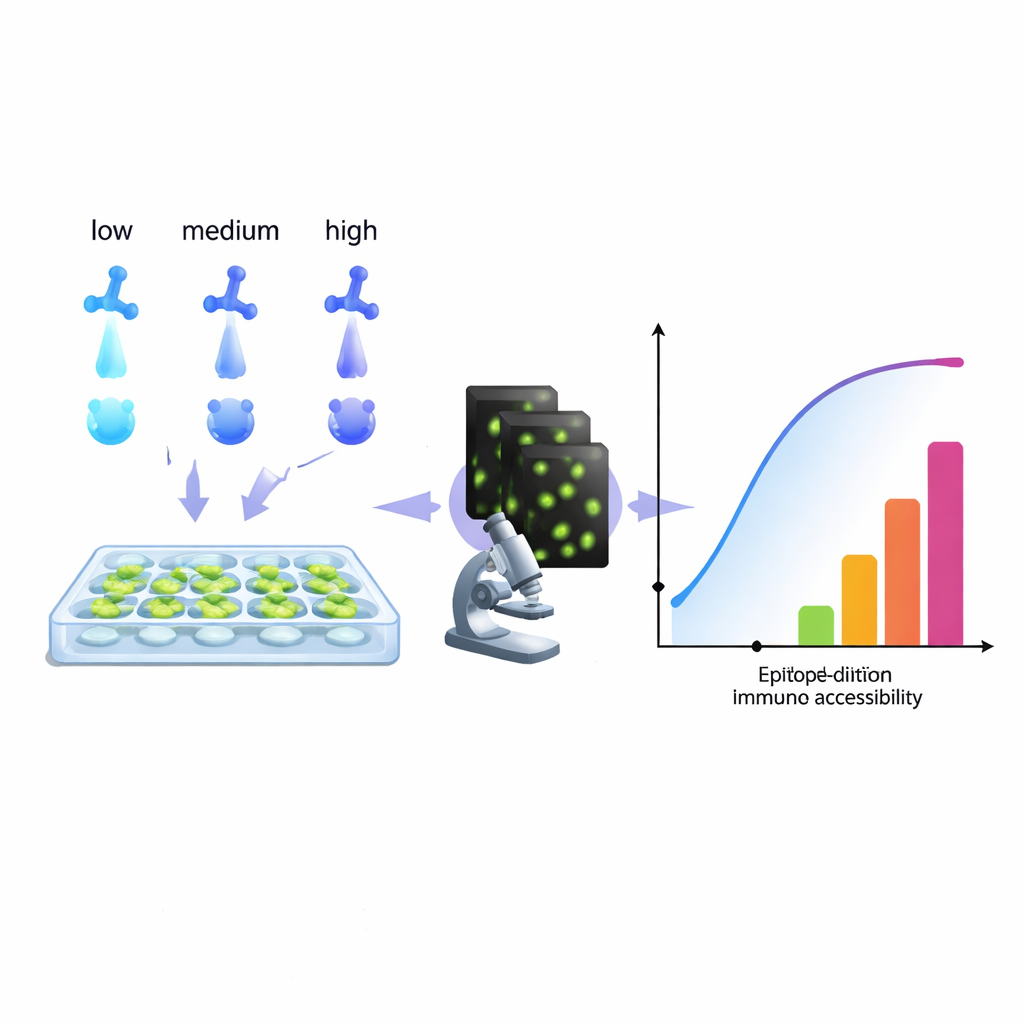
Bilim insanları genellikle antikor boyamalarını nasıl ayarlar
Araştırmacılar bir immün boyama deneyi kurarken genellikle veri sayfasından bir antikor konsantrasyonu tahmin eder, birkaç seyreltme dener ve "güzel görüneni" seçerler. Ancak perde arkasında, protein şekli, hücre içindeki sıkışıklık, pH ve antikorun yerine girme yeteneği gibi sayısız küçük faktör antikorun yapışıp yapışmayacağını belirler. Yüzey plazmon rezonansı gibi geleneksel antikor bağlanma ölçüm araçları, saflaştırılmış proteinler üzerinde ve yapay yüzeylerde en iyi sonuç verir; yoğun hücre veya doku örneklerinde değil. Bu da sağladıkları sayıların, antikorun gerçekte kullanıldığı biyolojik sisteme uymayabileceği anlamına gelir. Sonuç olarak, laboratuvarlar farkında olmadan bulanık arka planı artıran veya daha az erişilebilir önemli hedefleri gizleyen konsantrasyonları seçebilirler.
Basit seyreltme serilerini "erişilebilirlik haritalarına" dönüştürmek
Yazarlar farklı bir yaklaşım öneriyor: standart bir antikor-seyreltme serisini zengin bir veri seti olarak ele almak ve görüntülemenin gerçekten gördüğünü yansıtan—tekrar yıkamadan sonra bile bağlı kalan antikorları—bir modelle uydurmak. Sinyalin konsantrasyonlar boyunca nasıl büyüdüğünü analiz ederek, algoritmaları bir "erişilebilirlik histogramı" yeniden yapılandırıyor. Saf kimyasal bağlanma sabitlerini izole etmeye çalışmak yerine, bu histogram hedef bölgelerini gerçek koşullar altında ne kadar kolay boyanabildiklerine göre teknik "epitop sınıflarına" ayırır. Tek bir biyolojik epitop, örneğin hücrenin bir bölümünde ulaşılması kolayken sıkışık bir bölgede daha zor olduğunda birden fazla sınıfta görünebilir. Kritik olarak, bu yöntem saf proteinlere veya ek donanıma ihtiyaç duymadan doğrudan mikroskop çıktısıyla çalışır; bu yüzden bir seyreltme serisi çalıştırıp floresansı nicelendirilebilen herhangi bir laboratuvar teoride bu tür histogramları oluşturabilir. 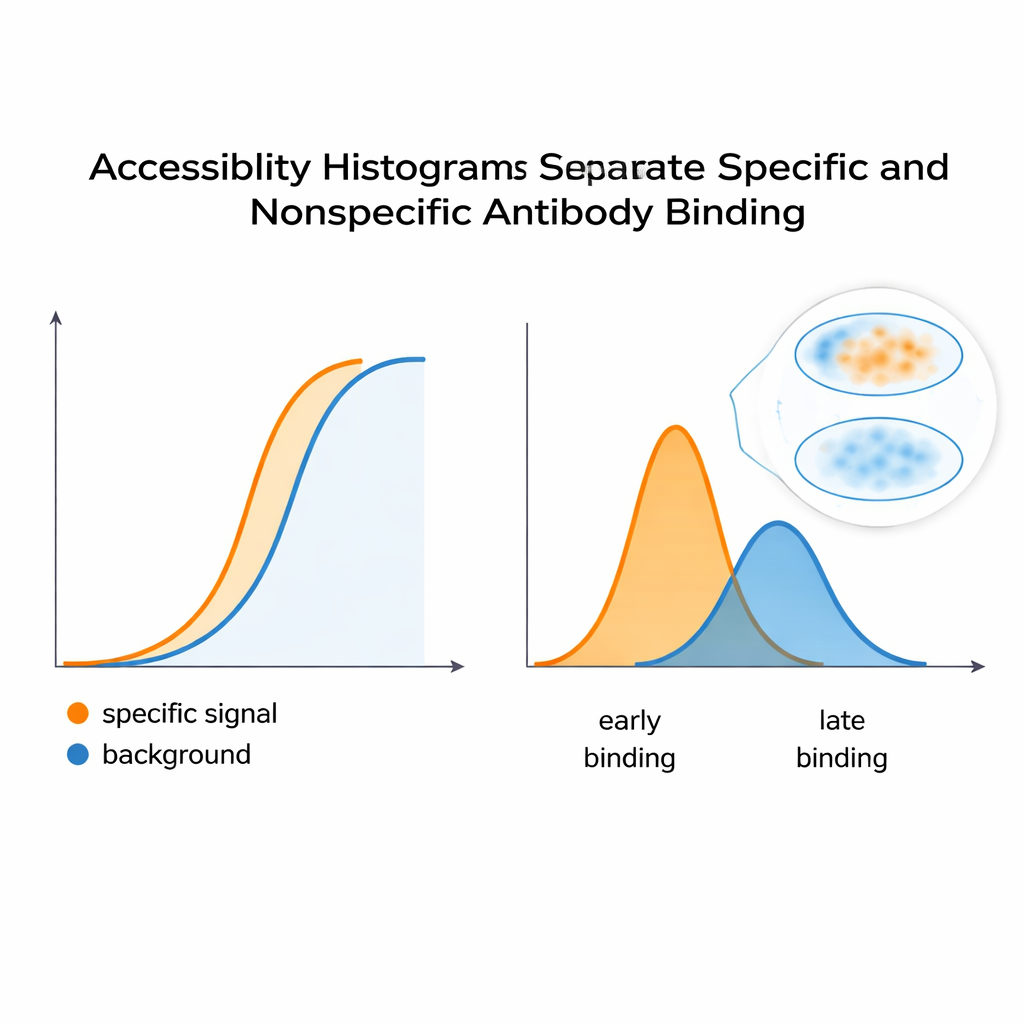
Gerçek sinyali arkadan ayırmak
Bu histogramların gerçekten boyama davranışını yakalayıp yakalamadığını test etmek için ekip, istenen özgül sinyali taklit eden bir monoklonal antikor ve istenmeyen arka plan gibi davranan başka bir antikor kullanan HeLa hücreleriyle kontrollü bir sistem kurdu. Birlikte karıştırıldığında birleşik floresan eğrisi tek, düzgün bir yanıt gibi görünüyordu—hiçbir şey iki ayrı katkıcıyı açıkça göstermiyordu. Ancak hesaplamalı analiz bu eğriyi erişilebilirlik histogramında ayrı tepelere böldü ve en az iki altta yatan epitop sınıfını açığa çıkardı. Şekil-bağımlı bir bölgeyi tanıyan bir PKA düzenleyici alt birimini hedef alan antikora uygulanan benzer bir strateji, cAMP adlı bir molekül tarafından tetiklenen protein konformasyon değişikliklerinin erişilebilir epitopların dağılımını kaydırdığını gösterdi. Bu, yöntemin protein yapılarının açılıp kapanıp kapanmadığını ve bunun hücre içinde antikor bağlanabilirliğini nasıl değiştirdiğini tespit edebileceğini öne sürüyor.
Daha iyi seyreltmeler seçmek ve tek renkle daha çok boyamak
Erişilebilirlik histogramındaki her tepe esasen belirli bir konsantrasyon aralığında katkıda bulunduğundan, yazarlar bu tepeleri "tatlı nokta" seyreltmelerini seçmek için bir rehber olarak kullanıyorlar. Çok yüksek antikor seviyelerinde yalnızca görünen düşük erişilebilirlikteki tepeler muhtemelen özgül olmayan bağlanmayı içerir; oysa erken ortaya çıkan tepeler genellikle amaçlanan hedefi yansıtır. Bireysel tepelerin genel doz–cevap eğrisini nasıl oluşturduğunu modelleyerek ekip, sorunlu tepelerin devreye girmesinden önce özgül sinyali maksimize eden seyreltmeleri önerebiliyor—bazen üretici önerilerinden çok daha seyreltilmiş. Bu fikri ayrıca zekice bir "hesaplamalı çoklama" biçimine genişletiyorlar. Aynı sabit örneği dikkatle seçilmiş konsantrasyonlarla tekrar tekrar boyayarak, her turdan sonra görüntüleyip önceki görüntüleri sonraki görüntülerden çıkararak, farklı erişilebilirlik sınıflarıyla ilişkili sinyalleri izole ediyorlar; böylece tek bir floresan kanalında birden çok hedefi birbirinden ayırıyorlar.
Günlük laboratuvar çalışmaları için ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma rutin bir sorun giderme adımı—bir antikor-seyreltme serisi çalıştırmayı—nicel bir araca dönüştürüyor. Erişilebilirlik histogramları, bilim insanlarının boyamalarındaki gizli karmaşıklığı görmelerine, yanıltıcı arka planı azaltan seyreltmeleri seçmelerine ve bazı durumlarda ek floresan etiketlere ihtiyaç duymadan çakışan sinyalleri ayırmalarına yardımcı oluyor. Temel model kasıtlı olarak basittir ve her moleküler detayı yakalamasa da, kullanımı kolay ve gerçek dünya verileri için yeterince sağlam olacak şekilde tasarlanmıştır. Yaygın olarak benimsenirse, bu yaklaşım antikor tabanlı teknikleri—temel görüntülemeden tanısal testlere kadar—daha güvenilir, daha bilgilendirici ve deneme-yanılmaya daha az bağlı hale getirebilir.
Atıf: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
Anahtar kelimeler: antikor boyama, immünofloresans, epitop erişilebilirliği, doz-cevap, hesaplamalı çoklama