Clear Sky Science · tr
Küçük (<100 kDa) GPCR’lerin kriyo‑EM yapısal çalışmaları için stratejik ilerlemeler
Hücre içi küçük anahtarların tıp için önemi
Modern tıbbın büyük bir kısmı, hücre zarlarımızda yer alan ve G protein‑bağlı reseptörler (GPCR’ler) olarak adlandırılan küçük anahtarları nazikçe dürterek çalışır. Bu anahtarlar hormonları, kokuları ve ilaçları algılar ve onaylanmış ilaçların yaklaşık üçte biri bunları hedef alır. Daha güvenli ve akıllı ilaçlar tasarlamak için bilim insanlarının bu reseptörlerin, özellikle birçok ilacın özgül olarak hedeflediği “kapalı” yani inaktif hallerinin ayrıntılı 3B görüntülerine ihtiyacı vardır. Bu makale, araştırmacıların molekülleri neredeyse doğal halleriyle dondurup görüntüleyebilen güçlü bir yöntem olan kriyo‑elektron mikroskopisi (kriyo‑EM) ile en küçük GPCR’lerden bazılarını nasıl görmeyi öğrendiğini anlatıyor.
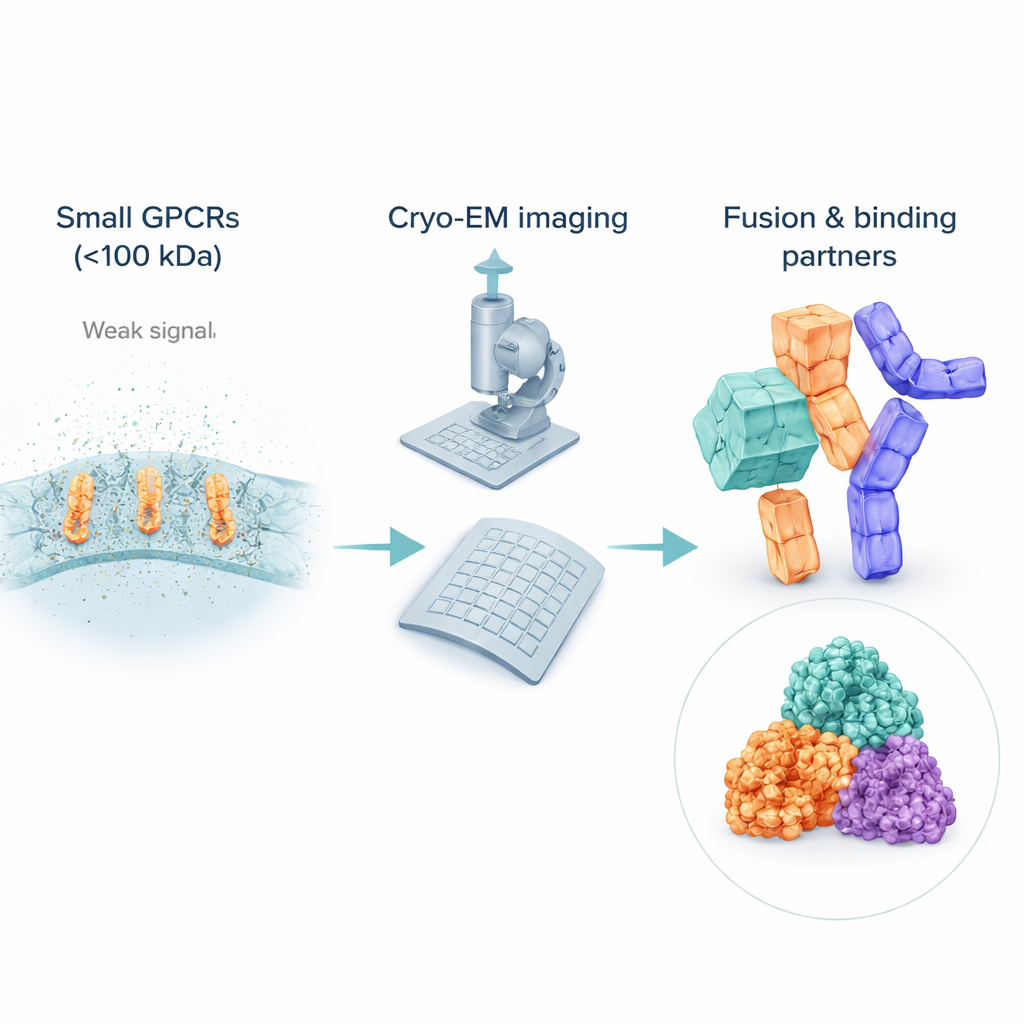
Çok küçük reseptörleri görmenin zorluğu
Kriyo‑EM yapısal biyolojide devrim yaratsa da küçük, esnek moleküllerle başa çıkmakta hâlâ zorlanıyor. Birçok inaktif GPCR 100 kilodaltonun çok altında ağırlığa sahiptir, bu da onları gürültülü görüntülerde tespit etmeyi ve hizalamayı zorlaştırır. Çözünebilir tutmak için bilim insanları bu reseptörleri deterjan kabarcıkları veya lipit taklitleri içine sarar; bu yapılar elektron ışınına reseptörden daha “büyük” görünerek ilgilenilen proteinin sinyalini gölgeleyebilir. G proteinler gibi hacimli ortaklara bağlı aktif reseptörlerin aksine, inaktif GPCR’ler genellikle belirgin dış özelliklerden yoksundur, bu yüzden bilgisayarlar çok sayıda görüntüyü keskin bir 3B görünümde ortalamakta güçlük çeker. Sonuç olarak, inaktif GPCR yapılarının çoğu hala daha eski X‑ışını yöntemlerinden geliyor ve birçok ilacın etki gösterdiği noktada kriyo‑EM kapsamında bir boşluk kalıyor.
Yerleşik yardımcılarla reseptörleri büyütmek
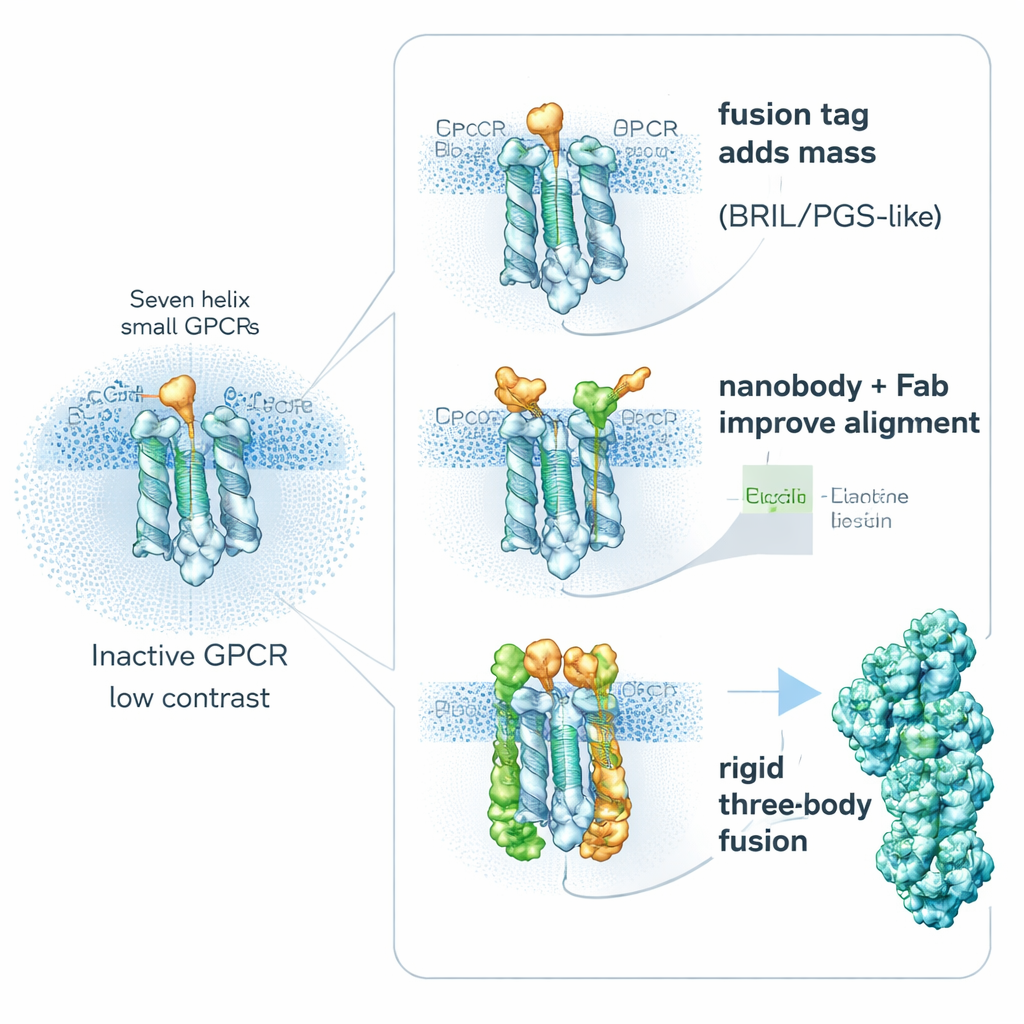
Temel stratejilerden biri şaşırtıcı derecede basittir: reseptörü kasıtlı olarak “daha ağır” yapmak. Araştırmacılar, önemli ilaç bağlanma bölgelerini engellemeden GPCR’lerin esnek kısımlarına küçük, stabil yardımcı proteinleri genetik olarak füzeleyerek boyutlarını ve rijitliklerini artırır. Popüler yardımcılar arasında BRIL (dört‑heliks demeti), PGS (termostabil enzim fragmanı) ve calcineurin adı verilen daha büyük kelepçe‑benzeri bir protein bulunur. Bu füzyon partnerleri genellikle iki heliks arasında bağlantı kuran hareketli bir iç döngüye yerleştirilir. Bu bölgeyi sertleştirerek moleküler hareketten kaynaklanan bulanıklığı azaltır ve bilgisayarların partikülleri hizalamasına yardımcı olan tanınabilir şekiller sağlar. Çalışmalar, füzyon parçasının tam konumu ve yöneliminin bir projenin başarısını belirleyebileceğini gösteriyor: bir reseptörde, PGS etiketinin farklı yerleştirilmesi çözünürlüğü flu 6 Å’den çok daha net 3,7 Å’ye yükseltmişti.
Antikorlar ve tasarımcı bağlayıcıları tutamak olarak ödünç almak
İkinci yol, reseptöre büyük füzyonlar yerleştirmekten kaçınır ve bunun yerine dışarıdan yüksek afiniteli “tutamaklar” bağlar. Nanobody olarak adlandırılan küçük antikor fragmentleri ve benzeri bağlayıcılar, inaktif GPCR’leri tanıyacak şekilde elde edilebilir ve esnek iç döngülere tutunabilir. Öne çıkan bir örnek Nanobody‑6’dır; ilk olarak bir opioid reseptörü için sensör olarak oluşturulmuş ve sonra küçük değişikliklerle birkaç başka GPCR’yi de inaktif halde stabilize etmek için yeniden kullanılmıştır. Merkezi olmayan bir bölgeye bağlandığı için her partiküle net bir yönelim ipucu verir ve görüntü ortalamasını daha güvenilir kılar. Araştırmacılar genellikle bu fikri, nanobody’yi tanıyan sıradan bir antikor fragmenti ekleyerek genişletirler; bu, kriyo‑EM’de net görünen daha hacimli ve daha rijit bir kompleks oluşturur. DARPins gibi diğer mühendislik bağlayıcıları, modüler mesafe elemanları veya daha büyük protein kafeslerine bağlayıcılar olarak kullanılabilir ve çok küçük hedeflerden gelen sinyali daha da artırır.
Daha akıllı örnek tasarımı ve yapay zekâ destekli görüntü işleme
Yardımcıları füzelemek veya bağlayıcılar eklemek hikâyenin sadece bir kısmıdır. Derleme, iyi yapıların dikkatle tasarlanmış reseptör konstrüksiyonlarıyla başladığını vurgular: gevşek kuyruk bölgelerinin kırpılması, stabilize edici mutasyonların tanıtılması ve sorun yaratma olasılığı yüksek parçaları belirlemek için modern yapı tahmin araçlarının kullanılması. Görüntüleme tarafında, zayıf partiküller için kontrastı artıran faz plakaları gibi eski yöntemler, yapay zekâ araçlarıyla tamamlanıyor veya yerini alıyor. Derin öğrenme programları gürültülü mikrograflarda gizlenmiş küçük partikülleri seçebiliyor ve yeni algoritmalar, reseptörler birçok konformasyon örneklediğinde görüntüleri farklı şekillere ayırabiliyor. Fiducial yardımcılarla birlikte bu ilerlemeler, bir zamanlar çalışmak için çok küçük veya çok dinamik olduğu düşünülen zar proteinlerini çözmede kriyo‑EM’yi güvenilir hâle doğru itiyor.
Gelecekteki ilaçlar için bunun anlamı
Makale, tüm reseptörler için işe yarayan tek bir “sihirli” yardımcının olmadığını, ancak füzyon partnerleri, antikor‑benzeri bağlayıcılar ve yapay zekâ destekli yöntemlerden oluşan büyüyen bir araç kutusunun GPCR’lerin inaktif manzarasını kriyo‑EM’e açtığını sonuç olarak belirtir. Uzman olmayanlar için çıkarılacak ana mesaj şudur: küçük reseptörleri mikroskop için daha büyük ve daha düzenli göstererek, bilim insanları birçok ilacın bağlanmayı tercih ettiği tam şekillerin ayrıntılı anlık görüntülerini nihayet elde edebilirler. Bu yapısal planlar, bu hücresel anahtarları daha kesin bir şekilde kapatacak — veya aktivitelerini ince ayar yapacak — ve daha az yan etkiyle ilaç tasarımını hızlandırmalıdır.
Atıf: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Anahtar kelimeler: G protein‑bağlı reseptörler, kriyo‑elektron mikroskopisi, ilaç keşfi, yapısal biyoloji, nanobody iskeletleri